-
有关化学键和晶体的说法中正确的是
A.离子键的本质是静电作用,阴阳离子电荷越大、离子半径越小,静电作用越强
B.共价键的本质是共用电子对,因此必须由成键的两原子各提供一个电子形成
C.分子晶体的基本微粒是分子,分子晶体熔沸点由分子内部共价键强弱决定
D.原子晶体由于是空间网状结构,因此只能由碳、硅两元素构成
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的有几句( )
①离子键与共价键的本质都是静电作用;②任何物质中都存在化学键;③氢键是极弱的化学键;④离子键就是阴、阳离子之间的静电吸引力;⑤活泼金属与活泼非金属化合时能形成离子键;⑥任何共价键中,成键后原子均满足8电子稳定结构;⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电;⑧两种非金属元素形成的化合物不可能含有离子键;⑨化学键断裂,一定发生化学变化
A. 1 B. 2 C. 3 D. 4
高二化学单选题中等难度题查看答案及解析
-
下列关于CaF2的表述正确的是
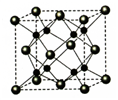
A. Ca2+与F-间仅存在静电吸引作用
B. F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
C. 阴阳离子比为2:1的物质,均与CaF2晶体构型相同
D. CaF2中的化学键为离子键,因此CaF2在晶体状态下能导电
高二化学选择题中等难度题查看答案及解析
-
下列有关晶体的叙述中,正确的是( )
A.离子晶体中阴阳离子的配位数之比等于其电荷数之比
B.石墨可以导电,晶体中含有金属键,因此为金属晶体
C.MCO3中M2+的离子半径越小,分解的温度越高
D.水溶液能导电的晶体一定是离子晶体
高二化学单选题中等难度题查看答案及解析
-
下列说法错误的是( )
A. 离子晶体中阴阳离子间的作用力为静电引力
B. 离子键没有方向性和饱和性
C. 在氯化铯晶体中无CsCl分子单独存在
D. CaF2晶胞中F-的配位数为4
高二化学单选题中等难度题查看答案及解析
-
下列说法不正确的是( )
A. 离子晶体的晶格能越大离子键越强
B. 阳离子的半径越大则可同时吸引的阴离子越多
C. 通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成离子化合物的晶格能越大
D. 拆开1mol离子键所需的能量叫该离子晶体的晶格能
高二化学单选题中等难度题查看答案及解析
-
下列关于晶格能的叙述中正确的是( )
A. 晶格能仅与形成晶体中的离子所带电荷数有关
B. 晶格能仅与形成晶体的离子半径有关
C. 晶格能是指相邻的离子间的静电作用
D. 晶格能越大的离子晶体,其熔点越高
高二化学单选题简单题查看答案及解析
-
下表列出了有关晶体的知识其中错误的是( )
A
B
C
D
晶体
硫化钾
干冰
金刚石
碘
组成晶体的微粒
阴阳离子
分子
原子
分子
晶体微粒间存在的作用力
离子键
共价键
共价键
范德华力
A.A B.B C.C D.D
高二化学单选题简单题查看答案及解析
-
下列说法不正确的是( )
A.离子晶体的晶格能越大,离子键越强
B.阳离子的半径越大则可同时吸引的阴离子越多
C.通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成的离子化合物的晶格能越大
D.拆开1mol离子键所需的能量叫该离子晶体的晶格能
高二化学选择题中等难度题查看答案及解析
-
下列说法不正确的是( )
A.离子晶体的晶格能越大离子键越强
B.阳离子的半径越大则可同时吸引的阴离子越多
C.通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成离子化合物的晶格能越大
D.拆开1mol离子键所需的能量叫该离子晶体的晶格能高二化学选择题中等难度题查看答案及解析