-
[化学——选修3:物质结构与性质](15分)
研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
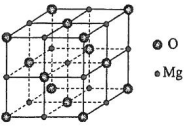
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
高三化学填空题中等难度题查看答案及解析
-
[2017新课标Ⅲ]研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
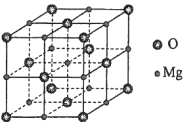
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
高三化学综合题困难题查看答案及解析
-
[2017新课标Ⅲ]研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
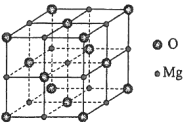
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
高三化学综合题困难题查看答案及解析
-
研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。下列关于该反应的说法中错误的是( )
A.CO2和Mn都属于金属晶体
B.CO2和CH3OH分子中C原子的杂化形式相同
C.该反应利用了H2的还原性
D.干冰晶体中每个CO2分子周围有12个紧邻分子
高三化学多选题中等难度题查看答案及解析
-
研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
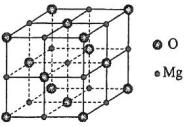
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
高三化学简答题困难题查看答案及解析
-
研究发现,在
低压合成甲醇反应(
)中,
氧化物负载的
氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)
和
分子中
原子的杂化形式分别为__________和__________。
(2)在
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____,原因是_____。
(3)硝酸锰是制备上述反应催化剂的原料,
中的化学键除了
键外,还存在__________。
高三化学填空题中等难度题查看答案及解析
-
研究CO2、CO的利用对促进低碳社会的构建具有重要意义,CO2、CO都可用于合成甲醇。
(1)CO2用于合成甲醇的热化学方程式为:CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H
①该反应的平衡常数表达式为K= 。
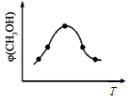
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图所示,则该反应的ΔH 0(填“>”、“<”或“=”)。
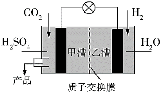
③科学家现正研发的以实现CO2转化为甲醇在常温常压下进行的装置如图所示,写出甲槽的电极反应式______________。
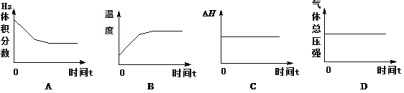
(2)CO用于合成甲醇的热化学方程式为:CO(g)+2H2(g)
CH3OH(g) △H,在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与2a mol H2的混合气体在催化剂作用下发生下面反应2生成甲醇,下列图像正确且说明可逆反应达到平衡状态的是 。(填序号)
(3)以CH4和H2O为原料,也可通过下列反应1和反应2来制备甲醇。
反应1:CH4(g)+ H2O(g)
CO(g)+ 3H2(g) ΔH= + 206.0 kJ·mol-1
反应2:CO(g)+ 2H2(g)
CH3OH(g) ΔH=-129.0 kJ·mol-1
①CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________________。
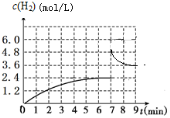
②已知:在700 ℃,1 MPa时,1 mol CH4与1 mol H2O在1 L密闭容器中发生反应1,6min达到平衡(如图),此时CH4的转化率为________________。根据右图分析,由第一次平衡到第二次平衡,平衡向__________方向移动(填“正反应”或“逆反应”),采取的措施可能是_____________________。
高三化学填空题极难题查看答案及解析
-
CO2催化加氢制取甲醇的研究,对于环境、能源问题都具有重要的意义。反应如下:
反应ⅰ:CO2(g) + 3H2(g) ⇌ CH3OH(g) + H2O(g) ∆H1 =﹣58 kJ· mol-1
反应ⅱ:CO2(g) + H2(g) ⇌ CO(g) + H2O(g) ∆H2 = +42 kJ· mol-1
下列说法不正确的是
A.增大氢气浓度能提高二氧化碳的转化率
B.增大压强,有利于向生成甲醇的方向进行,反应ⅰ的平衡常数增大
C.升高温度,生成甲醇的速率加快,反应ⅱ的限度同时增加
D.选用理想的催化剂可以提高甲醇在最终产物中的比率
高三化学单选题中等难度题查看答案及解析
-
反应CO2(g)+3H2(g)
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究人员发现,一定条件下,Pt 单原子催化剂有着高达 90.3%的甲醇选择性。反应历程如图,其中吸附在催化剂表面上的物种用*表示,TS 表示过渡态。
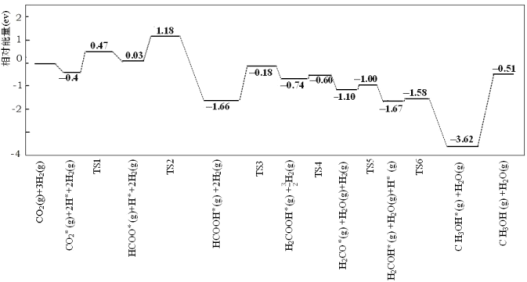
下列说法正确的是
A.该反应的△H>0
B.经历 TS1,CO2共价键发生断裂,且生成羧基
C.能垒(活化能)为 1.48ev 的反应为 HCOOH*(g)+2H2(g)=H2COOH*(g)+
H2(g)
D.如果换用铜系催化剂,所得反应历程与上图相同
高三化学单选题困难题查看答案及解析
-
CO2催化加氢制取甲醇、乙醇等低碳醇的研究,对于环境问题和能源问题都具有非常重要的意义。已知一定条件下的如下反应:
CO2(g) + 3H2(g)
CH3OH(g) + H2O(g) ∆H =-49.0 kJ· mol-1
2CO2(g) + 6H2(g)
CH3CH2OH(g) + 3H2O(g) ∆H=-173.6 kJ· mol-1
下列说法不正确的是
A.CH3OH(g) + CO2(g) + 3H2(g)
CH3CH2OH(g) + 2H2O(g) ∆H<0
B.增大压强,有利于反应向生成低碳醇的方向移动,平衡常数增大
C.升高温度,可以加快生成低碳醇的速率,但反应限度降低
D.增大氢气浓度可以提高二氧化碳的转化率
高三化学单选题中等难度题查看答案及解析