反应 2NO+2CO N2+2CO2 可应用于汽车尾气的净化。下列判断正确的是
A.CO2 是氧化剂 B.NO 是还原剂
C.N2 是氧化产物 D.CO 发生氧化反应
高一化学单选题简单题
反应 2NO+2CO N2+2CO2 可应用于汽车尾气的净化。下列判断正确的是
A.CO2 是氧化剂 B.NO 是还原剂
C.N2 是氧化产物 D.CO 发生氧化反应
高一化学单选题简单题
反应 2NO+2CO N2+2CO2 可应用于汽车尾气的净化。下列判断正确的是
A.CO2 是氧化剂 B.NO 是还原剂
C.N2 是氧化产物 D.CO 发生氧化反应
高一化学单选题简单题查看答案及解析
反应2NO+2CON2+2CO2可应用于汽车尾气的净化。下列判断正确的是
A.该反应是置换反应 B.该反应是复分解反应
C.CO是氧化剂 D.NO发生还原反应
高一化学选择题简单题查看答案及解析
反应2NO+2CON2+2CO2可应用于汽车尾气的净化。下列判断正确的是
A. 该反应是置换反应 B. 该反应是复分解反应
C. 该反应是氧化还原反应 D. 该反应是非氧化还原反应
高一化学null简单题查看答案及解析
反应2NO+2CO=N2+2CO2可应用于汽车尾气的净化。下列判断正确的
A. 该反应是置换反应 B. 该反应是复分解反应
C. 该反应是氧化还原反应 D. 该反应是分解反应
高一化学单选题简单题查看答案及解析
反应2NO+2CO N2+2CO2 是汽车尾气的净化原理。下列判断正确的是
A. 该反应是置换反应 B. 该反应是复分解反应
C. CO发生氧化反应 D. NO是还原剂
高一化学选择题中等难度题查看答案及解析
2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
汽车尾气净化的主要原理为:2NO(g)+2CO(g)2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。

据此判断:
(1)该反应的ΔH____(填“>”或“<”)0。
(2)在T2温度下,0~2 s内的平均反应速率v(N2)=____。
(3)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。___________________
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____(填代号)。
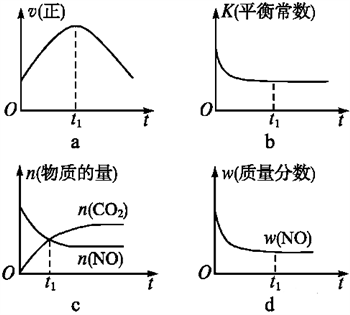
高一化学填空题中等难度题查看答案及解析
近年来,雾霾天气成为我国华北地区乃至全国的环境问题之一。
Ⅰ汽车尾气是空气污染的重要原因。汽车尾气净化原理为:
2NO(g)+2CO(g)2CO2(g)+N2(g) △H <0。
(1)该反应的平衡常数表达式为____________________。
(2)在一恒容的绝热容器(不与外界发生热交换)中模拟上述反应。下面各示意图正确且能说明反应在t1时刻达到平衡状态的是__________。
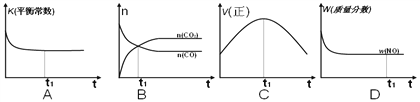
Ⅱ煤燃烧产生的烟气中含有大量硫、氮的氧化物,会引起严重的环境污染问题。
(1) 硫、氮的氧化物都会形成酸雨。为减少酸雨产生,下列措施中不可行的有_______(填序号)。
a.少用煤作燃料 b.把工厂的烟囱加高 c.燃料脱硫
d.燃煤时鼓入足量空气 e.开发新能源
(2)煤燃烧产生的氮的氧化物可以用CH4催化还原。已知:
CH4(g) + 2NO2(g) = N2(g) +CO2(g) + 2H2O(g) △H =-867kJ/mol
2NO2(g) = N2O4(g) △H =-56.9kJ/mol
H2O(l) = H2O(g) △H =+44kJ/mol
写出CH4(g) 还原N2O4(g)生成N2(g) 、CO2(g)和H2O(l)的热化学方程式________________。
高一化学填空题困难题查看答案及解析
近年来,雾霾天气成为我国华北地区乃至全国的环境问题之一。
Ⅰ汽车尾气是空气污染的重要原因。汽车尾气净化原理为:
2NO(g)+2CO(g)2CO2(g)+N2(g) △H <0。
(1)该反应的平衡常数表达式为____________________。
(2)在一恒容的绝热容器(不与外界发生热交换)中模拟上述反应。下面各示意图正确且能说明反应在t1时刻达到平衡状态的是__________。
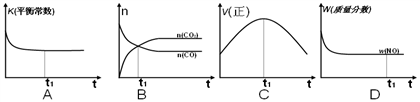
Ⅱ煤燃烧产生的烟气中含有大量硫、氮的氧化物,会引起严重的环境污染问题。
(1) 硫、氮的氧化物都会形成酸雨。为减少酸雨产生,下列措施中不可行的有_______(填序号)。
a.少用煤作燃料 b.把工厂的烟囱加高 c.燃料脱硫
d.燃煤时鼓入足量空气 e.开发新能源
(2)煤燃烧产生的氮的氧化物可以用CH4催化还原。已知:
CH4(g) + 2NO2(g) = N2(g) +CO2(g) + 2H2O(g) △H =-867kJ/mol
2NO2(g) = N2O4(g) △H =-56.9kJ/mol
H2O(l) = H2O(g) △H =+44kJ/mol
写出CH4(g) 还原N2O4(g)生成N2(g) 、CO2(g)和H2O(l)的热化学方程式________________。
高一化学填空题困难题查看答案及解析
反应2NO+2CON2+2CO2可应用于汽车尾气的净化,下列关于该反应的说法正确的是( )
A.升高温度能减慢反应速率
B.使用恰当的催化剂能加快反应速率
C.减小NO浓度能加快反应速率
D.NO与CO反应时能100%转化为N2和CO2
高一化学单选题简单题查看答案及解析
每到冬季,雾霾天气肆虐京津冀等地区。其中,燃煤和汽车尾气是造成空气污染的原因之一。
(l)汽车尾气净化的主要原理为:2NO(g)+2CO(g)2CO2(g)+N2(g)△H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________________(填代号)。
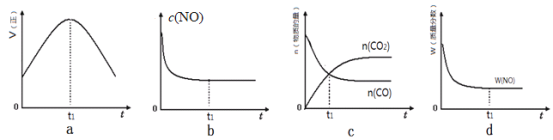
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)N2O4(g) △H=-56.9 kJ/mol ②
H2O(g)=H2O(l) △H=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式__________________。
(3)甲烷燃料电池可以提升能量利用率。
①碱性介质中甲烷燃料电池的负极反应式_________________________。
②如果电路上有0.1mol电子通过,理论上消耗标准状况下氧气的体积为_______。
(4)已知燃料电池的比能量与单位质量的燃料失去的电子数成正比。理论上,氢气、甲烷、甲醇燃料电池的比能量从大到小的顺序是_________。
高一化学综合题中等难度题查看答案及解析