-
“稀土之父”徐光宪对稀土萃取分离做出了巨大贡献。稀土是隐形战机、超导、核工业等高精尖领域必备的原料。钪(Sc)是稀土金属之一,如图是制备Sc的工艺流程。
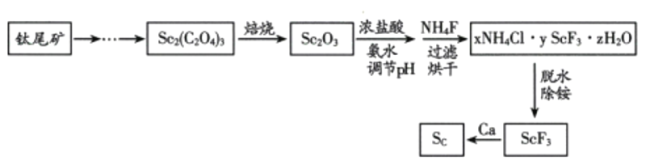
已知:xNH4Cl•yScF3•zH2O是ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。“脱水除铵”是复盐沉淀的热分解过程。
据此回答:
(1)在空气中焙烧Sc2(C2O4)3只生成一种碳氧化物的化学方程式为 ________。
(2)图1是含Sc元素的离子与F-浓度和pH的关系。用氨调节溶液pH,调节3.5<pH<4.2原因是________。

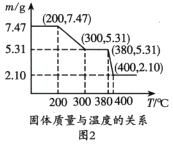
(3)图2是“脱水除铵”过程中固体质量与温度的关系,其中在380℃到400℃会有白烟冒出,保温至无烟气产生,即得到ScF3,由图像中数据计算复盐中x:z=________;工艺流程中可回收利用的物质是________。
(4)传统制备ScF3的方法是先得到ScF3•6H2O沉淀,再高温脱水得ScF3,但通常含有ScOF杂质,原因是________(用化学方程式表示)。流程中将复盐沉淀后“脱水除铵”制得纯度很高的SeF3,其原因是________。
-
钇钡铜氧、汞钡铜氧、汞钡钙铜氧等都是常见的高温超导体。回答下列问题:
(1)钇(39Y)是一种重要的稀土金属,基态Y原子的价电子排布式为______。下列科学家中,在稀土化学领域做出重要贡献的是_________(填标号)。
a.侯德榜 b.屠呦呦 c.徐光宪
(2)BaCO3可用于制备上述高温超导体,其3种组成元素中,第一电离能最大的是______(填元素符号),CO32-的空间构型为________,其中碳原子的杂化方式为________________。
(3)汞钡铜氧晶体的晶胞如下图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。

汞钡铜氧晶体的密度为______g·cm-3(设NA为阿伏加德罗常数的值)。图A晶胞中钡离子的分数坐标为( )和_________。掺杂Ca2+所得超导材料的化学式为_________。
)和_________。掺杂Ca2+所得超导材料的化学式为_________。
-
我国著名的化学家、教育家徐光宪先胜因在稀土金属等研究领域做出杰出贡献,荣获了2008年度“国家最高科学技术奖”。 是地壳中含量最高的稀土金属饰元素。下列关于
是地壳中含量最高的稀土金属饰元素。下列关于 的说法错误的是
的说法错误的是
A.质量数为140 B 中子数为82
C.质子数为58 D 核外电子数为198
-
平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质).某课题以此粉末为原料,资源回收的工艺流程如下:
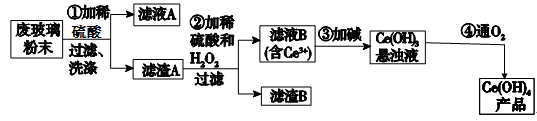
(1)铈(Ce)是稀土元素之一,萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP应满足的条件________________________。
(2)写出第①步反应的离子方程式________________________________,第①步不能用浓盐酸的理由____________________________________________
(3)第①步洗涤滤渣A,检验滤渣A是否洗净的方法是___________________________,写出第②步反应的化学方程式________________________________
(4)工业上利用上述回收的资源以及焦炭、氯气、氢气制取纯硅,写出制取纯硅的相关化学方程式_______________________________________________
(5)取上述流程中得到的Ce(OH)4 产品0.5g ,加硫酸溶解后,用0.1000mol/LFeSO4 标准溶液滴定到终点时( 还原产物为Ce3+ ),消耗20mL 标准溶液,该产品中Ce(OH)4 的质量分数为__________(保留小数点后一位)。
-
著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石 ,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
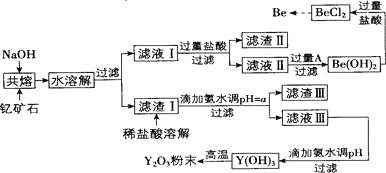
已知:
 钇
钇 的常见化合价为
的常见化合价为 价;
价;
 铍和铝处于元素周期表的对角线位置,化学性质相似;
铍和铝处于元素周期表的对角线位置,化学性质相似;
 、
、 形成氢氧化物沉淀时的pH如下表:
形成氢氧化物沉淀时的pH如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2:1 | 3:1 |
| Y3+ | 6.0 | 8.3 |
 将钇矿石与NaOH共熔的反应方程式补充完整:
将钇矿石与NaOH共熔的反应方程式补充完整:
_____ _____
_____ _____
_____ _____
_____ _____
_____ _____
_____ _____
_____ _____
_____
 滤渣Ⅱ的主要成分是_________。
滤渣Ⅱ的主要成分是_________。
 试剂A可以是_________
试剂A可以是_________ 填序号
填序号 。
。
A NaOH溶液  氨水
氨水 

 用氨水调节
用氨水调节 时,a的取值范围是_____________。
时,a的取值范围是_____________。
 计算常温下
计算常温下 的平衡常数
的平衡常数 ____________。
____________。 常温下
常温下
 滤液Ⅲ加入氨水产生沉淀的离子方程式为___________。
滤液Ⅲ加入氨水产生沉淀的离子方程式为___________。
 从
从 溶液中得到
溶液中得到 固体的操作是_______。
固体的操作是_______。
-
著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
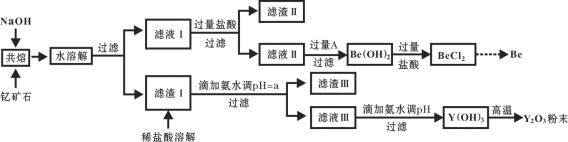
已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |
(1)将钇矿石与NaOH共熔的反应方程式补充完整:
__Y2FeBe2Si2O10+__NaOH+____  __Y(OH)3 +__Fe2O3 + __Na2SiO3 + __Na2BeO2 + __H2O
__Y(OH)3 +__Fe2O3 + __Na2SiO3 + __Na2BeO2 + __H2O
(2)滤渣Ⅱ的主要成分是____________。
(3)试剂A可以是___________。
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是_____________________。
(5)计算常温下Y3+ +3H2O Y(OH)3+3H+的平衡常数K=________。(常温下Ksp [Y(OH)3] = 8.0×10-23)
Y(OH)3+3H+的平衡常数K=________。(常温下Ksp [Y(OH)3] = 8.0×10-23)
(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为_______________。
(7)从BeCl2溶液中得到BeCl2固体的操作是________。
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由_________。
-
近年来我国政府强化了对稀土元素原料的出口管制,引起了美、日等国家的高度关注与不满。所谓“稀土元素”是指镧系元素及第五周期ⅢB族的钇(39Y),它们被称为“工业味精”。它们在军工生产、高科技领域中有极为重要的作用,下列有关“稀土元素”的说法正确的是 ( )。
A. 它们的原子核外均有5个电子层
B. 它们的原子最外层均含有3个电子
C. 它们均是金属元素
D. 76Y、80Y中子数不同,化学性质不同
-
近年来我国政府强化了对稀土元素原料的出口管制,引起了美、日等国家的高度关注与不满。所谓“稀土元素”是指镧系元素及第五周期ⅢB族的钇(39Y),它们被称为“工业味精”。它们在军工生产、高科技领域中有极为重要的作用,下列有关“稀土元素”的说法正确的是 ( )。
A.它们的原子核外均有5个电子层
B.它们的原子最外层均含有3个电子
C.它们均是金属元素
D.76Y、80Y中子数不同,化学性质不同
-
稀土元素在发光材料、储氢材料、激光材料、催化剂、高温超导材料等方面有重要应用.下列关于稀土元素4421Sc(钪)的说法不正确的是( )
A.是一种核素
B.原子核内有23个中子
C.与4721Sc互为同位素
D.比4721Sc少3个电子
-
2019年诺贝尔化学奖授予了锂离子电池领域做出巨大贡献的三位科学家。某锂离子电池 为负极,
为负极, 为正极,锂盐有机溶液作电解质溶液,电池反应为
为正极,锂盐有机溶液作电解质溶液,电池反应为 则下列有关说法正确的是
则下列有关说法正确的是
A.金属锂的密度、熔点和硬度均比同族的碱金属低
B.该锂离子电池可用乙醇作有机溶剂
C.电池放电时,Li+从正极流向负极
D.电池充电时,阳极的电极反应式为






