-
碳、氮、铜形成的单质及它们形成的化合物有重要研究和应用价值,回答下列问题:
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结简式如图所示。
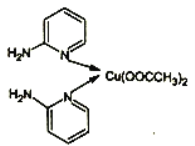
①基态Cu原子的价电子排布式为_________,在元素周期表中铜位于_________区(填“s”“p”“d”或“ds”)。
②C、N、O三种元素的第一电离能由大到小的顺序为_________。
③邻氨基吡啶的铜配合物中,Cu2+的配位数是_________,N原子的杂化类型为_________。
(2)C60是富勒烯族分子中稳定性最高的一种,N60是未来的火箭燃料,二者结构相似。
①有关C60和N60的说法中正确的是_________。
A.C60和N60均属于分子晶体 B.N60的稳定性强于N2
C.C60中碳原子是sp3杂化 D.C60易溶于CS2、苯
②近年来,科学家合成了一种具有“二重结构”的球形分子,它是把足球形分子C60容纳在足球形分子Si60中,则该分子中含有的化学键类型为___________ (填“极性键”“非极性键”)。
(3)原子坐标参数和晶胞参数是晶胞的两个基本参数。
①图中原子坐标参数分别为:A(0,0,0),B(1/2,1/2,0),C(1/2,0,1/2),则D的原子坐标参数为_________。
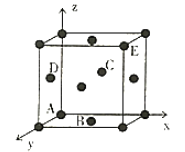
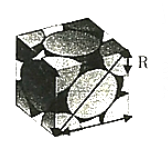
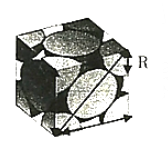
②图为铜的晶胞,铜原子半径为Rnm,NA是阿伏加德罗常数的值,则铜晶体的密度为_________g·cm-3(用含R、NA的式子表示)
-
碳、氮、铜形成的单质及它们形成的化合物有重要研究和应用价值,回答下列问题:
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结简式如图所示。

①基态Cu原子的价电子排布式为_________,在元素周期表中铜位于_________区(填“s”“p”“d”或“ds”)。
②C、N、O三种元素的第一电离能由大到小的顺序为_________。
③邻氨基吡啶的铜配合物中,Cu2+的配位数是_________,N原子的杂化类型为_________。
(2)C60是富勒烯族分子中稳定性最高的一种,N60是未来的火箭燃料,二者结构相似。
①有关C60和N60的说法中正确的是_________。
A.C60和N60均属于分子晶体 B.N60的稳定性强于N2
C.C60中碳原子是sp3杂化 D.C60易溶于CS2、苯
②近年来,科学家合成了一种具有“二重结构”的球形分子,它是把足球形分子C60容纳在足球形分子Si60中,则该分子中含有的化学键类型为___________ (填“极性键”“非极性键”)。
(3)原子坐标参数和晶胞参数是晶胞的两个基本参数。
①图中原子坐标参数分别为:A(0,0,0),B(1/2,1/2,0),C(1/2,0,1/2),则D的原子坐标参数为_________。
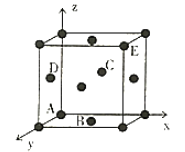
②图为铜的晶胞,铜原子半径为Rnm,NA是阿伏加德罗常数的值,则铜晶体的密度为_________g·cm-3(用含R、NA的式子表示)
-
氮、硒形成的单质及其化合物有重要的科学研究价值,请回答下列问题:
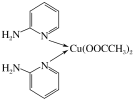
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。基态氮原子的价电子轨道表示式为______________;其核外电子共占据____个能级;邻氨基吡啶的铜配合物中Cu2+的配位数是_______。
(2)高聚氮晶体结构如图所示,每个氮原子与另外三个氮原子结合形成空间网状结构。固态高聚氮是_______晶体;该晶体中n(N)与n(N—N)之比为_______;这种高聚氮N—N键的键能为160 kJ·mol-1,而N2的键能为942 kJ·mol-1,其可能潜在的应用是__________。

(3)NO3-的空间构型是________;HNO3的酸性比HNO2强,试从结构的角度解释其原因__________。
(4)硒有三种晶体(α单斜体、β单斜体和灰色三角晶),灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如图所示:
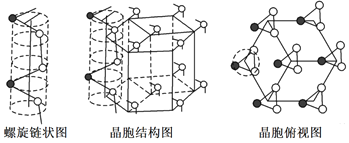
已知正六棱柱的边长为a cm,高为b cm,阿伏加德罗常数的值为NA,则该晶体的密度为_____g·cm-3(用含NA、a、b的式子表示)。
-
国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。
(1)邻氨基吡啶( )的铜配合物在有机不对称合成中起催化诱导效应。
)的铜配合物在有机不对称合成中起催化诱导效应。
①邻氨基吡啶中所有元素的电负性由小到大的顺序为__(填元素符号)。设NA为阿伏加德罗常数的值,1mol 中含有σ键的数目为__。
中含有σ键的数目为__。
②一定条件下-NH2可以被氧化成-NO2,-NH2中N原子的杂化方式为__杂化。
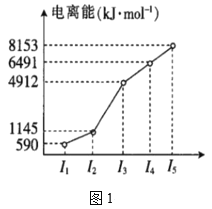
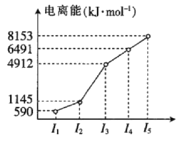
(2)第四周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素的基态原子电子排布式为___。
①嘌呤中轨道之间的夹角∠1比∠2大,原因是___。
② 分子中的大π键可以用符号
分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
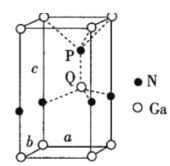
(3)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图3所示。
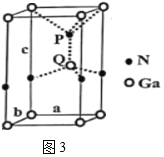
若该晶体密度为dg·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120o,阿伏加德罗常数的值为NA,则晶胞参数c=__(写出代数式)nm。
-
Ⅰ.邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图甲所示。
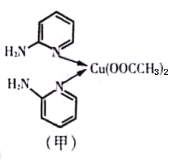
(1)基态Cu原子的价电子排布式为__________________。在元素周期表中铜位于_____区(填“s”、“P”、“d”或“ds”)
(2)C、N、O第一电离能由大到小的顺序为________________。
(3)邻氨基吡啶的铜配合物中,Cu2+的配位数是___________,N原子的杂化类型为_____________。
(4)如图乙所示,Fe3O4.晶体中,O2-围成正四面体空隙(1、3.6、7号氧围成)和正八面体空隙(3、6、7、8、9、12号氧围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中,晶体中正四面体空隙与正八面体空隙数之比为___________,有_______________%的正八面体空隙没有填充阳离子。
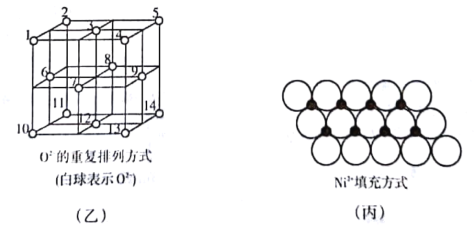
(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图丙),已知O2-的半径为a nm,每平方米面积上分散的该晶体的质量为________g(用a、NA表示)。
-
国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物,科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。
请回答下列问题:
(1)邻氨基吡啶( )的铜配台物在有机不对称合成中起催化诱导效应。
)的铜配台物在有机不对称合成中起催化诱导效应。
①邻氨基吡啶中所有元素的电负性出小到大的顺序为__(填元素符号)。设NA为阿伏加德罗常数的值,1mol 中含有σ键的数目为__。
中含有σ键的数目为__。
②一定条件下-NH2可以被氧化成-NO2,-NO2中N原子的杂化方式为__杂化。
(2)第四周期的某主族元素,其第一至第五电离能数据如图所示,则该元素的基态原子电子排布式为___。
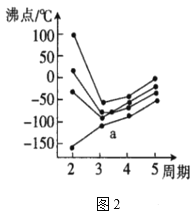
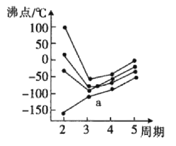
(3)元素周期表中的第IVA族~第VIIA族中部分元素的最简单氢化物的沸点变化趋势线如图,其中一个小黑点代表-种氢化物,则趋势线a代表第__族元素的最简单氢化物的沸点变化趋势,判断依据是__。
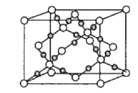
(4)干冰是常见的分子晶体,而CO2在高温高压下能形成另一种晶体其晶胞如图所示,该CO2晶体的熔点__(填“>”“<”或“=”)SiO2晶体的熔点。
(5)一种嘌呤和一种吡啶的结构如图。
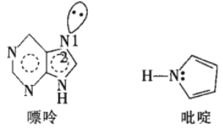
①嘌呤中轨道之间的夹角∠1比∠2大,原因是__。
②分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
(6)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图所示。若该晶体密度为dg·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c=___nm(写出代数式)。
-
吡啶类化合物是合成医药、农药、香料、染料等产品的重要原料。现有一种新型的N,O一二齿配体吡啶类化合物(A),将它和ZnEt2反应后可以得到含锌的有机化合物(B),其具有优异的催化性能。
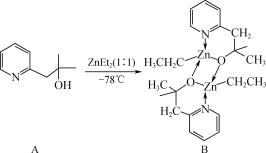
(1)基态Zn原子核外电子排布式为________。
(2)1 mol化合物A中含有的σ键数目为________。
(3)化合物A能与水以任意比例互溶,这是因为______________________________。
(4)化合物A中碳原子轨道的杂化类型为________,化合物B中含有________(填字母)。
a. 极性共价键 b. 非极性共价键 c. 配位键 d. 氢键
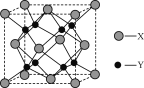
(5)某化合物甲具有与吡啶类化合物相似的性质,其晶胞结构如图所示,其中X原子的配位数为________。
-
端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
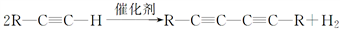
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
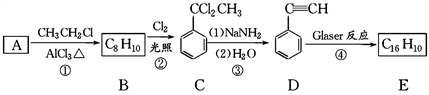
回答下列问题:
(1)B的结构简式为_______________,D的化学名称为________。
(2)①和③的反应类型分别为________、________。
(3)反应④ 化学反应方程式为______________________。
(4)下列说法不正确的是(____)
A.用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气4mol;
B.E分子中处于同一条直线上的原子最多有8个;
C.C分子的核磁共振氢谱面积比为1:2:2:3
D.可用酸性高锰酸钾溶液鉴别A和B
(5)化合物( )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为:_______________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为:_______________________。
(6)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为 3∶1,符合该条件的同分异构体有_______种。
(7)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线 _____________________。
-
端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
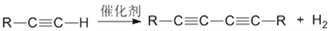
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:
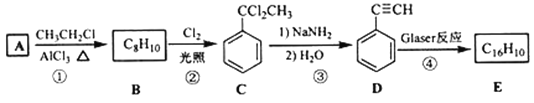
回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(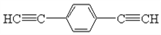 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
-
端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
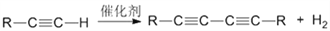
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(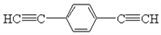 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。





















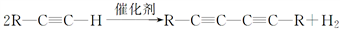

 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为:_______________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为:_______________________。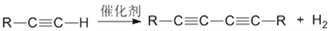

 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。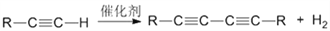

 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。