-
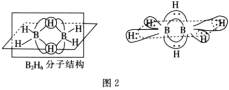
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:

(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
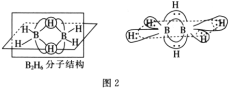
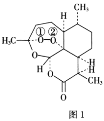
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知 ≈1.414,结果保留三位有效数字)。
≈1.414,结果保留三位有效数字)。
-
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:
(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知 ≈1.414,结果保留三位有效数字)。
≈1.414,结果保留三位有效数字)。
-
青蒿素是从黄花蒿中提取的一种无色针状晶体,双氢青蒿素是青蒿素的重要衍生物,抗疟疾疗效优于青蒿素,请回答下列问题:
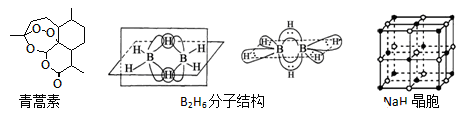
(1)组成青蒿素的三种元素电负性由大到小排序是__________,画出基态O原子的价电子排布图__________。
(2)一个青蒿素分子中含有_______个手性碳原子。
(3)双氢青蒿素的合成一般是用硼氢化钠(NaBH4)还原青蒿素.硼氢化物的合成方法有:
2LiH+B2H6=2LiBH4; 4NaH+BF3═NaBH4+3NaF
①写出BH4﹣的等电子体_________(分子、离子各写一种);
②B2H6分子结构如图,2个B原子和一个H原子共用2个电子形成3中心二电子键,中间的2个氢原子被称为“桥氢原子”,它们连接了2个B原子.则B2H6分子中有______种共价键,B原子的杂化方式为________ ;
③NaBH4的阴离子中一个B原子能形成4个共价键,而冰晶石(Na3AlF6)的阴离子中一个Al原子可以形成6个共价键,原因是______________;
④NaH的晶胞如图,则NaH晶体中阳离子的配位数是_________;设晶胞中阴、阳离子为刚性球体且恰好相切,求阴、阳离子的半径比 =__________。
=__________。
-
青蒿素是从复合花序植物黄花蒿中提取得到的一种有效的疟疾治疗药物。查阅资料知:常温下,青蒿素为无色针状晶体,味道较苦,难溶于水,易溶于有机溶剂,熔点为 ;从青蒿中提取青蒿素的方法主要有乙醚浸提法和溶剂汽油浸提法。
;从青蒿中提取青蒿素的方法主要有乙醚浸提法和溶剂汽油浸提法。
回答下列问题:
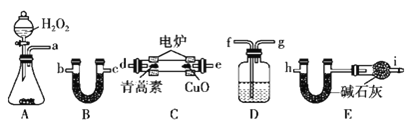
(一)用乙醚浸提法提取青蒿素的流程如下图:

(1)对青蒿进行破碎的目的是______。
(2)操作Ⅰ所用到的玻璃仪器是______,操作Ⅱ的仪器选择及安装都正确的是______(填标号)。
(3)操作Ⅲ的主要过程可能是______。
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(二)青蒿素分子式的测定
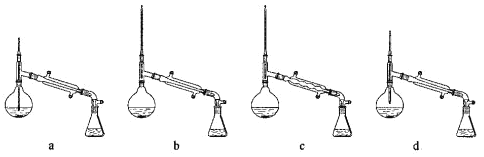
用如图所示的实验装置测定青蒿素的分子式,将28.2 g青蒿素放在燃烧管C中充分燃烧:
(4)①仪器各接口的连接顺序从左到右依次为______ 每个装置限用一次
每个装置限用一次 ;
;
②装置E中干燥管的作用是______;
③装置D中的试剂为______;
④已知青蒿素分子中只含碳、氢、氧三种元素,用合理连接后的装置进行实验,测量数据如表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
则青蒿素分子中碳、氢、氧三种原子的个数比为______。
-
2015年,中国药学家屠哟坳获得诺贝尔生理学和医学奖,其突出贡献是创制新型抗疟药青蒿素和双氢青蒿素。青蒿素是从黄花篙中提取得到的一种无色针状晶体,双氢青蒿素是青蒿素的重要衍生物,抗疟疾疗效优于青蒿素。请回答下列问题:

(1)组成青蒿素的三种元素电负性由大到小排序是_________,画出基态O原子的价电子排布图_________。(2)一个青蒿素分子中含有_________个手性碳原子;
(3)双氢青蒿素的合成一般是用硼氢化钠(NaBH4)还原青蒿素。硼氢化物的合成方法有:
2LiH+B2H6=2LiBH4 4NaH+BF3=NaBH4+3NaF
①写出BH4-的等电子体_________ (分子、离子各写一种);
②1976年,美国科学家利普斯康姆(W.N.Lipscomb)因提出多中心键的理论解释B2H6的结构而获得了诺贝尔化学奖。B2H6分子结构如图,2个B原子和一个H原子共用2个电子形成3中心二电子键,中间的2个氢原子被称为“桥氢原子”,它们连接了2个B原子。则B2H6分子中有_________种共价键,B原子的杂化方式为_________。
③NaBH4的阴离子中一个B原子能形成4个共价键,而冰晶石(Na3AlF6)的阴离子中一个Al原子可以形成6个共价键,原因是_________。
④NaH的晶胞如图,则NaH晶体中阳离子的配位数是_________;设晶胞中阴、阳离子为刚性球体且恰好相切,求阴、阳离子的半径比 =_________。
=_________。
-
青蒿素是一种有效的抗疟药。常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃。提取青蒿素的方法之一是乙醚浸取法,提取流程如下:
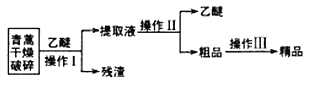
请回答下列问题:
(l)对青蒿进行破碎的目的是__________________。
(2)操作I用到的玻璃仪器是__________,操作Ⅱ的名称是_______。
(3)用下列实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
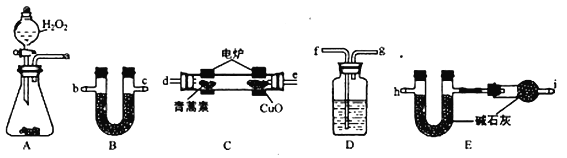
① 仪器各接口的连接顺序从左到右依次为_______(每个装置限用一次)。A装置中发生的化学反应方程式为_________________。
② 装置C中CuO的作用是_________________。
③ 装置D中的试剂为_________________。
④ 已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验.测量数据如下表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
则青蒿素的最简式为__________。
(4)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH 、酚酞的水溶液中,青蒿素的溶解度较小,加热并搅拌,青蒿素的溶解度增大,且溶液红色变浅,与青蒿素化学性质相似的物质是______(填字母代号)。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
-
青蒿素是一种有效的抗疟药。常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃。提取青蒿素的方法之一是乙醚浸取法,提取流程如下:
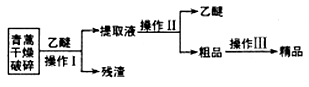
请回答下列问题:
(l)对青蒿进行破碎的目的是__________________。
(2)操作I用到的玻璃仪器是__________,操作Ⅱ的名称是_______。
(3)用下列实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
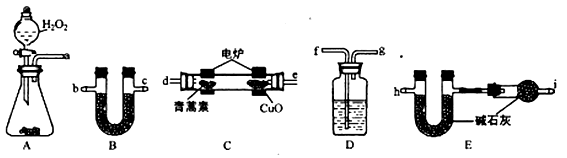
① 仪器各接口的连接顺序从左到右依次为_______(每个装置限用一次)。A装置中发生的化学反应方程式为_________________。
② 装置C中CuO的作用是_________________。
③ 装置D中的试剂为_________________。
④ 已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验.测量数据如下表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
则青蒿素的最简式为__________。
(4)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH 、酚酞的水溶液中,青蒿素的溶解度较小,加热并搅拌,青蒿素的溶解度增大,且溶液红色变浅,与青蒿素化学性质相似的物质是______(填字母代号)。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
-
从青蒿中提取青蒿素的方法之一是以萃取原理为基础的。乙醚浸取法的主要工艺如图所示:
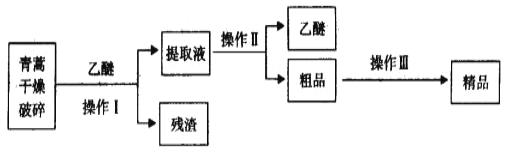
已知:青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差,青蒿素是高效的抗疟药。乙醚沸点为35℃。下列叙述错误的是( )
A.对青蒿干燥破碎后,加入乙醚的目的是溶解青蒿素
B.操作Ⅰ需要的玻璃仪器主要有烧杯、漏斗、玻璃棒
C.操作Ⅱ的名称是过滤
D.操作Ⅲ的主要过程可能是加95%的乙醇,浓缩、结晶、过滤
-
(15分) 【化学 ― 选修 3 物质结构与性质】
氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
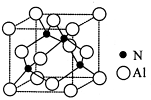
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因 是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
-
常温下,青蒿素为无色针状晶体,难溶于水,易容有机溶剂,熔点为156-157℃。青蒿素是一种有效的抗疟药,某化学兴趣小组对青蒿素的提取和组成进行如下的探究。
Ⅰ.提取青高素的方法之一是乙醚浸取法,提取流程如下:
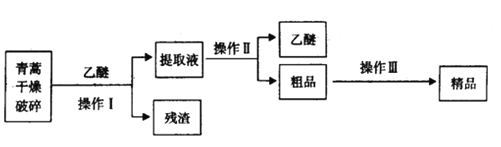
(1)对青蒿进行破碎的目的是___________
(2)操作Ⅰ用到的玻璃仪器是__________,操作Ⅱ的名称是__________
Ⅱ.燃烧法测定青蒿素的最简式:
利用下列实验装置,将28.2g青蒿素放在燃烧管C中充分燃绕,测出生成的CO2和H2O的质量后,计算得出青蒿素的最简式。
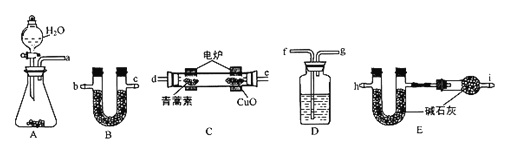
主要实验步骤如下:
①组装仪器,并检查装置的气密性。
②先将A装置的药品反应一会后,再将C装置通电反应。
③称量有关装置的实验前后的质量。
请回答下列问题:
(3)仪器各接口的连接顺序从左到右依次为_____(每个装置限用一次)。
(4)①装置B中的试剂为________,其作用是__________。
②装置C中CuO的作用是__________。
③装置D中的试剂为______,其作用是________________。
④装置E中的试剂为______,其作用是________________。
⑤装置F中的试剂为______,其作用是_________________。
(5)已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E | 80.2 | 146.2 |
则青蒿素的最简式为_____________.


≈1.414,结果保留三位有效数字)。














