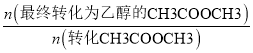-
乙酸甲酯的催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式如下:CH3COOCH3(l)+C6H13OH(l) CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
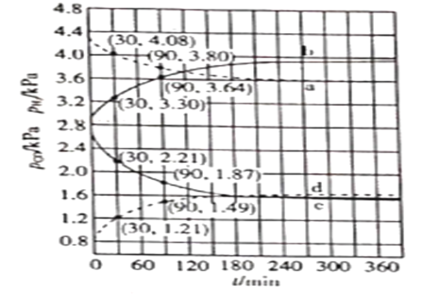
已知v正=k正×x(CH3COOCH3) ×x(C6H13OH),v逆=k逆×x(CH3COOC6H13) ×x(CH3OH),其中是k正、k逆为速率常数(受温度影响),x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1:1投料,测得338K、343K、348K三个温度下CH3COOCH3转化率( )随时间(
)随时间( )的变化关系如图所示。下列说法正确的是
)的变化关系如图所示。下列说法正确的是

A.该反应的△H>0
B.348K时,该反应的平衡常数为1.8
C.A、B、C、D四点中,v正最大的是D
D.在曲线①、②、③中,k正与k逆的差值最大的曲线是①
-
乙酸甲酯催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为: CH3COOCH3(l) +C6H13OH (l)  CH3COOC6H13(l) +CH3OH(l)
CH3COOC6H13(l) +CH3OH(l)
反应开始时,己醇和乙酸甲酯按物质的量之比 1:1 投料,测得 348 K、343 K 两个温度 下乙酸甲酯转化率(α)随时间(t)的变化关系如下图所示:
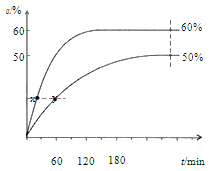
下列说法不正确的是
A.该醇解反应的ΔH > 0
B.反应速率:v(x)> v(y)
C.343K时,以物质的量分数表示的化学平衡常数 Kx=2.25
D.348K时,初始投料 分别按 1:1和2:1进行,Kx 相同
分别按 1:1和2:1进行,Kx 相同
-
乙酸甲酯的催化醇解反应可用于制备甲醇和乙酸已酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l) CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正·x(CH3COOCH3)·x(C6H13OH),v逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响),x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1:1投料,测得338K、343K、348K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是( )
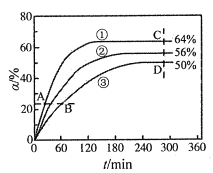
A.该反应的△H>0
B.348K时,该反应的平衡常数为1.8
C.A、B、C、D四点中,v正最大的是D
D.在曲线①、②、③中,k正-k逆最大的曲线是①
-
聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l) CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)反应开始时,已醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。
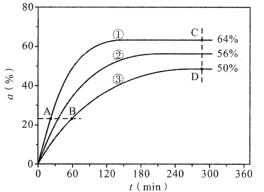
该醇解反应的ΔH____0(填>或<)。348K时,以物质的量分数表示的化学平衡常数Kx=____(保留2位有效数字)。在曲线①、②、③中,k正-k逆值最大的曲线是____;A、B、C、D四点中,v正最大的是___,v逆最大的是____。
(2)343K时,己醇和乙酸甲酯按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比____时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx___(填增大、减小或不变)。
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是____。
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
-
某项目由乙酸甲酯为原料在催化剂作用下制备乙醇,过程包括以下3个主要反应:
Ⅰ.CH3COOCH3(g)+2H2(g)  C2H5OH(g) + CH3OH(g) △H1
C2H5OH(g) + CH3OH(g) △H1
Il.CH3COOCH3(g)+ C2H5OH(g)  CH3COOC2H5(g)+ CH3OH(g) △H2
CH3COOC2H5(g)+ CH3OH(g) △H2
III.CH3COOCH3(g)+H2(g)  CH3CHO (g) + CH3OH(g) △H3
CH3CHO (g) + CH3OH(g) △H3
(1)乙醇的燃烧热为-1366.8kJ· mol—1,写出乙醇的燃烧热化学方程式______.
(2)相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性如下图所示.
例如:乙醇的选择性=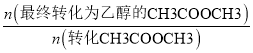
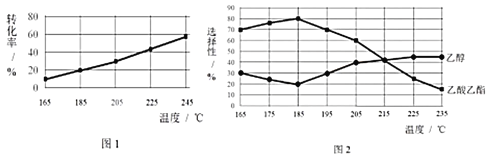
①已知:ΔH1<0.随温度降低,反应I化学平衡常数的变化趋势是____________
②下列说法不合理的是_____________
A.温度可影响反应的选择性
B.225℃~235℃,反应I处于平衡状态
C.增大H2的浓度,可以提高CH3COOCH3的转化率
③为防止“反应Ⅲ”发生,反应温度应控制的范围是____________,结合图像说明判断理由:______
④在185℃下,CH3COOCH3起始物质的量为5mol,生成乙醇的物质的量是_________
-
聚乙烯醇具有亲水性和成膜性,在适宜的浓度下,能起类似人工泪液的作用,作为润滑剂预防或治疗眼部刺激症状。聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l) CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)“洗衣凝珠”是由一层薄膜包裹洗衣液制成的新型洗涤产品,该薄膜的主要化学成分是可溶于水的聚乙烯醇(简称PVA)塑料,聚乙烯醇的化学式为(C2H4O)n,试回答:聚乙烯醇属于_____(填“金属材料”、“有机合成材料”、“硅酸盐材料”、“复合材料”之一),从物质结构的角度解释聚乙烯醇具有亲水性的原因___________________________。
(2)343K时,乙酸甲酯和己醇按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比____时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx___(填增大、减小或不变)。
(3)反应开始时,已醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。
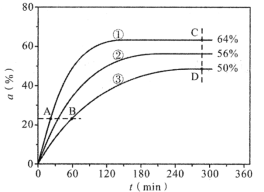
该醇解反应的ΔH____0(填>或<)。348K时,以物质的量分数表示的化学平衡常数Kx=____(保留2位有效数字)。A、B、C、D四点中,v逆最大的是___,v正最大的是____。
(4)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是____。
a.参与了醇解反应,但并不改变反应历程 b.提高乙酸甲酯的平衡转化率
c.提高了醇解反应的活化能 d.使k正和k逆增大相同倍数
-
一氧化碳和氢气是重要的化工原料,常用于合成甲醇、二甲醚、甲酸甲酯等有机物。
(1)已知 的燃烧热分别是
的燃烧热分别是 ,则甲醇与一氧化碳催化合成乙酸的热化学方程式为_____________。
,则甲醇与一氧化碳催化合成乙酸的热化学方程式为_____________。
(2)有人设想将 按下列反应除去
按下列反应除去 ,该反应能否自发进行______________(填“是”或“否”),依据是_____________。
,该反应能否自发进行______________(填“是”或“否”),依据是_____________。
(3)向体积可变的密闭容器中投入 和
和 ,在不同条件下发生反应:
,在不同条件下发生反应: 。测得
。测得 的平衡转化率随温度、压强的变化如图所示。
的平衡转化率随温度、压强的变化如图所示。
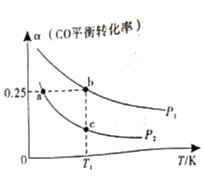
①该可逆反应的 __________0(填>”、“<”或“=”)。a、b、c三点对应的平衡常数
__________0(填>”、“<”或“=”)。a、b、c三点对应的平衡常数 的大小关系是____________________。
的大小关系是____________________。
②在恒温恒容条件下进行该反应,能表示反应达到平衡状态的是______________(填字母)。
a. CO的体积分数保持不变
b. 容器内混合气体的密度保持不变
c.容器内混合气体的平均摩尔质量保持不变
d.单位时间内消耗CO的浓度等于生成 的浓度
的浓度
(4)在催化剂作用下, 时分别进行反应:
时分别进行反应: ,
, ,测得CO和
,测得CO和 的分压随时间的变化关系如图所示。起始时,体系中
的分压随时间的变化关系如图所示。起始时,体系中 和
和 相等、
相等、 和
和 相等。计算曲线a的反应在
相等。计算曲线a的反应在 内的平均速率
内的平均速率 _______
_______ 。
。 时
时 随时间变化关系的曲线是_______,
随时间变化关系的曲线是_______, 时
时 随时间变化关系的曲线是___________。
随时间变化关系的曲线是___________。
(5)一定条件下, 与粉末状氢氧化钠反应生成甲酸钠。已知:常温时,甲酸的电离平衡常数
与粉末状氢氧化钠反应生成甲酸钠。已知:常温时,甲酸的电离平衡常数 。向
。向 的甲酸钠溶液中加入
的甲酸钠溶液中加入 的盐酸,混合液呈__________性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为__________________。
的盐酸,混合液呈__________性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为__________________。
-
甲醇(CH3OH)是重要的有机化工原料,可用于制取氢气、甲酸甲酯(HCOOCH3)。(1) 在一定条件下用氧气催化氧化甲醇制氢气,原料气中n(O2)/n(CH3OH)对反应的选择性影响如图所示(选择性越大表示生成的该物质越多)。当n(O2)/n(CH3OH)=0.25 时,主要反应的化学方程式为____________,制备H2 时最好控制n(O2)/n(CH3OH)=___________。

(2)甲醇催化脱氢制甲酸甲酯的反应为:2CH3OH(g) HCOOCH3(g)+2H2(g) △H =a kJ·mol-1
HCOOCH3(g)+2H2(g) △H =a kJ·mol-1
①已知 :CO(g)+ l/2O2(g)=CO2(g) △H1 =-283kJ·mol-1
2CH3OH(g)+O2(g)=2CO2(g)+4 H2(g) △H2 =-386kJ·mol-1
2CO(g)+2 H2(g)=HCOOCH3(g ) △H3 =-134kJ·mol-1
a=_________________。
②在310℃下,将2mol 甲醇置于VL恒容密闭容器中,反应20 分钟后到达平衡,平衡时甲醇和氢气的分压相等。从开始到平衡时甲醇的平均反应速率为____ mol·L-1·min-1,若平衡时气体总压为P总=5×104Pa,Kp=_______。(已知: Kp是用平衡气体分压代替平衡浓度求得的平衡常数。气体分压=气体总压×气体的物质的量分数)。若在310℃下,将2mol 甲醇置于VL恒压密闭容器中,反应到达平衡时甲醇的分压______氢气的分压(填“>”,“=”或“<”)。
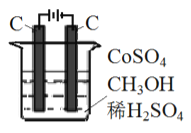
(3) 电解法可消除甲醇对水质造成的污染,原理是: 通电将Co2+ 氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,请写出:
①阴极的电极反应式_______________________________________。
②除去甲醇的离子方程式为_________________________。
-
“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂,其化学名称为“乙酸三氯甲基苯甲酯”,通常以三氯甲基苯基甲醇和醋酸酐为原料制备:
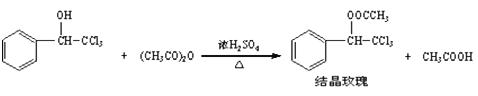
已知:

操作步骤如下:
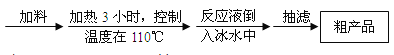
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和酷酸酐,然后慢慢加入浓硫酸并______,待混合均匀后,最适宜的加热方式为______(填“水浴加热”或“油浴加热”)。
(2)粗产品的成分是结晶攻瑰与少量_______(填名称)的混合物,设计了如下方案进行提纯和检验。请完成表中内容:
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将粗产品溶解在中,按粗产品、溶剂的质量比为1:__混合,用水浴加热到70℃回流溶剂使粗产品充分溶解 | 得到无色溶液 | |
| ② | 将步骤1所得溶液____________抽滤 | 得到白色晶体 | |
| ③ | 干燥步骤2所得白色晶体,____________ | _____________ | 白色晶体是结晶玫瑰 |
(3)4.51g三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰4.68g,则产率是________(小数点后保留两位有效数字)。
-
乙酸甲酯是树脂、涂料、油墨、油漆、胶粘剂、皮革生产过程所需的有机溶剂,而且乙酸甲酯还可作为原料制备燃料乙醇。已知:乙酸甲酯可由乙酸和甲醇进行酯化反应得到。请回答下列问题:
(1)①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ∆H1=-874.5kJ/mol
②2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ∆H2=-1453kJ/mol
③2CH3COOCH3(l)+7O2(g)=6CO2(g)+6H2O(l) ∆H3=-3189.8kJ/mol
由上述反应,可求出CH3COOH(l)+CH3OH(l)=CH3COOCH3(l)+H2O(l)的∆H=________ 。
。
(2)对于反应CH3COOH(l)+CH3OH(l)⇌CH3COOCH3(l)+H2O(l),判断下列选项可以提高乙酸平衡转化率的是______
A.加入催化剂,增快反应速率
B.加入过量的甲醇
C.加入过量的乙酸
D.将乙酸甲酯从体系中分离
E.适当地提高反应温度
F.适当地降低反应温度
(3)在刚性容器压强为1.01MPa时,乙酸甲酯与氢气制备乙醇发生了两个反应:
主反应:CH3COOCH3(g)+2H2(g) ⇌ CH3OH(g)+CH3CH2OH(g) ∆H<0,
副反应:CH3COOCH3(g)+H2(g) ⇌ CH3OH(g)+CH3CHO(g) ∆H>0,实验测得,在相同时间内,反应温度与CH3CH2OH和CH3CHO的产率之间的关系如图所示:

①在540℃之前CH3CHO的产率远低于CH3CH2OH产率的原因是________。
②在470℃之后CH3CHO与CH3CH2OH产率变化趋势可能的原因是________。
(4)若在470℃时,以n(CH3COOCH3):n(H2)=1:10的投料比只进行主反应(不考虑副反应),乙酸甲酯转化率与气体总压强的关系如图所示:
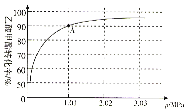
①A点时,CH3COOCH3(g)的平衡分压为________MPa,CH3CH2OH(g)的体积分数________%(保留一位小数)。
②470℃时,该反应的化学平衡常数Kp=________(MPa)-1(Kp为以分压表示的平衡常数,列出计算式,不要求计算结果)。
CH3COOC6H13(l)+CH3OH(l)
)随时间(
)的变化关系如图所示。下列说法正确的是