-
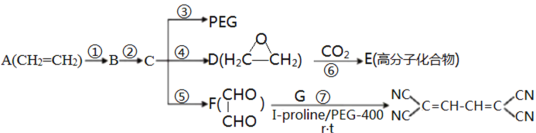
聚乙二醇(PEG)是一种非离子性惰性溶剂和绿色有机合成的重要催化剂,如图是合成PEG等的简单流程,其中E是一种聚碳酸酯高分子化合物。
已知①RCH2Cl RCH2CN
RCH2CN
②R’CHO+RCH2CN +H2O
+H2O
请根据以上信息回答下列问题:
(1)反应②所需的试剂和反应条件___;反应⑥的反应类型是___。
(2)物质F的名称为___。
(3)物质E的结构简式为___;反应⑦的另一种产物为水,则G的结构简式为___。
(4)反应③的化学方程式为___。
(5)M与D的组成元素相同,且M中各原子数目为D中各原子数目的2倍,写出符合下列条件的M的结构简式___ (只写一种)。
a.能与新制的氢氧化铜悬浊液反应生成砖红色沉淀
b.能在稀硫酸中发生水解反应
(6)写出以乙烯为原料合成 的路线图,其它无机试剂任选___。
的路线图,其它无机试剂任选___。
-
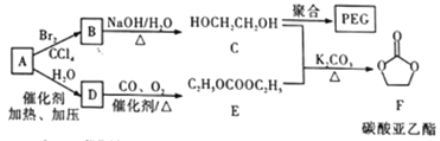
聚乙二醇(PEG) 是一种用途广泛的聚合物,1,2-乙二醇碳酸酯(又称为碳酸亚乙酯) 是一种医药中间体。某小组以烃A 为原料合成PEG和碳酸亚乙酯的路线设计如下:
已知: 2C2H5OH+CO+1/2O2  C2H5OCOOC2H5+H2O
C2H5OCOOC2H5+H2O
回答下列问题:
(1)A的名称为____________; A→B的反应类型为__________;C 的核磁共振氢谱中峰面积比为___________;F的分子式为____________________。
(2)B→C的化学方程式为____________。
(3)C在一定条件下发生聚合反应生成PEC,化学方程式为___________________;若某种PEG的平均相对分子质量为2000, 则其平均聚合度为____________________。
(4)E的同分异构体中,含有—OCOO—基团的共有___种(不包含E和立体异构)。
(5)有人认为C和E生成F的反应历程可能如下:
①HOCH2CH2OH + CO32- HOCH2CH2O-+HCO3-
HOCH2CH2O-+HCO3-
②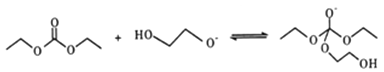
③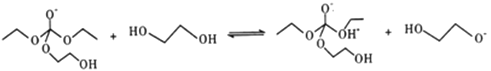
④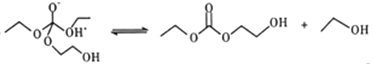
⑤
⑥⑦⑧……
⑨HOCH2CH2O- +HCO3-→HOCH2CH2OH+CO32-
写出上述历程中⑥⑦⑧的反应方程式___________________。
-
聚乙二醇(PEG) 是一种用途广泛的聚合物,1,2-乙二醇碳酸酯(又称为碳酸亚乙酯) 是一种医药中间体。某小组以烃A 为原料合成PEG和碳酸亚乙酯的路线设计如下:
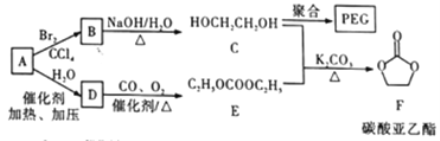
已知: 2C2H5OH+CO+1/2O2  C2H5OCOOC2H5+H2O
C2H5OCOOC2H5+H2O
回答下列问题:
(1)A的名称为____________; A→B的反应类型为__________;C 的核磁共振氢谱中峰面积比为___________;F的分子式为____________________。
(2)B→C的化学方程式为____________。
(3)C在一定条件下发生聚合反应生成PEC,化学方程式为___________________;若某种PEG的平均相对分子质量为2000, 则其平均聚合度为____________________。
(4)E的同分异构体中,含有—OCOO—基团的共有___种(不包含E和立体异构)。
(5)有人认为C和E生成F的反应历程可能如下:
①HOCH2CH2OH + CO32- HOCH2CH2O-+HCO3-
HOCH2CH2O-+HCO3-
②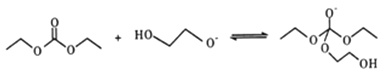
③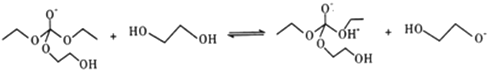
④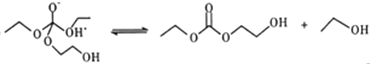
⑤
⑥⑦⑧……
⑨HOCH2CH2O- +HCO3-→HOCH2CH2OH+CO32-
写出上述历程中⑥⑦⑧的反应方程式___________________。
-
硫化碳又称氧硫化碳(化学式为COS),是农药、医药和其它有机合成的重要原料。COS的合成方法之一是在无溶剂的条件下用CO与硫蒸气反应制得,该法流程简单、收效高,但含有CO2、SO2等杂质。
(1)COS的电子式为_________。
(2)已知CO2催化加氢合成乙醇的反应原理是: 2CO2(g)+6H2(g) C2H5OH+3H2O(g) △H=-173.6 kJ/mol
C2H5OH+3H2O(g) △H=-173.6 kJ/mol
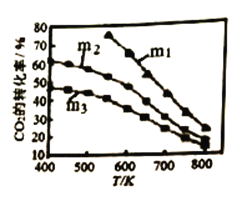
下图是不同起始投料时,CO2的平衡转化率随温度变化的关系,图中m= ,为起始时的投料比,则 m1、m2、m3从大到小的顺序为_______,理由是____________。
,为起始时的投料比,则 m1、m2、m3从大到小的顺序为_______,理由是____________。
(3)天然气部分氧化制取的化工原料气中,常含有COS。目前COS水解是脱除COS的常见方法,即COS在催化剂作用下与水蒸气反应生成硫化氢,生成的硫化氢可用氧化锌等脱硫剂脱除。
①COS 水解的化学方程式为_________________。
②常温下,实验测得脱硫(脱除硫化氢)反应过程中,每消耗4.05gZnO,放出3.83 kJ热量。该脱硫反应的热化学方程式为_________________。
③近年来,电化学间接氧化法处理硫化氢的技术得到较快发展。该方法是利用Fe3+在酸性条件下与H2S反应生成硫单质,反应后的溶液再用电解的方法“再生”,实现循环利用。电解法使Fe3+“再生”的离子方程式为___________,该反应的阳极材料是______。
④常温下,HCl和CuCl2的混合溶液中,c(H+) =0.30mol/L,c(Cu2+) =0.10mol/L,往该溶液中通入H2S 至饱和(H2S的近似浓度为0.10mol/L),_____(填“能”或“不能”)出现沉淀,用必要的计算过程和文字说明理由。
(已知Ka1(H2S)= 1.3×10-7,Ka2(H2S)= 7.0×10-5,Ksp(CuS) = 1.4×10-36)
-
二氧化碳和乙二醇在氧化锌或锌盐催化下可合成碳酸乙烯酯。
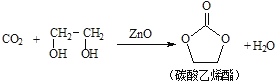
回答下列问题:
(1)锌基态离子的价电子排布图为_______________;在基态18O原子中,核外电子存在_________种空间运动状态。
(2)乙二醇中C、H、O的电负性大小关系是__________ ;碳酸乙烯酯中碳原子的杂化轨道类型有___________;1mol 碳酸乙烯酯中含有的σ键的数目为__________NA。
(3)锌盐水溶液中Zn2+可与H2O之间形成[Zn(H2O)6]2+,配体中的配位原子是_________(填微粒符号),[Zn(H2O)6]2+中所含化学键的类型为__________________________。
(4)阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为______________。
(5)一种锌金合金晶体的立方体晶胞中,金原子位于顶点,锌原子位于面心,则该合金中金原子与锌原子的个数之比为_________;若该晶体的晶胞棱长为apm(1pm=10-12m),则该合金的密度为_______g·cm-3(用NA表示阿伏加德罗常数的值,列出算式不要求结果)。
-
二氧化碳和乙二醇在氧化锌或锌盐催化下可合成碳酸乙烯酯。
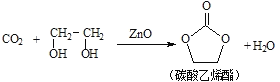
回答下列问题:
(1)锌基态离子的价电子排布图为_______________;在基态18O原子中,核外电子存在_________种空间运动状态。
(2)乙二醇中C、H、O的电负性大小关系是__________ ;碳酸乙烯酯中碳原子的杂化轨道类型有___________;1mol 碳酸乙烯酯中含有的σ键的数目为__________NA。
(3)锌盐水溶液中Zn2+可与H2O之间形成[Zn(H2O)6]2+,配体中的配位原子是_________(填微粒符号),[Zn(H2O)6]2+中所含化学键的类型为__________________________。
(4)阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为______________。
(5)一种锌金合金晶体的立方体晶胞中,金原子位于顶点,锌原子位于面心,则该合金中金原子与锌原子的个数之比为_________;若该晶体的晶胞棱长为apm(1pm=10-12m),则该合金的密度为_______g·cm-3(用NA表示阿伏加德罗常数的值,列出算式不要求结果)。
-
氯化亚铜不仅在无机化工生产中具有重要作用,在有机合成工业中还可作催化剂.以下是从含Cu2+、Fe3+的电镀废液中制备氯化亚铜的工艺流程图.
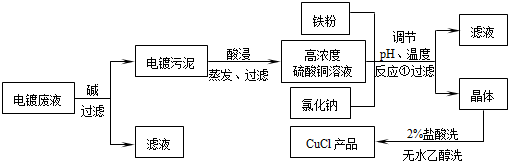
如图曲线可表示滤液中金属离子含量与pH、CuCl产率与反应①混合液中pH的关系.
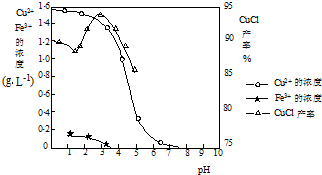
试填空.
(1)当pH=5时,在电镀废液中再加入氢氧化钠溶液生成电镀污泥的离子反应方程式为:________.
(2)由反应①制备CuCl时的最佳pH在________左右.
(3)已知在隔绝空气条件下进行反应①时CuCl产率较高,则CuCl具有________的特性.
(4)反应①中1mol铁粉完全反应转移2mol电子,该离子反应的方程式为:________.如果将反应①中铁粉换为亚硫酸钠,也可以得到氯化亚铜,则化学方程式为:________.
-
氯化亚铜不仅在无机化工生产中具有重要作用,在有机合成工业中还可作催化剂.以下是从含Cu2+、Fe3+的电镀废液中制备氯化亚铜的工艺流程图.
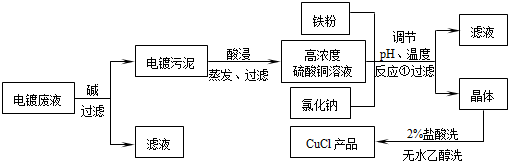
如图曲线可表示滤液中金属离子含量与pH、CuCl产率与反应①混合液中pH的关系.
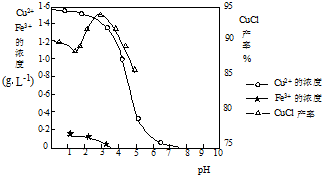
试填空.
(1)当pH=5时,在电镀废液中再加入氢氧化钠溶液生成电镀污泥的离子反应方程式为:________.
(2)由反应①制备CuCl时的最佳pH在________左右.
(3)已知在隔绝空气条件下进行反应①时CuCl产率较高,则CuCl具有________的特性.
(4)反应①中1mol铁粉完全反应转移2mol电子,该离子反应的方程式为:________.如果将反应①中铁粉换为亚硫酸钠,也可以得到氯化亚铜,则化学方程式为:________.
-
乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。下列说法不正确的是
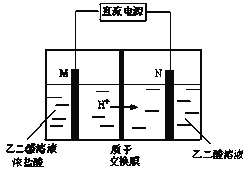
A.N电极上的电极反应式:HOOC-COOH+2e-+2H+=HOOC-CHO+H2O
B.若有2 mol H+ 通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol
C.M电极上的电极反应式为:2Cl--2e-=Cl2↑
D.乙二醛与M电极的产物反应生成乙醛酸的化学方程式: Cl2+OHC-CHO+ H2O = HOOC-CHO+2HCl
-
乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。下列说法正确的是
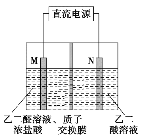
A. M极与直流电源的负极相连
B. 每得到lmol乙醛酸将有2molH+从右室迁移到左室
C. N电极上的电极反应式:HOOC-COOH-2eˉ+2H+ = HOOC-CHO+H2O
D. 每消耗0.1mol乙二醛在M电极放出2.24L气体(标准状况)

RCH2CN
 +H2O
+H2O的路线图,其它无机试剂任选___。


















