常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是
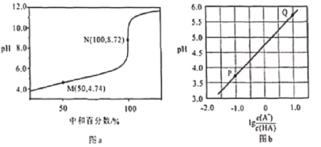
A. 当滴定至溶液呈中性时,c(A-)>c(HA) B. N点,c(Na+)·c(A-)=
C. Ka(HA)的数量级为10-5 D. P-Q过程中,水的电离程度逐渐增大
高三化学单选题中等难度题
常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是

A. 当滴定至溶液呈中性时,c(A-)>c(HA) B. N点,c(Na+)·c(A-)=
C. Ka(HA)的数量级为10-5 D. P-Q过程中,水的电离程度逐渐增大
高三化学单选题中等难度题
常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是
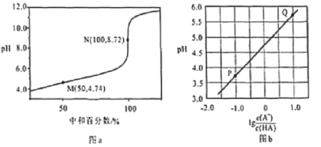
A. 当滴定至溶液呈中性时,c(A-)>c(HA) B. N点,c(Na+)·c(A-)=
C. Ka(HA)的数量级为10-5 D. P-Q过程中,水的电离程度逐渐增大
高三化学单选题中等难度题查看答案及解析
常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是

A. 当滴定至溶液呈中性时,c(A-)>c(HA) B. N点,c(Na+)·c(A-)=
C. Ka(HA)的数量级为10-5 D. P-Q过程中,水的电离程度逐渐增大
高三化学单选题中等难度题查看答案及解析
常温下,用0.1mol·L-1NaOH溶液滴定0.10 mol·L-1HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列陈述错误的是
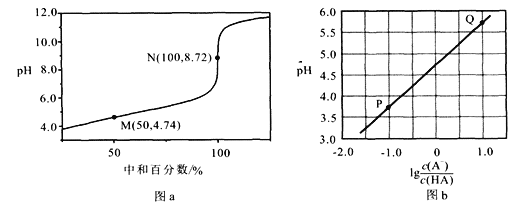
A.Ka(HA)的数量级为10-5
B.N点,c(Na+)-c(A-)=
C.P到Q过程中,水的电离程度逐渐增大
D.当滴定至溶液呈中性是,c(A-)>c(HA)
高三化学单选题中等难度题查看答案及解析
常温下,用0.10 moI/LNaOH溶液滴定0.10 mol/LHA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列叙述错误的是
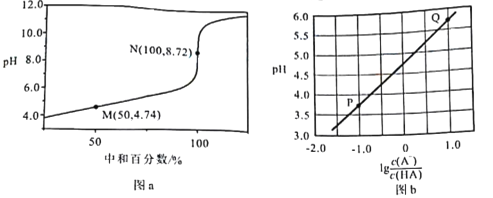
A. Ka(HA)的数量级为10-5
B. N点,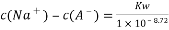
C. P—Q过程中,水的电离程度逐渐增大
D. 当滴定至溶液呈中性时,c(A-)>c(HA)
高三化学单选题中等难度题查看答案及解析
常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1HA溶液和HB溶液所得滴定曲线如图,下列说法不正确的是
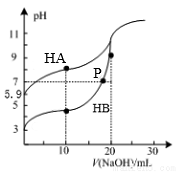
A. Ka(HA)=10-10.8
B. 滴定至P点时,溶液中:c(B-)+c(OH-)<c(HB)+c(H+)
C. 当滴定分别消耗l0mLNaOH 溶液时:c(B-)-c(A-)=c(HA)-c(HB)
D. 当滴定分别消耗20mLNaOH溶液时,将二种溶液混合:c(Na+)>c(B-)>c(A-)>c(H+)
高三化学选择题困难题查看答案及解析
常温时,体积均为50 mL物质的量浓度均为0.10 mol/L 的HX、HY、HZ 三种弱酸,分别用0.10 mol/L 的NaOH溶液滴定,滴定曲线如图所示。下列有关说法错误的是
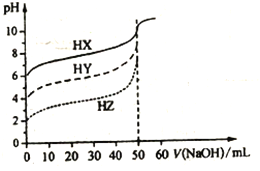
A. 浓度均为0.10 mol/L时,酸的电离度:HX<HY<HZ
B. pH均为3.0的三种酸加水稀释至pH均为6.5,加入水的量:HX>HY>HZ
C. 图中当均滴入50 mL NaOH 溶液时,所得溶液中水的电离程度:HX>HY>HZ
D. 用NaOH溶液中和pH 与体积均相等的三种酸时,消耗n(NaOH):HX<HY<HZ
高三化学单选题简单题查看答案及解析
常温下,用0.10 mol/L NaOH溶液分别滴定20.00 mL浓度均为0.10 mol/LCH3COOH溶液和 HCN 溶液所得滴定曲线如图[Ka(CH3COOH)>Ka(HCN)]。下列说法正确的是
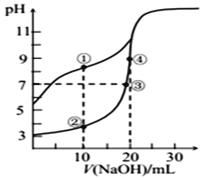
A.点①和点②所示溶液中:c(CH3COO﹣)<c(CN﹣)
B.点①和点②所示溶液中:c(CH3COO﹣)-c(CN﹣) = c(HCN)-c(CH3COOH)
C.溶液中水的电离程度:③>④
D.点③和点④所示溶液中都有:c(CH3COO﹣)+c(OH﹣) = c(CH3COOH)+c(H+)
高三化学单选题困难题查看答案及解析
已知电导率越大导电能力越强。常温下用0.10 mol·L-1NaOH溶液分别滴定10mL浓度均为0.10 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
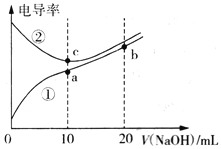
A.曲线①代表滴定盐酸的曲线
B.滴定醋酸的过程应该选择甲基橙作为指示剂
C.a、b、c三点溶液中水的电离程度:c>a>b
D.b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
高三化学单选题困难题查看答案及解析
常温下,用0.10mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COONa溶液和NaCN溶液,所得滴定曲线如图(忽略体积变化)。下列说法正确的是( )
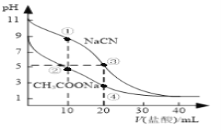
A.溶液中阳离子的物质的量浓度之和:点②等于点③
B.点①所示溶液中:c(CN-)+c(HCN)﹤2c(Cl-)
C.点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)>c(CH3COOH)
D.点④所示溶液中:c(Na+)+c(CH3COOH)+c(H+)>0.10mol·L-1
高三化学单选题中等难度题查看答案及解析
常温下,用酚酞作指示剂,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1的 CH3COOH溶液和HCN溶液所得滴定曲线如图。
(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)
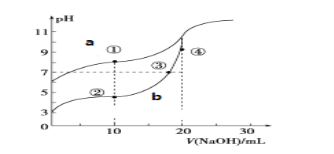
(1)图__(a或b)是NaOH溶液滴定HCN溶液的pH变化的曲线,判断的理由是__。
(2)点③所示溶液中所含离子浓度的从大到小的顺序:__。
(3)点①和点② 所示溶液中:c(CH3COO-)-c(CN-)__c(HCN)-c(CH3COOH)(填“>、<或=”)
(4)点②③④所示的溶液中水的电离程度由大到小的顺序是:__。
高三化学解答题中等难度题查看答案及解析