-
如图是一个电化学过程的示意图,请按要求回答下列问题
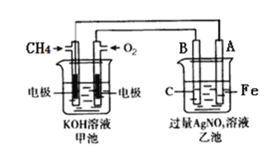
(1)甲池是 _______装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入 CH4的电极________; A(Fe)电极_______ 。
(3) 反应一段时间后,甲池中消耗 1.6g甲烷,则乙池中某电极的质量增加 _____ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的______(填“正”或“负”)极,C口流出的物质是______。
②SO32-放电的电极反应式为______。
-
下图是一个电化学过程的示意图,回答下列问题:

(1)甲池是___________(填“原电池”、“电解池”或“电镀池”)装置,乙装置中电极A的名称是_______(填“正极”、“负极”、“阴极”或“阳极”)。
(2)甲装置中通入CH4的电极反应式为__________________________________,乙装置中电极B(Ag)的电极反应式为________________________________,丙装置中D极的产物是____________(写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=________(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入________(写化学式)。
-
(10分)下图是一个电化学过程的示意图。
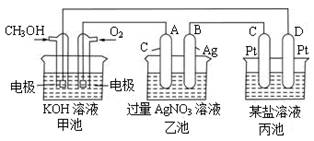
请回答下列问题:
(1)图中甲池的名称________(填“原电池”“电解池”或“电镀池”)。
(2)写出通入CH3OH的电极的电极反应式: 。
(3)乙池中反应的化学方程式为 ,当乙池中B极的质量增加5.4g时,甲池中理论上消耗O2的体积为________L(标准状况下),此时丙池中________电极(填“C”或“D”)析出1.6g某金属,则丙池的某盐溶液可能是 (填序号)
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液
【解析】(1)甲属于燃料电池,给乙池和丙池供电。在燃料电池中可燃物在负极通入,所以电极反应式为CH3OH+8OH――6e-=CO32-+6H2O。电极A和电池的正极相连,所以A是阳极、B是阴极、C是阳极、D是阴极。A是惰性电极,所以乙池中反应式为4AgNO3+2H2O  4Ag+O2↑+4HNO3。5.4g是单质银,转移的电子是
4Ag+O2↑+4HNO3。5.4g是单质银,转移的电子是 ,所以根据得失电子守恒可知氧气的物质的量是
,所以根据得失电子守恒可知氧气的物质的量是 。金属阳离子只有在阴极放电,所以在D电极放电。镁和钠属于活泼的金属,在水溶液中其离子不可能放电。1.6g若是铜,则转移的电子为
。金属阳离子只有在阴极放电,所以在D电极放电。镁和钠属于活泼的金属,在水溶液中其离子不可能放电。1.6g若是铜,则转移的电子为 ,正确。若是银,则说明硝酸银不足,还有氢气生成,所以答案是BD。
,正确。若是银,则说明硝酸银不足,还有氢气生成,所以答案是BD。
-
(14分)下图是一个电化学过程的示意图。
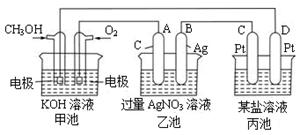
请回答下列问题:
(1)图中甲池的名称________(填“原电池”“电解池”或“电镀池”)。
(2)写出通入CH3OH的电极的电极反应式:________。
(3)乙池中反应的化学方程式为 ________
(4)当乙池中B极的质量增加5.4g时,甲池中理论上消耗O2的体积为________L(标况下),此时丙池中________电极(填“C”或“D”)析出1.6g某金属,则丙池的某盐溶液可能是________(填序号)
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液
-
如图所示是一个电化学装置的示意图。
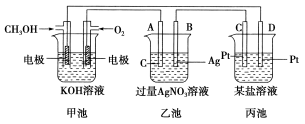
请回答下列问题:
(1)图中甲池是________(填“原电池”、“电解池”或“电镀池”)。
(2)A(石墨)电极的名称是________(填“正极”、“负极”、“阴极”或“阳极”)。
(3)写出通入CH3OH的电极的电极反应式:_________________________________。
(4)乙池中反应的化学方程式为______________________________________。
(5)当乙池中B(Ag)极质量增加5.4 g时,甲池中理论上消耗O2的体积为________L(标准状况),此时丙池中某电极析出1.6 g某金属,则丙池中的某盐溶液可能是________(填字母)。
A. MgSO4 B.CuSO4 C. NaCl D. AgNO3
-
如图是一个化学过程的示意图。
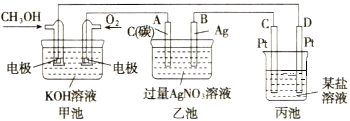
(1)图中甲池是______装置(填“电解池”或“原电池”),其中OH-移向______极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:_______。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________极(填“A”或“B”),并写出此电极的反应式_______。
(4)乙池中总反应的离子方程式_________。
(5)常温下,当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是_______(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是________(填序号)。
A.MgSO4 B.CuSO4 C.NaCl D.KOH
-
下图是一个化学过程的示意图。
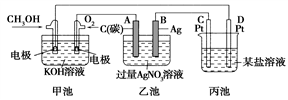
(1)图中甲池是________装置(填“电解池”或“原电池”),其中OH-移向________极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式: _______________________。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________极(填“A”或“B”),并写出此电极的反应式:______________。
(4)乙池中总反应的离子方程式:____________。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________(若此时乙池中溶液的体积为500 mL);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是________(填序号)。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
-
下图是一个化学过程的示意图。
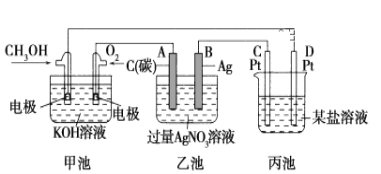
(1)图中甲池是________装置(填“电解池”或“原电池”)
(2)写出通入CH3OH的电极的电极反应式: _______________________。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________极(填“A”或“B”),并写出此电极的电极反应式:______________。
(4)若丙中电极不变,将其溶液换成NaCl溶液,丙池中总反应的离子方程式:__________。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________(若此时乙池中溶液的体积为500 mL);
-
下图是一个化学过程的示意图。
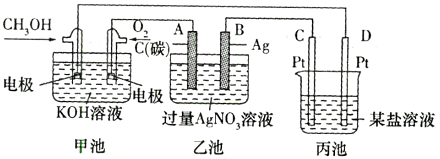
(1)图中丙池是____________装置(填“电解池”或“原电池”),甲池中K+移向____________极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:____________。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为____________极(填“A”或“B")。
(4)乙池中总反应的离子方程式____________。
(5)当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是____________(若此时乙池中溶液的体积为500 mL);通过导线的电量是____________(结果保留3位有效数字,已知:NA =6.02×1023,电子的电量为1.60 ×10-19);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是____________
A.MgSO4 B.CuSO4
C.NaC1 D.AgNO3
-
下图是一个电化学过程的示意图,请回答下列问题:
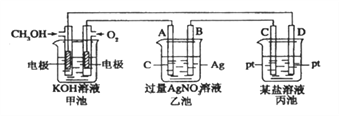
(1)图中甲池是_________ (填“原电池” “电解池”或“电镀池”)。
(2)A(石墨)电极的名称是_________ (填“正极” “负极” “阴极”或“阳极”)。
(3)写出通入CH3OH的电极的电极反应式________________。
(4)乙池中反应的化学方程式为__________________。当乙池中B(Ag)极质量增加54g,甲池中理论上消耗O2的体积为____L(标准状况)。










