-
室温下,0.1 mol·L-1的氨水中,下列关系式中不正确的是( )
A.c(OH-)>c(H+)
B.c(NH3·H2O)+c(NH4+)=0.1 mol·L-1
C.c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+)
D.c(OH-)=c(NH4+)+c(H+)
高二化学单选题中等难度题查看答案及解析
-
室温下,0.1mol/L氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
①电离度增大 ②C(OH-)增大 ③C(H+)增大 ④KW增大 ⑤导电性增强 ⑥C(OH-)/C(NH3·H2O)增大
A.①②③ B.①③⑤ C.①③⑥ D.②④⑥
高二化学单选题中等难度题查看答案及解析
-
室温下,下列事实不能说明NH3•H2O为弱电解质的是
A. 0.1 mol•L-1 NH3•H2O溶液的pH小于13
B. Al(OH)3在浓氨水中不能溶解
C. 相同条件下,浓度均为0.1 mol•L-1的NaOH溶液和氨水,氨水的导电能力弱
D. 向0.1 mol•L-1 NH3•H2O溶液中加入MgCl2溶液产生白色沉淀
高二化学单选题简单题查看答案及解析
-
室温下,下列有关溶液中微粒的物质的量浓度的关系正确的是
A. 0.1mol/L NH4 Cl溶液与0.1 mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c(NH4+)>c(C1-)>c(OH-)>c(H+)
B. 0.1 mol/LCH3 COONa溶液与0.1 mol/L盐酸等体积混合:c(OH-)<c(CH3COO-)< c(H+)< c(C1-)=o.1 mol/L
C. 0.1mol/LNa2CO3溶液与0.1 mol/L盐酸等体积混合:2c(CO32-)+C(HCO3-)+ c(OH-)=c(Na+)+c(H+)
D. 0.1 mol/LNaHS溶液与0.2 mol/LNaOH溶液等体积混合:c(OH-)-c(H+) =C(S2-)+ 2c(HS-)+ 3c(H2S)
高二化学单选题困难题查看答案及解析
-
室温时,将氨水与氯化铵溶液混合得到c(NH3·H2O)+c(NH4+)=0.1mol·L-1的混合溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如图所示。下列说法正确的是
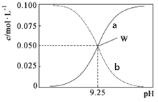
A.W点溶液中:c(H+)=c(OH-)
B.pH=8时溶液中:c(C1-)+c(OH-)=c(H+)+c(NH4+)
C.室温时NH3·H2O的电离平衡常数的值为10-9.25
D.pH=10溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+)
高二化学多选题中等难度题查看答案及解析
-
下列溶液中微粒的物质的量浓度关系正确的是( )
A. 浓度均为0.1 mol·L-1的氨水和盐酸等体积混合后:c(H+)=c(OH-)+c(NH3·H2O)
B. 等浓度的碳酸钠、碳酸氢钠溶液混合后:c(CO
)<c(HCO
)
C. 在NaHB溶液中一定有:c(Na+)=c(HB-)+2c(B2-)
D. Na2CO3溶液中:2c(Na+)=c(CO
)+c(HCO
)+c(H2CO3)
高二化学单选题中等难度题查看答案及解析
-
常温下,下列溶液中各离子浓度关系正确的是 ( )
A. 等体积等物质的量浓度的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
B. 浓度为0.1 mol·L-1的碳酸钠溶液:c(Na+)=2c(CO32-+c(HCO3-)+c(H2CO3)
C. pH=12的氨水与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D. 醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-)
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A.0.1mol·L−1 NH3·H2O中:c(OH-)>c(NH4+)>c(NH3·H2O)>c(H+)
B.0.1mol·L−1 NaHSO3溶液(室温下pH<7)中:c(SO32-)<c(H2SO3)
C.浓度均为0.1mol·L−1 的Na2CO3和NaHCO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
D.0.1mol·L−1 (NH4)2CO3溶液中:c(NH4+)+c(NH3·H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
高二化学多选题简单题查看答案及解析
-
下列坐标图均涉及平衡原理,其中相关表述正确的是

A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g)
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g)
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s)
Ag+(
aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
高二化学选择题困难题查看答案及解析
-
下列坐标图均涉及平衡原理,其中相关表述正确的是

A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g)
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g)
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s)
Ag+(
aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
高二化学选择题困难题查看答案及解析