-
某化学兴趣小组取部分变质的Ca(OH)2(含杂质CaCO3)样品4.0g投入200.0g水中,充分搅拌,通入足量CO2,溶液质量与反应的CO2质量的关系如图所示.则:
(1)以Ca(OH)2全部转化为CaCO3时消耗的CO2质量为_____g;
(2)4.0g样品中杂质CaCO3的质量为______________?(写出计算过程)

(3)通入m3gCO2时,溶液中生成物的溶质的质量分数为_____(精确到0.1%).若所取样品中的Ca(OH)2没有完全溶于水,对最后的计算结果_____(填“有”、“没有”)影响.原因是_____.
-
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
回答下列问题:
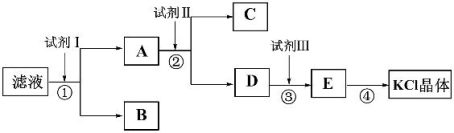
(1)①中发生反应的化学方程式为__________。
(2)②中加入试剂Ⅱ的目的是__________。
(3)操作④为蒸发,蒸发的作用之一是得到KCl晶体,另一作用是__________。
(4)某同学称取提纯的产品0.76g,溶解后定容在100mL容量瓶中,取25.00mL溶液,与25.00mL浓度为0.1000mol/L的硝酸银溶液恰好完全反应,则该产品的纯度为__________。
-
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作。回答下列问题:

(1)试剂Ⅰ的化学式为_______。
(2)试剂Ⅱ的化学式为_______,②中加入试剂Ⅱ的目的是除去A中的____,检验该离子已经除尽的方法是________________________________________________________。
(3)③中发生反应的化学方程式为_________________________________________________。
(4)由E得到KCl晶体的实验操作是_______________。
-
KCl样品中含有少量KOH、K2SO4和不溶于水的杂质,为了提纯KCl,某同学先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作
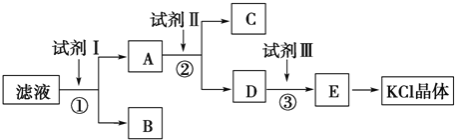
(1)试剂Ⅰ的化学式为__________,其作用是除去__________(填离子符号),
检验该离子完全除尽的操作是__________________________________________
(2)加入试剂Ⅱ时发生反应的化学方程式为_____________________________
(3)试剂Ⅲ的名称是__________,各步操作中所加试剂都必须过量,欲检验试剂Ⅲ已经过量,可以选用__________(填字母).
A.AgNO3 B.pH试纸 C.K2CO3溶液
-
工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取ag工业纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体。则该样品中纯碱的质量分数是( )
A. ×100% B.
×100% B. ×100%
×100%
C. ×100% D.
×100% D. ×100%
×100%
-
为测定某大理石样品中CaCO3的纯度,称取10.0g大理石样品投入到50mL未知浓度的盐酸中,两者恰好完全反应(杂质不反应),生成1.12L(标准状况)CO2气体。
计算:(1)该大理石样品中CaCO3的质量分数___。
(2)盐酸的物质的量浓度___。
-
工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取a g纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体.则该样品中纯碱的质量分数为( )
A. ×100% B.
×100% B. ×100%
×100%
C. ×100% D.
×100% D. ×100%
×100%
-
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为____________。
(2)实验中,需加热至恒重的目的是_____________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是__________。
[方案三]按如下图所示装置进行实验:
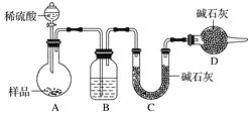
(1)D装置的作用是________,分液漏斗中_____(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中碳酸钠的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是_________。
-
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。则坩埚中发生反应的化学方程式为____________________________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是_________________________。
[方案三]按如下图所示装置进行实验:
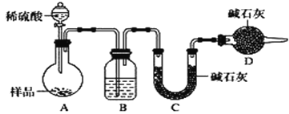
(1)D装置的作用是______________________,分液漏斗中__________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_____。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是____________。
-
某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3 的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2 溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2+ +OH-+HCO3-==BaCO3 ↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
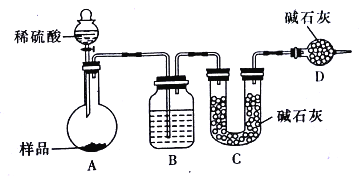
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90 g样品,实验后测得C装置增重8.80 g,则样品中Na2CO3 的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。






