-
请根据信息填空:
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3 +Cu ===2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用的电极材料为____;当线路中转移0.2mol电子时,则被腐蚀的铜的质量为____。
(2)如图所示,把试管放入盛有25℃的饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中,可观察到溶液变浑浊,试回答下列问题:
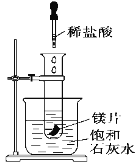
①产生上述现象的原因是___________________________;
②写出有关反应的离子方程式___________________。
③由实验推知,MgCl2和H2的总能量__________(填“大于”、“小于”或“等于”)Mg和HCl的总能量。
-
I.请根据信息填空:
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3 +Cu ===2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用的电极材料为__________________;当线路中转移0.2mol电子时,则被腐蚀的铜的质量为__________________。
(2)如图所示,把试管放入盛有25℃的饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中,可观察到溶液变浑浊,试回答下列问题:
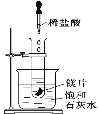
①产生上述现象的原因是___________________________;
②写出有关反应的离子方程式___________________。
③由实验推知,MgCl2溶液和H2的总能量__________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
Ⅱ.在1×105 Pa和298 K时,将1 mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
| 共价键 | H2分子 | N2分子 | NH3分子 |
| 键能(kJ·mol-1) | 436 | 945 | 391 |
(1)根据上表中的数据判断工业合成氨的反应是______(填“吸热”或“放热”)反应;
(2)在298 K时,取1 mol N2和3 mol H2放入一密闭容器中,在催化剂存在下进行反应,理论上生成2molNH3时放出或吸收的热量为Q,则Q为________。
-
制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
2FeCl3 + Cu = 2FeCl2 + CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应
结束后,溶液中存在的金属阳离子不可能出现的是( )
A.只有Fe2+ B.只有Fe2+、Cu2+
C.有Fe3+、Fe2+、Cu2+ D.只有Fe3+、Cu2+
-
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路(已知发生的反应为 2FeCl3 + Cu =2FeCl2 + CuCl2)。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取100 mL废液加入足量的AgNO3溶液,生成沉淀 86.1g。(2)另取100 mL废液放入铜片充分反应,铜片质量减少了2.56 g。下列关于原废液组成的判断错误的是
A.c(Fe2+)︰c(Fe 3+)︰c(Cu2+) = 2︰1 ︰1
B.c(Fe2+)︰c(Cu2+) = 2︰1
C.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ
D.c(Clˉ) = 6mol / L,c(Fe 2+) = 1.2mol / L
-
制印刷电路时常用氯化铁溶液作为“腐蚀液”。铜被氯化铁溶液腐蚀的方程式为2FeCl3 + Cu = 2FeCl2 + CuCl2 ;FeCl3 溶液也能与铁反应2FeCl3+Fe=3FeCl2;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是
A.有铜无铁 B.有铁无铜 C.有铁有铜 D.无铁无铜
-
制印刷电路时常用氯化铁溶液作为“腐蚀液”。铜被氯化铁溶液腐蚀的方程式为2FeCl3 + Cu = 2FeCl2 + CuCl2;FeCl3溶液也能与铁反应2FeCl3+Fe=3FeCl2;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是( )
A.无铁无铜 B. 有铜无铁 C.有铁有铜 D.有铁无铜
-
(8分)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式:
 Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
(1)请在上式中标出电子转移的方向和数目 。
(2)上述反应中的氧化剂是: 。
(3)写出FeCl3的电离方程式: 。
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是 (填序号)
A.氯气 B.铁 C.双氧水 D.稀硫酸
-
制印刷电路板时常用氯化铁溶液作为“腐蚀液”,其反应的化学方程式为Cu + 2FeCl3 = 2FeCl2+ CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A. 烧杯中有铜无铁 B.烧杯中铁、铜都无
烧杯中有铜无铁 B.烧杯中铁、铜都无
C.烧杯中铜、铁都有 D.烧杯中有铁无铜
-
工业上常用FeCl3溶液与铜反应制作印刷电路板。该反应的化学方程式为:
2FeCl3 + Cu = 2FeCl2 + CuCl2 。取上述反应后溶液10 mL进行分析,测得其中c(Fe3+)为1mol·L—1。向其中加入足量的硝酸银溶液,过滤、干燥,可得到沉淀l7.22g。则上述反应后的10mL溶液中c(Cu2+)为
A.0.5mol·L—1 B.1.5 mol·L—1 C.0.4 mol·L—1 D.0.25 mol·L—1
-
制印刷电路时常用FeCl3溶液作为“腐蚀液”,发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2。
向盛有FeCl3溶液的烧杯中同时加入铁粉和铜粉,反应结束后,杯底固体中不可能出现
A.有铜无铁 B.有铁无铜 c.铁、铜都有 D.铁、铜都无

