-
2018年11月《Nature Energy》报道了巾科院大连化学物理研究所科学家用Ni- BaH2 /Al2O3、Ni- LiH等作催化剂,实现了在常压、100-300℃的条件下合成氨。
(1)在元素周期表中,氧和与其相邻且同周期的两种元素的第一电离能由大到小的顺序为 __ ;基态Ni2+的核外电子排布式为 ___,若该离子核外电子空间运动状态有15种,则该离子处于 ___(填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中NO3⁻的空间构型为____。
②甘氨酸中N原子的杂化类型为____,分子中σ键与π键的个数比为____,晶体类型是 ___,其熔点、沸点远高于相对分子质量几乎相等的丙酸(熔点为-2l℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是____。
(3)NH3分子中的键角为107°,但在[Cu(NH3)4]2+离子中NH3分子的键角如图l所示,导致这种变化的原因是____
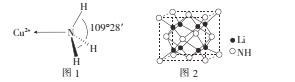
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为d pm,密度为ρg/cm3,则阿伏加德罗常数NA=____(列出表达式)mol-l。
-
2018 年 11 月《Nature Energy》报道了中科院大连化学物理研究所科学家用 Ni-BaH2/Al2O3、Ni-LiH 等作催化剂,实现了在常压、100~300℃的条件下合成氨。
(1)在元素周期表中,Li、O、H 三种元素的电负性由大到小的顺序为___________;Al 原子核外电子空间运动状态有 8 种,则该原子处于____(填“基态”或“激发态”)。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为 182℃,沸点为 233℃。
①硝酸溶液中 NO3‑的空间构型为__________ 。
②甘氨酸中 N 原子的杂化类型为 ________,分子中σ键与π键的个数比为_________;其熔点、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为 141℃)的主要原因:一是甘氨酸能形成内盐,二是______________。
(3)[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式___________________。
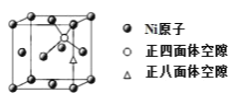
(4)X-射线衍射分析表明,由 Ni 元素形成的化合物 Mg2NiH4 的立方晶胞如图所示,其面心和顶点均被 Ni 原子占据,所有 Mg 原子的 Ni 配位数都相等。则 Mg 原子填入由 Ni 原子形成的 ___空隙中(填“正四面体”或“正八面体”),填隙率是____。
(5)已知 Mg2NiH4 晶体的晶胞参数为 646.5 pm,液氢的密度为0.0708 g•cm-3。若以材料中氢的密度与液氢密度之比定义为储氢材料的储氢能力,在 Mg2NiH4 的储氢能力为____________(列出计算式即可)。
-
2018年11月《 Nature Energy》报道了我国科学家用 Ni-BaH2/A12O3、 Ni-LiH等作催化剂,利用化学链合成氨。回答下列问题:
(1)基态Al原子价层电子的电子排布图(轨道表达式)为___________,Ni在周期表中位于第___________族,属于___________区元素。
(2)BaH2的熔点(675℃)比CaH2(816℃)的低,其原因是___________。
(3)NH3可用于制备NaN3、NH4NO3、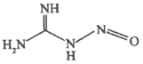 (亚硝基胍)等含氮化合物:NaN3中阴离子空间构型为___________;NH4NO3中阳、阴离子中中心原子杂化方式依次为___________,亚硝基胍分子中含σ键___________个。
(亚硝基胍)等含氮化合物:NaN3中阴离子空间构型为___________;NH4NO3中阳、阴离子中中心原子杂化方式依次为___________,亚硝基胍分子中含σ键___________个。
(4)N、P位于同一主族,NH3、PH3分子结构如下图所示:

①NH3中N-H键的键长比PH3中P-H键的键长短,其主要原因是___________。
②NH3和PH3中,N、P原子杂化方式相同,但H-N-H间的夹角比H-P-H间的大,其主要原因是___________。
③NH3比PH3易液化,其主要原因是___________。
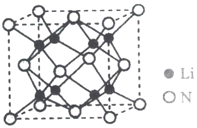
(5)该化学链合成氨过程中涉及中间化合物亚氨基锂(Li2NH),亚氨基锂是一种反荧石结构,晶体结构如上图所示(H已略去)。NA为阿伏加德罗常数的值,晶体密度为1.48g·cm-3,Li2NH的摩尔质量为28.897g·mol-1.则晶胞参数为___________nm(列出计算式)。
-
2017 年5月4 日《光明日报》报道称,中科院大连化学物理研究所的研究团队利用多功能催化剂首次实现了CO2直接加氢制汽油的过程。其转化过程如图所示:
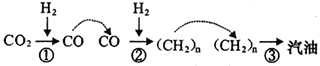
下列说法正确的是
A. 反应①的产物中含有水。
B. 反应②为化合反应
C. 所制得汽油的主要成分是烃和烃的含氧衍生物
D. 这种人造汽油用作汽车的燃料时,汽车尾气中不含氮氧化物
-
2017 年5月4 日《光明日报》报道称,中科院大连化学物理研究所的研究团队利用多功能催化剂首次实现了CO2直接加氢制汽油的过程。其转化过程如图所示:
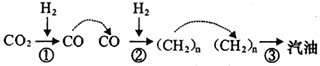
下列说法正确的是
A. 反应①的产物中含有水。
B. 反应②为化合反应
C. 所制得汽油的主要成分是烃和烃的含氧衍生物
D. 这种人造汽油用作汽车的燃料时,汽车尾气中不含氮氧化物
-
2019年2月27日,科技日报报道中科院大连化学物理研究所创新性地提出锌碘单液流电池的概念,锌碘单液流电池中电解液的利用率达到近100% ,进而大幅度提高了电池的能量密度,工作原理如图所示。下列说法正确的是
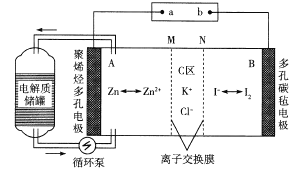
A.该电池放电时电路中电流方向为A→a→b→B→A
B.M为阴离子交换膜,N为阳离子交换膜
C.如果使用铅蓄电池进行充电,则B电极应与铅蓄电池中的Pb电极相连
D.若充电时C区增加的离子数为2NA,则A极增重65 g
-
2019年2月27日,科技日报报道中科院大连化学物理研究所创新性地提出锌碘单液流电池的概念,锌碘单液流电池中电解液的利用率达到近100%,进而大幅度提高了电池的能量密度,工作原理如图所示。下列说法不正确的是( )
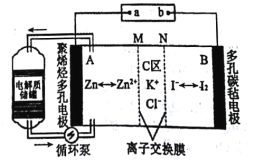
A.该电池放电时电路中电流方向为B→b→a→A
B.M为阴离子交换膜,N为阳离子交换膜
C.如果使用铅蓄电池进行充电,则a电极应连接铅蓄电池中的Pb电极
D.若充电时C区增加的离子数为2NA,则A极增重65g
-
CO2的资源化利用一直是化学家们关注的重要课题,中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油: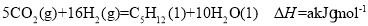 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1)已知氢气的燃烧热为 ,若要利用
,若要利用 的燃烧热求a的值,则还需要知道一个反应的
的燃烧热求a的值,则还需要知道一个反应的 ,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
(2)向某密闭容器中按一定投料比充入 、
、 ,控制条件使其发生反应:
,控制条件使其发生反应: 。测得
。测得 的平衡转化率与温度、压强之间的关系如图1所示:
的平衡转化率与温度、压强之间的关系如图1所示:
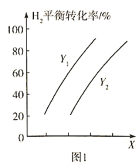
则X表示______________, ___________
___________ (填“>”或“<”)。欲提高
(填“>”或“<”)。欲提高 的平衡转化率并提高单位时间内
的平衡转化率并提高单位时间内 的产量,可采取的措施是______________________(填两种)。
的产量,可采取的措施是______________________(填两种)。
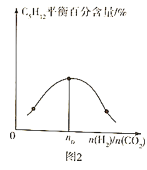
(3)控制一定温度、催化剂,按不同投料比 将反应物通入到某密闭容器中,测得平衡时
将反应物通入到某密闭容器中,测得平衡时 的百分含量与投料比之间的关系如图2所示,则
的百分含量与投料比之间的关系如图2所示,则 ____________。
____________。
(4)在钌-铑双金属催化剂的作用下,CH3OH、CO2、H2可高效地转化为乙酸,反应方程式为 。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/kPa | 3 | 2.7 | 2.5 | 2.35 | 2.26 | 2.2 | 2.2 |
则反应开始到达到平衡的过程中, ______________
______________ ______________
______________ 。
。
(5)碳捕捉技术的发展也有利于CO2在资源应用方面得到充分利用。常温下,若某次用NaOH溶液捕捉空气中的CO2所得溶液的pH=10,并测得溶液中 ,则
,则 _____________
_____________ 。
。
-
中科院大连化学物理研究所的“煤基甲醇制取低碳烯烃技术(简称DMTO)”荣获2014年度国家技术发明一等奖。DMTO技术主要包括煤的气化、液化、烯烃化三个阶段,相关反应的热化学方程式如下:
(i)煤气化制合成气:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
(ii)煤液化制甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(iii)甲醇制取低碳烯烃:2CH3OH(g) C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
3CH3OH(g) C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
回答下列问题:
(1)已知:C(s)+CO2(g)=2CO(g) ΔH= +172.5kJ·mol-1,
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH= -41.0kJ·mol-1
反应(i)能自发进行的条件是 (填“高温”、“低温”或“任何温度”)。
(2)反应(ii)中以氢碳[n(H2)∶n(CO)]投料比为2制取甲醇,温度、压强与CO的平衡转化率关系如下图1。
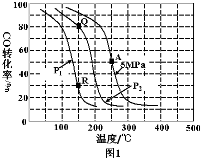
①对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则A点时反应(ii)的Kp= (保留两位有效数字,分压=总压×物质的量分数)。
②比较P1 P2,Kp(Q) Kp(R)(填“大于”、“小于”或“等于”)。
③工业上常以铜基催化剂,压强5MPa,温度275℃下发生反应(ii),CO转化率可达到40%左右。为提高CO转化率除了可以适当改变反应温度和压强外,还可以采取的措施有 (写出2个)。
④若反应(ii)在恒容密闭容器内进行,T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t2时刻迅速降温到T2,t3时刻体系重新达到平衡。试在图中画出t2时刻后甲醇浓度随时间变化趋势图(在图中标出t3)。
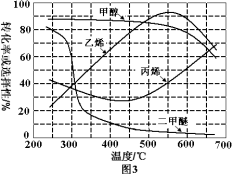
(3)烯烃化阶段:在常压和某催化剂作用下,甲醇的平衡转化率及乙烯、丙烯等物质的选择性(指除了水蒸气以外的产物中乙烯、丙烯等物质的物质的量分数)与反应温度之间的关系如图3。为尽可能多地获得乙烯,控制反应温度为550℃的理由是 。
-
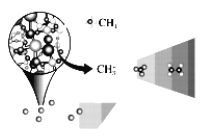
中科院大连化学物理研究所的一项最新成果实现了甲烷高效生产乙烯,如图所示,甲烷在催化作用下脱氢,在不同温度下分别形成 等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
| 物质 | 燃烧热/(kJ•mol-1) |
| 氢气 | 285.8 |
| 甲烷 | 890.3 |
| 乙烯 | 1411.0 |
(1)已知相关物质的燃烧热如上表所示,写出甲烷制备乙烯的热化学方程式______________。
(2)现代石油化工采用Ag作催化剂,可实现乙烯与氧气制备X(分子式为C2H4O,不含双键)该反应符合最理想的原子经济,则反应产物是____________(填结构简式)
(3)在400℃时,向初始体积为1L的恒压密闭反应,器中充入1 mol CH4,发生(1)中反应,测得平衡混合气体中C2H4的体积分数为25.0%。则:
①在该温度下,其平衡常数KC=____________。
②若向该反应器中通入高温水蒸气(不参加反应,高于400℃),则C2H4的产率____________。(填“增大”“减小”“不变”或“无法确定”),理由是_______________________________。
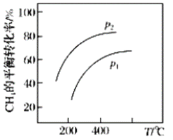
③若反应器的体积固定,不同压强下可得变化如右图所示,则压强P1,P2的大小关系是____________。
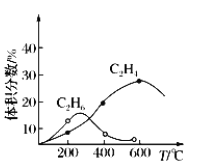
(4)实际制备C2H4时,通常存在副反应2CH4(g) C2H4(g)+2H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如右图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是____________。
C2H4(g)+2H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如右图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是____________。
(5)C2H4、C2H6常常作为燃料电池的原料,请写出C2H4在NaOH溶液中做燃料电池的负极的电极反应方程式________________________________________________。


 (亚硝基胍)等含氮化合物:NaN3中阴离子空间构型为___________;NH4NO3中阳、阴离子中中心原子杂化方式依次为___________,亚硝基胍分子中含σ键___________个。
(亚硝基胍)等含氮化合物:NaN3中阴离子空间构型为___________;NH4NO3中阳、阴离子中中心原子杂化方式依次为___________,亚硝基胍分子中含σ键___________个。





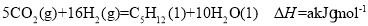 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。






