-
硫脲[SC(NH2)2]别名硫代尿素,是一种白色固体,熔点182℃。硫脲可代替氰化物用于提炼金的新工艺。酸性条件下,硫脲在氧化剂(如Fe3+、H2O2、O2)存在下能溶解金,形成配离子Au[SC(NH2)2] 。
。
回答下列问题:
(1)C、N、S三种元素中第一电离能最大的是___(填元素符号)。
(2)Au与Cu同族,价电子排布式为5d106s1,Au位于元素周期表的___区,Au+的价电子排布式为___。
(3)硫脲分子中碳原子的杂化方式为___,σ键和π键数目之比为___。
(4)写出硫脲在硫酸铁存在下溶解金的离子方程式___。
(5)硫脲加热到150℃时可转变成硫氰酸铵(NH4SCN),SCN-的空间构型为___形。
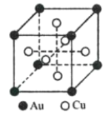
(6)一种铜金合金晶体具有面心立方最密堆积的结构,其晶胞如图所示,则该合金中Au原子与Cu原子个数之比为___。若铜和金的半径分别为apm和bpm,相对原子质量分别为MA和MB,阿伏加德罗常数的值为NA,计算晶体的密度为___g/cm3。
-
CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质。
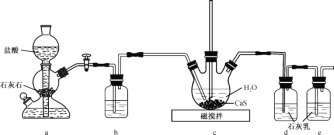
(1)制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
①装置a中反应发生的操作为 _________;装置b中盛放的试剂是________ 。
②装置c中的长直导管的作用是________。
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是__________;该反应的化学方程式为____________________。
(3)探究硫脲的性质:①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是_____(填化学式,下同)
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为 ______。
③可用酸性KMnO4溶液滴定硫脲,已知MnO 被还原为Mn2+,CS(NH2)2被反应为CO2、N2及SO
被还原为Mn2+,CS(NH2)2被反应为CO2、N2及SO ,该反应中氧化剂与还原剂的物质的量之比为_____。
,该反应中氧化剂与还原剂的物质的量之比为_____。
-
氰化钠,白色结晶颗粒或粉末,易潮解,剧毒,水溶液显弱碱性,化学式为NaCN,熔点为563.1℃,是一种重要的化工原料,多用于化学合成,电镀冶金等方面。其制备工艺如下:
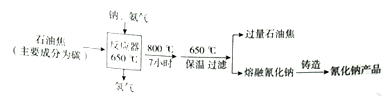
(1)制备过程的化学反应方程式为____________________________________。
(2)工厂中,氰化钠存储区应贴的标志为________(填选项字母)。

(3)已知NaCN中碳、氮原子均满足8电子稳定结构,其电子式为_____________。
(4)丙烯氨氧化法制丙烯腈的过程中有大量副产物HCN,HCN被NaOH溶液吸收,也是制备NaCN的一种重要方法。含等物质的量的NaCN和HCN的混合溶液,其pH>7,该溶液中下列关系式一定正确的是________(填选项字母)。
A.2c(Na+)=c(CN-) B.c(CN-)<c(HCN)
C.c(H+)=c(OH-)-c(HCN) D.c(Na+)-c(CN-) =c(OH-)-c(H+)
已知25℃时,HCN的电离平衡常数Ka=4.9×10-10,则该温度下NaCN的水解平衡常数Kb=________(结果保留到小数点后一位)。
(5)泄露的含NaCN的溶液可用双氧水处理,生成一种常见的酸式盐和一种常见的碱性气体,化学方程式为__________________________________。
(6)某废水样品中主要含有CN-和Cl-,若用电解法除去废水中的CN-,装置如图所示,控制废水的pH范围在9~10,阳极产生的ClO-可将CN-氧化为N2和CO32-,阳极的电极反应式为________。 除去CN-的离子反应方程式为____________________________。

-
过氧化尿素的化学式为CO(NH2)2•H2O2,是过氧化氢和尿素的加合物,外观为白色针状晶体,无毒无味,热分解温度为 45℃,易溶于水和乙醇,熔点 75-85℃,其水溶液兼有尿素和过氧化氢的性质,具有活性氧含量高、稳定性好等特点,被广泛用于医药、纺织领域。已知尿素与KMnO4溶液、NaOH 溶液都不反应。
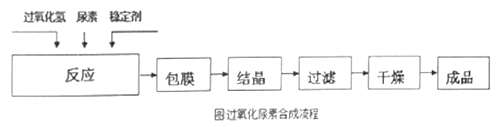
I.合成过氧化尿素的流程及反应器的示意图如下:
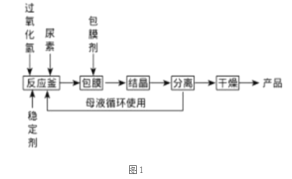
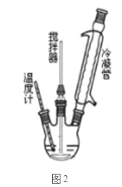
回答下列问题:
(1)图1中分离操作的名称为 _______,图 2 中反应器的名称是 _______;
(2)过氧化尿素是尿素分子与过氧化氢分子之间通过_________(填字母)结合形成的。
A.氢键 B.共价键 C.离子键 D.化学键
反应器中发生反应的化学方程式为____________。
(3)工业生产中,除向反应釜中投料反应物过氧化氢、工业尿素(含少量杂质铁、铜等离子)外,添加稳定剂可以提高产品的稳定性。不加稳定剂导致产品稳定率差的原因是 __。
(4)活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品 2.500g,溶解于水,在250mL 容量瓶中定容,准确量取其中 25.00mL 溶液于锥形瓶中,加入1mL6mol/LH2SO4,然后用0.1000mol/L KMnO4标准溶液滴定样品中的H2O2,三次滴定平均消耗KMnO4溶液 8.000mL。
①达到滴定终点的现象是____________。
②根据滴定结果确定产品质量_(填“合格”或“不合格”),活性氧的质量分数为___。
II.过氧化尿素的性质探究:
(5)过氧化尿素的催化分解实验:在试管中加入 0.1g 产品、少量水及二氧化锰,用火柴余烬检验生成气体,可观察到火柴复燃。实验中加入二氧化锰的量一定要少(固体控制在小米粒大小)的原因是:_________。
(6)测定过氧化尿素溶液的酸碱性:在试管中加入1mL 6mol/L NaOH溶液、1mL过氧化尿素溶液和 2mL无水乙醇,振荡试管。测得pH约为6,并观察到有白色的胶状沉淀生成,该沉淀为生成的NaHO2在乙醇中析出。写出该反应的化学方程式:___
-
过氧化尿素是一种新型漂白剂、消毒剂。合成过氧化尿素的流程及反应器的示意图如下:
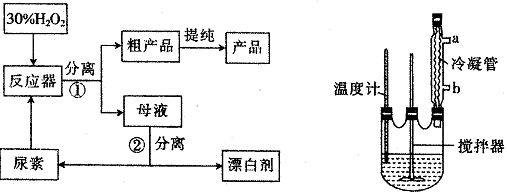
过氧化尿素的部分参数见下表:
| 分子式 | 外观 | 热分解温度 | 熔点 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75~85℃ |
(1)流程中操作①是过滤,用到的玻璃仪器有漏斗、______________和______________;
(2)反应器中发生反应的化学方程式为______________;
(3)反应器中冷凝管中的冷水从______________(填“a”或“b”)口流进,反应器加热温度不能太高的原因是______________;
(4)搅拌器不能选择铁质或铝质材料的原因是______________;
(5)为测定产品中过氧化尿素的含量,称取干燥样品12.0 g,溶于水,在250 mL容量瓶中定容。准确量取25.00 mL于锥形瓶中,加入1mL6mol/L硫酸,然后用0. 20 mol/L的KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
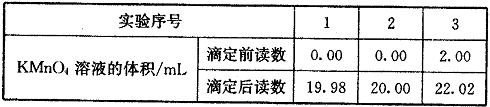
①KMnO4溶液应盛放在_________ (填“酸式”或“碱式”)滴定管中,滴定终点的现象为_________;
②若滴定前滴定管尖嘴处无气泡,滴定后有气泡。则会使测得的过氧化尿素的含量_________ (填“偏高”“偏低”或“不变”)。
③产品中过氧化尿素的质最分数为_________。
-
过氧化尿素是一种新型漂白、消毒剂,漂白、消毒效果优于H2O2和过氧乙酸,某工业用过氧化尿素的部分参数列于下表。
| 分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75—85℃ | 500g·L—1 |
合成过氧化尿素的流程及反应器的示意图如下:
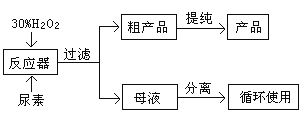
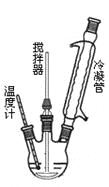
请回答下列问题:
(1)写出合成过氧化尿素的化学方程式:___________________________________。
(2)反应器里冷凝管中冷水从___(填“上”或“下”)口流入;反应器的加热方式是___。
①直接加热;②水浴加热;③蒸气浴加热;④冰浴
(3)搅拌器选用的材料是玻璃而不是铁质或铝质材料的原因是________________,
(4)从母液中分离出H2O2和尿素,采用的是减压蒸发、冷却结晶的方法,其原因是_________。
(5)活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品2.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL 6mol/LH2SO4,然后用0.1000mol/L KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液不与尿素反应),至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液6.000mL:
完成并配平下列化学方程式:
____MnO4—+ H2O2+ H+= Mn2++ H2O+ 
②KMnO4溶液应盛放在__________滴定管中,若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量__________(填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量_______(填“合格”或“不合格”),活性氧的质量分数为___________________。
-
过氧化尿素是一种新型漂白剂、消毒剂、漂白、消毒的效果优于H2O2和过氧乙酸。某工业用过氧化尿素的部分参数见下表:
| 分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 500g·L-1 |
合成过氧化尿素的步骤及反应器的示意图如下:在250mL三颈烧瓶中加入一定量的30%的H2O2溶液,再加入30g尿素,在不断搅拌下升温至300℃,使尿素完全溶解,保温30min,冷却至-5℃进行结晶。抽滤得白色粉末状结晶。在50℃下干燥2h,得过氧化尿素产品。回答下列问题:
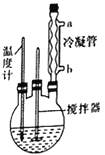
(1)控制反应温度的适宜方法是__________ (填序号)。
A.酒精灯加热 B.酒精喷灯加热 C.电炉加热 D.水浴加热
(2)反应器中发生反应的化学方程式为___________________________________。
(3)反应器中冷凝管中冷水从______(填“a”或“b”)流进;反应器加热温度不能太高的原因是___________。
(4)搅拌器不能选择铁质或铝质材料的原因是_______________________________________。
(5)为测定产品中活性氧的含量(活性氧16%,相当于含H2O234%),称取干燥样品12.000g,溶解,在250mL 容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL6mol·L-1的硫酸,然后用0.2000mol·L-1KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
| 实验序号 | 1 | 2 | 3 |
| KMnO4溶液体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
| 滴定后读数 | 19.98 | 21.70 | 22.02 |
①KMnO4溶液应盛放在__________滴定管中,滴定终点的现象是_____________。
②产品中活性氧的质量分数为____________。
③若滴定前滴定管尖嘴处无气泡,滴定后有气泡,会使测得的活性氧含量__________(填“偏高”“偏低”或“不变”)。
-
过氧化尿素是一种新型漂白剂、消毒剂、漂白、消毒的效果优于H2O2和过氧乙酸。某工业用过氧化尿素的部分参数见下表:
| 分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 500g·L-1 |
合成过氧化尿素的步骤及反应器的示意图如下:在250mL三颈烧瓶中加入一定量的30%的H2O2溶液,再加入30g尿素,在不断搅拌下升温至300℃,使尿素完全溶解,保温30min,冷却至-5℃进行结晶。抽滤得白色粉末状结晶。在50℃下干燥2h,得过氧化尿素产品。回答下列问题:
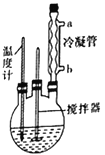
(1)控制反应温度的适宜方法是__________ (填序号)。
A.酒精灯加热 B.酒精喷灯加热 C.电炉加热 D.水浴加热
(2)反应器中发生反应的化学方程式为___________________________________。
(3)反应器中冷凝管中冷水从______(填“a”或“b”)流进;反应器加热温度不能太高的原因是___________。
(4)搅拌器不能选择铁质或铝质材料的原因是_______________________________________。
(5)为测定产品中活性氧的含量(活性氧16%,相当于含H2O234%),称取干燥样品12.000g,溶解,在250mL 容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL6mol·L-1的硫酸,然后用0.2000mol·L-1KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
| 实验序号 | 1 | 2 | 3 |
| KMnO4溶液体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
| 滴定后读数 | 19.98 | 21.70 | 22.02 |
①KMnO4溶液应盛放在__________滴定管中,滴定终点的现象是_____________。
②产品中活性氧的质量分数为____________。
③若滴定前滴定管尖嘴处无气泡,滴定后有气泡,会使测得的活性氧含量__________(填“偏高”“偏低”或“不变”)。
-
过氧化尿素[CO(NH2)2·H2O2]是一种白色粉末,溶于水形成的溶液呈弱酸性。过氧化尿素不稳定,在痕量重金属离子等活性催化剂的存在下迅速分解。工业生产过氧化尿素的原理和流程如下。
原理:CO(NH2)2+H2O2  CO(NH2)2·H2O2
CO(NH2)2·H2O2
流程:
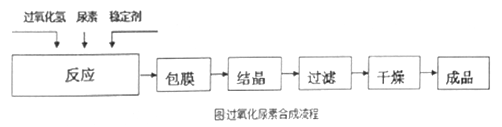
回答下列问题:
(l)已知过氧化尿素[CO(NH2)2·H2O2]中的CO(NH2)2与H2O2以氢键连接,其中碳元素的化合价是___________。(填序号)
A. +2价 B. -l价 C. 0价 D. +4价
(2)过氧化尿素鉴定反应:在重铬酸钾酸性溶液中加入乙醚和少许过氧化尿素,振荡。上层乙醚呈蓝色,这是由于在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5)。写出H2O2与重铬酸钾反应的离子方程式__________。
(3)经过上述化学工艺后的产品是粗产品。已知30℃时尿素的溶解度远大于过氧化尿素的溶解度,则提纯粗产品的操作顺序是___________ (填序号)。
①冷却至30℃结晶 ②过滤 ③蒸发浓缩 ④溶解 ⑤洗涤
(4)在实验室中采用上述原理制取过氧化尿素,搅拌器的材质一般用玻璃而非铁质,原因是___。
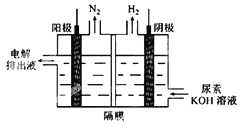
(5)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为________。
(6)Ⅰ.为测定产品中H2O2的含量,常用KMnO4溶液滴定H2O2,高锰酸钾标准溶液通常放置时间较长,因此在滴定H2O2前,常用现配的草酸钠溶液先标定出KMnO4标准溶液的浓度。
Ⅱ.称取过氧化尿素样品4.000g ,溶解在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1.00mL 6mo1/L的硫酸,用标定过的0.2000mol/L的高锰酸钾标准溶液滴定至滴入最后一滴时溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4标准溶液10.00mL,(KMnO4与尿素不反应)。
①H2O2的质量分数是_______ (精确至0.1%)。
②若装草酸钠溶液的滴定管水洗后未润洗,最终H2O2的质量分数______ (填“偏大”、“偏小”或“不变”)
-
过氧化尿素[CO(NH2)2·H2O2]是一种白色粉末,溶于水形成的溶液呈弱酸性。过氧化尿素不稳定,在痕量重金属离子等活性催化剂的存在下迅速分解。工业生产过氧化尿素的原理和流程如下。
原理:CO(NH2)2+H2O2  CO(NH2)2·H2O2
CO(NH2)2·H2O2
流程:
回答下列问题:
(l)已知过氧化尿素[CO(NH2)2·H2O2]中的CO(NH2)2与H2O2以氢键连接,其中碳元素的化合价是___________。(填序号)
A. +2价 B. -l价 C. 0价 D. +4价
(2)过氧化尿素鉴定反应:在重铬酸钾酸性溶液中加入乙醚和少许过氧化尿素,振荡。上层乙醚呈蓝色,这是由于在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5)。写出H2O2与重铬酸钾反应的离子方程式__________。
(3)经过上述化学工艺后的产品是粗产品。已知30℃时尿素的溶解度远大于过氧化尿素的溶解度,则提纯粗产品的操作顺序是___________ (填序号)。
①冷却至30℃结晶 ②过滤 ③蒸发浓缩 ④溶解 ⑤洗涤
(4)在实验室中采用上述原理制取过氧化尿素,搅拌器的材质一般用玻璃而非铁质,原因是___。
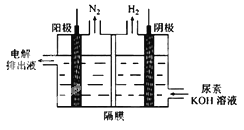
(5)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为________。
(6)Ⅰ.为测定产品中H2O2的含量,常用KMnO4溶液滴定H2O2,高锰酸钾标准溶液通常放置时间较长,因此在滴定H2O2前,常用现配的草酸钠溶液先标定出KMnO4标准溶液的浓度。
Ⅱ.称取过氧化尿素样品4.000g ,溶解在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1.00mL 6mo1/L的硫酸,用标定过的0.2000mol/L的高锰酸钾标准溶液滴定至滴入最后一滴时溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4标准溶液10.00mL,(KMnO4与尿素不反应)。
①H2O2的质量分数是_______ (精确至0.1%)。
②若装草酸钠溶液的滴定管水洗后未润洗,最终H2O2的质量分数______ (填“偏大”、“偏小”或“不变”)
。
















