-
NO、SO2是大气污染物但又有着重要用途。
I.已知:N2 (g) + O2(g) = 2NO (g) ΔH1=180.5kJ·mol−1
C(s) + O2(g) = CO2(g) ΔH2 = −393.5kJ·mol−1
2C(s) + O2(g) =2CO(g) ΔH3 =−221.0kJ·mol−1
(1)某反应的平衡常数表达式为K= , 此反应的热化学方程式为:_________
, 此反应的热化学方程式为:_________
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是_______(填序号)。
a.容器中的压强不变 b.2v正(CO)=v逆(N2)
c.气体的平均相对分子质量保持34.2不变 d.该反应平衡常数保持不变
e.NO和CO的体积比保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如下实验流程:
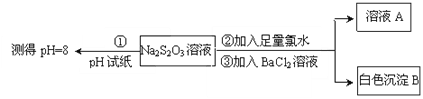
用离子方程式表示Na2S2O3溶液具有碱性的原因___________。Na2S2O3与氯水反应的离子方程式是__________。
(4)含SO2的烟气可用Na2SO3溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为_________________________(任写一个)。离子交换膜______(填标号)为阴离子交换膜。

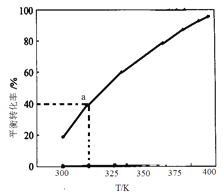
(5)2SO3(g) 2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将___________(填“向正反应方向”或“向逆反应方向” “不”) 移动。
2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将___________(填“向正反应方向”或“向逆反应方向” “不”) 移动。
-
NO、SO2是大气污染物但又有着重要用途。
I.已知:N2 (g) + O2(g) = 2NO (g) ΔH1= 180.5kJ·mol−1
C(s) + O2(g) = CO2(g) ΔH2 = −393.5kJ·mol−1
2C(s) + O2(g) =2CO(g) ΔH3 =−221.0kJ·mol−1
(1)某反应的平衡常数表达式为K=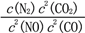 , 此反应的热化学方程式为:_________
, 此反应的热化学方程式为:_________
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是_______(填序号)。
a.容器中的压强不变 b.2v正(CO)=v逆(N2)
c.气体的平均相对分子质量保持34.2不变 d.该反应平衡常数保持不变
e.NO和CO的体积比保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如下实验流程:
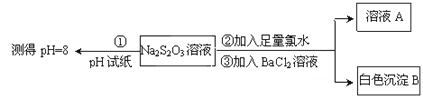
用离子方程式表示Na2S2O3溶液具有碱性的原因___________。Na2S2O3与氯水反应的离子方程式是__________。
(4)含SO2的烟气可用Na2SO3溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为_________________________(任写一个)。离子交换膜______(填标号)为阴离子交换膜。
(5)2SO3(g) 2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将___________(填“向正反应方向”或“向逆反应方向” “不”) 移动。
2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将___________(填“向正反应方向”或“向逆反应方向” “不”) 移动。

-
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g)
2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g)
2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol—1
SO3(g)+NO(g)的ΔH= kJ·mol—1
(2)利用反应6NO2+ 8NH3  7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。
7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。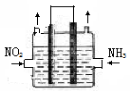
(3)一定条件下,将NO2与SO2以体积比1︰2置于恒容密闭容器中发生下述反应:NO2(g)+SO2(g) SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的物质的量比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
(4)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g) CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述
CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述 反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
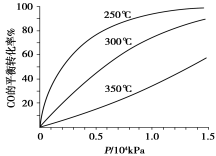
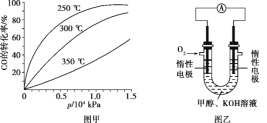
(5)不同温度CO的平衡转化率与压强的关系如上图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
-
雾霾天气给人们的出行带来了极大的不便,因此研究NO2、SO2等大气污染物的处理具有重要意义。
(1)某温度下,已知:
①2SO2(g)+O2(g) 2SO3(g) △H1=-196.6kJ/mol
2SO3(g) △H1=-196.6kJ/mol
②2NO(g)+O2(g) 2NO2(g)△H2
2NO2(g)△H2
③NO2(g)+SO2(g) SO3(g)+NO(g) △H3=-41.8kJ/mol
SO3(g)+NO(g) △H3=-41.8kJ/mol
则△H2= _____________。
(2)按投料比2:1把SO2和O2加入到一密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g) ,测得平衡时SO2的转化率与温度T、压强p的关系如图甲所示:
2SO3(g) ,测得平衡时SO2的转化率与温度T、压强p的关系如图甲所示:
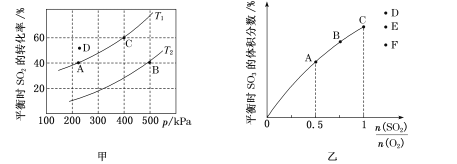
①A、B两点对应的平衡常数大小关系为KA __________(填“>”“<”或“=”,下同)KB;温度为T,时D点vD正与vD逆的大小关系为vD正 _____________vD逆;
②T1温度下平衡常数Kp=______________ kPa-1(Kp为以分压表示的平衡常数,结果保留分数形式)。
(3)恒温恒容下,对于反应2SO2(g)+O2(g) 2SO3(g),测得平衡时SO3的体积分数与起始
2SO3(g),测得平衡时SO3的体积分数与起始 的关系如图乙所示,则当
的关系如图乙所示,则当 =1.5达到平衡状态时,SO2的体积分数是图乙中D、E、F三点中的____________点。A、B两点SO2转化率的大小关系为aA ___(填“>”“<”或“=”)aB。
=1.5达到平衡状态时,SO2的体积分数是图乙中D、E、F三点中的____________点。A、B两点SO2转化率的大小关系为aA ___(填“>”“<”或“=”)aB。
(4)工业上脱硫脱硝还可采用电化学法,其中的一种方法是内电池模式(直接法),烟气中的组分直接在电池液中被吸收及在电极反应中被转化,采用内电池模式将SO2吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入SO2电极的反应式:____________;若40%的硫酸溶液吸收氨气获得(NH4)2SO4的稀溶液,测得常温下,该溶液的pH=5,则 ___________(计算结果保留一位小数,已知该温度下NH3·H2O的Kb=1.7×10-5);若将该溶液蒸发掉一部分水后恢复室温,则
___________(计算结果保留一位小数,已知该温度下NH3·H2O的Kb=1.7×10-5);若将该溶液蒸发掉一部分水后恢复室温,则 的值将_____(填“变大”“不变”或“变小”)。
的值将_____(填“变大”“不变”或“变小”)。
-
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:Ⅰ.2SO2(g) + O2(g) 2SO3(g)ΔH=-196.6 kJ· mol-1
2SO3(g)ΔH=-196.6 kJ· mol-1
Ⅱ.2NO(g) + O2(g)  2NO2(g)ΔH=-113.0 kJ· mol-1
2NO2(g)ΔH=-113.0 kJ· mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=____kJ· mol-1。
SO3(g)+NO(g)的ΔH=____kJ· mol-1。
(2)一定条件下,将NO2(g)与SO2(g)以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是____。
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变 D.每消耗1 mol SO3的同时生成1 mol NO
(3)CO可用于合成甲醇,化学方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图甲所示,该反应的ΔH____0(填“>”或“<”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图甲所示,该反应的ΔH____0(填“>”或“<”)。
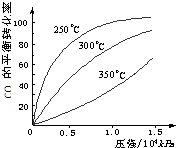
(4)依据燃烧的反应原理,合成的甲醇可以设计成如图乙所示的原电池装置。
①该电池工作时,OH-向____(填“正”或“负”)极移动。
②该电池正极的电极反应式为___________。
-
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)已知:2SO2(g)+O2(g)⇌2SO3(g)△H=-Q1kJ•mol-1
2NO(g)+O2(g)⇌2NO2(g)△H=-Q2kJ•mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g) 的△H=______kJ•mol-1.
(2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,当测得上述反应平衡时NO2与NO体积比为1:3,则平衡常数K=______.
(3)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)⇌CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H______0(填“>”或“<”).
Ⅱ.已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性.
(1)用离子方程式解释Na2C2O4溶液显碱性的原因______;
(2)常温下,比较0.1mol•L-1NaHC2O4溶液中各种离子浓度的大小关系______;
Ⅲ.某课外活动小组为了探究的BaSO4溶解度,分别将足量BaSO4放入:a.5ml 水;b.40ml 0.2mol•L-1的Ba(OH)2溶液;c.20ml 0.5mol•L-1的Na2SO4溶液;d.40ml 0.1mol•L-1的H2SO4溶液中,溶解至饱和.
(1)以上各溶液中,的浓度由大到小的顺序为______;
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
(2)某同学取同样的溶液b和溶液d直接混合,则混合溶液的pH值为______(设混合溶液的体积为混合前两溶液的体积之和).
-
用化学反应原理研究氮的氧化物和硫的氧化物有着重要的意义。
(1)已知:2SO2(g)+ O2(g)  2SO3(g) △H1
2SO3(g) △H1
2NO(g)+ O2(g)  2NO2 (g) △H2
2NO2 (g) △H2
NO2 (g) + SO2(g)  SO3(g) + NO(g) △H3
SO3(g) + NO(g) △H3
则△H3 = (用△H1、△H2 表示),如果上述三个反应方程式的平衡常数分别为K1、 K2、K3,则K3 = (用K1、K2 表示)。
(2)如图所示,A 是恒容的密闭容器,B 是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2mol NO 和1 mol O2 通过K1、K3 分别充入A、B 中,发生的反应为2NO(g)+ O2(g) 2NO2 (g) [不考虑2NO2 (g)
2NO2 (g) [不考虑2NO2 (g)  N2 O4 (g) ],起始时A、B 的体积相同均为a L。
N2 O4 (g) ],起始时A、B 的体积相同均为a L。
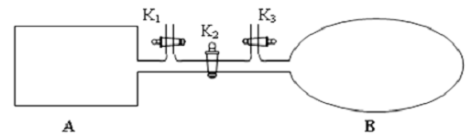
①下列说法和示意图正确,且既能说明A 容器中反应达到平衡状态,又能说明B 容器中反应达到平衡状态的是 。
a. A、B 容器中气体的颜色均不再发生变化
b. A、B 容器中NO 和O2物质的量浓度比均为2:1

② T℃时,A 容器中反应达到平衡时的平衡常数Kp = 8×10﹣2 (kPa) ﹣1 。若A 容器中反应达到平衡时p(NO2) = 200kPa,则平衡时NO的转化率为 。(Kp 是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数)
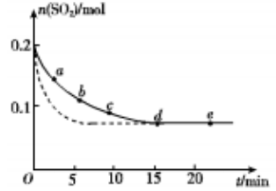
(3)将0.2 mol SO2 和0.15 mol O2通入2L 的密闭容器中,测得SO2的物质的量随时间变化如 图实线 所示。
| 编号 | a | b | c | d | e |
| n(SO2)/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
①ab 段平均反应速率 (填“大于”“小于”或“等于”)bc 段平均反应速率:de 段平均反应速率为 。
②仅改变某一个实验条件,测得SO2 的物质的量随时间变化如图中虚线所示,则改变的条件是 。
-
用化学反应原理研究氮的氧化物和硫的氧化物有着重要的意义。
(1)已知:2SO2(g)+ O2(g) 2SO3(g) △H1
2SO3(g) △H1
2NO(g)+ O2(g) 2NO2 (g) △H2
2NO2 (g) △H2
NO2 (g) + SO2(g) SO3(g) + NO(g) △H3
SO3(g) + NO(g) △H3
则△H3 =__________(用△H1、△H2表示),如果上述三个反应方程式的平衡常数分别为K1、 K2、K3,则K3 =__________(用K1、K2表示)。
(2)如图所示,A 是恒容的密闭容器,B 是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2mol NO 和1 mol O2通过K1、K3分别充入A、B 中,发生的反应为2NO(g)+ O2(g) 2NO2 (g) [不考虑2NO2 (g)
2NO2 (g) [不考虑2NO2 (g) N2 O4 (g) ],起始时A、B 的体积相同均为a L。
N2 O4 (g) ],起始时A、B 的体积相同均为a L。
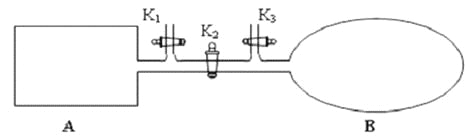
①下列说法和示意图正确,且既能说明A 容器中反应达到平衡状态,又能说明B 容器中反应达到平衡状态的是_________。
a. A、B 容器中气体的颜色均不再发生变化
b. A、B 容器中NO 和O2物质的量浓度比均为2:1

② T℃时,A 容器中反应达到平衡时的平衡常数Kp = 8×10﹣2 (kPa)﹣1。若A 容器中反应达到平衡时p(NO2) = 200kPa,则平衡时NO的转化率为_____________。(Kp 是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数)
(3)将0.2 mol SO2和0.15 mol O2通入2L 的密闭容器中,测得SO2的物质的量随时间变化如 图实线 所示。
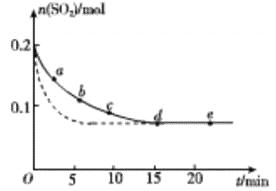
| 编号 | a | b | c | d | e |
| n(SO2)/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
①ab 段平均反应速率____________(填“大于”“小于”或“等于”)bc 段平均反应速率:de 段平均反应速率为_________________。
②仅改变某一个实验条件,测得SO2的物质的量随时间变化如图中虚线所示,则改变的条件是__________。
-
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)  2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
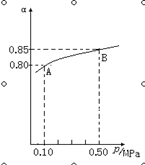
①平衡状态由A到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为________。
该反应的平衡常数为________。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为________;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是________。
-
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)  2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
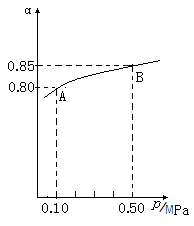
①平衡状态由A到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为________。
该反应的平衡常数为________。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=—574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=—1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为________;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是________。
 , 此反应的热化学方程式为:_________
, 此反应的热化学方程式为:_________

2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将___________(填“向正反应方向”或“向逆反应方向” “不”) 移动。

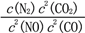 , 此反应的热化学方程式为:_________
, 此反应的热化学方程式为:_________














