-
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A. 浓度均为0.1 mol/L的Na2CO3与NaHCO3混合溶液:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B. 0.1mol·L-1CH3COOH与0.05mol·L-1NaOH溶液等体积混合(pH<7):c(CH3COO-)>c(Na+)>cCH3COOH)>c(H+)
C. 0.1 mol·L-1Na2CO3与0.05mol·L-1 NaHCO3溶液等体积混合:5c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)]
D. 在0.1 mol·L-1NaHC2O4溶液(pH<7)中:c(OH-)+c(C2O42-)=c(H+)+c(H2C2O4)
-
Na2CO3和NaHCO3在生活和生产中应用广泛。
(1)室温时下列指定溶液中微粒物质的量浓度关系正确的是_____ (填字母) .
A.0.1mol·L-1的Na2CO3溶液: c(Na+)+c(H+) =c(OH-)+c(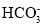 )+c(
)+c(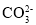 )
)
B.0.1mol·L-1的NaHCO3溶液: c(Na+) =c(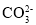 ) + c(
) + c(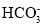 )+ c(H2CO3)
)+ c(H2CO3)
C.0.1mol·L-1的NaHCO3溶液: c(Na+)>c(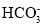 )>c(
)>c(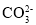 )>c(H2CO3)
)>c(H2CO3)
D.浓度均为0.1mol·L-1的Na2CO3和NaHCO3混合溶液:2c(H+)+c(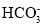 )+3c(H2CO3)=2c(OH-)+c(
)+3c(H2CO3)=2c(OH-)+c(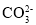 )
)
(2)水垢中的CaSO4可用Na2CO3溶液处理。当两种沉淀共存时, 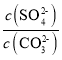 =________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
=________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
(3) 25℃时,碳酸及其盐溶液中含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。
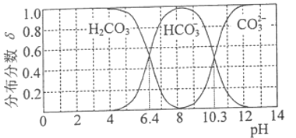
①纯碱溶液去油污的原理是_________(用离子方程式表示) 。25℃时,该反应的平衡常数表示为Kh,则pKh=_________(pKh=-lgKh)。
②25C时,下列三种溶液
A.0.1mol·L-1的NaHCO3溶液:
B.0.1mol·L-1的Na2CO3溶液:
C.0.1mol·L-1的NaCN溶液。
pH由大到小的顺序为________________(填字母)。[25℃时,K(HCN)= 10-9.3]
(4)NaHCO3可用于铝土矿(主要成分为Al2O3,含SiO2和Fe2O3)制铝。流程如下:
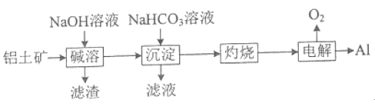
①滤渣中除含SiO2转化得到的铝硅酸钠外,还含_____(填化学式) 。
②写出“沉淀"步骤发生反应的离子方程式________和________。
-
Na2CO3和NaHCO3在生活和生产中应用广泛。
(1)室温时下列指定溶液中微粒物质的量浓度关系正确的是_____ (填字母) .
A.0.1mol·L-1的Na2CO3溶液: c(Na+)+c(H+) =c(OH-)+c(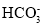 )+c(
)+c(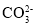 )
)
B.0.1mol·L-1的NaHCO3溶液: c(Na+) =c(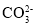 ) + c(
) + c(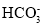 )+ c(H2CO3)
)+ c(H2CO3)
C.0.1mol·L-1的NaHCO3溶液: c(Na+)>c(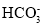 )>c(
)>c(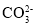 )>c(H2CO3)
)>c(H2CO3)
D.浓度均为0.1mol·L-1的Na2CO3和NaHCO3混合溶液:2c(H+)+c(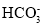 )+3c(H2CO3)=2c(OH-)+c(
)+3c(H2CO3)=2c(OH-)+c(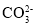 )
)
(2)水垢中的CaSO4可用Na2CO3溶液处理。当两种沉淀共存时, 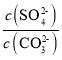 =________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
=________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
(3) 25℃时,碳酸及其盐溶液中含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。
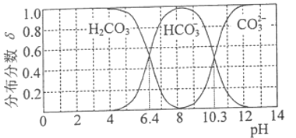
①纯碱溶液去油污的原理是_________(用离子方程式表示) 。25℃时,该反应的平衡常数表示为Kh,则pKh=_________(pKh=-lgKh)。
②25C时,下列三种溶液
A.0.1mol·L-1的NaHCO3溶液:
B.0.1mol·L-1的Na2CO3溶液:
C.0.1mol·L-1的NaCN溶液。
pH由大到小的顺序为________________(填字母)。[25℃时,K(HCN)= 10-9.3]
(4)NaHCO3可用于铝土矿(主要成分为Al2O3,含SiO2和Fe2O3)制铝。流程如下:
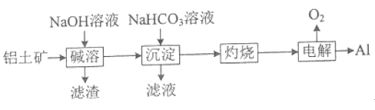
①滤渣中除含SiO2转化得到的铝硅酸钠外,还含_____(填化学式) 。
②写出“沉淀"步骤发生反应的离子方程式________和________。
-
常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体。下列指定溶液中微粒浓度大小比较正确的是[注:Kb(NH3·H2O)=1.7×10-5 mol•L-1、Ka1(H2CO3)=4.2×10-7 mol•L-1、K a2 (H2CO3)=5.6×10-11 mol•L-1]
A. 原NH4HCO3 溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+)
B. 原NH4HCO3溶液中c(OH-)= c(H+)- c(CO32-)- c(NH3·H2O)+ c(H2CO3)
C. 析出晶体后的溶液中:c(Cl-) =c(NH4+),c(Na+)= c(HCO3-)
D. 析出晶体后的溶液中:c(Cl-)+c(OH-)+c(Na+)=c(NH4+)+c(H+)+c(HCO3-)
-
H2A为二元弱酸。室温下,下列指定溶液中微粒物质的量浓度关系正确的是(忽略溶液混合引起的体积变化)( )
A.0.1mol/LH2A溶液:c(H2A)>c(HA-)>c(A2-)>c(H+)
B.0.1mol/LNaHA溶液(pH<7):c(Na+)>c(HA-);c(H2A)>c(A2-)
C.0.1mol/LNaHA溶液和0.1mol/LNaOH溶液等体积混合:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.0.1mol/LNaHA溶液(pH<7)和0.1mol/LH2A溶液等体积混合:c(Na+)>c(HA-)+2c(A2-)
-
下列溶液中微粒的物质的量浓度关系正确的是( )
A.室温下,向0.1 mol•L-1NH4HSO4溶液中滴加等物质的量溶质的NaOH溶液:[Na+]=[SO ]>[NH
]>[NH ]>[OH-]=[H+]
]>[OH-]=[H+]
B.0.1 mol•L-1NaHCO3溶液:[Na+]>[OH-]>[HCO ]>[H+]
]>[H+]
C.Na2CO3溶液:[OH-]-[H+]=[HCO ]+2[H2CO3]
]+2[H2CO3]
D.25℃时,pH=4.75,浓度均为0.1 mol•L-1的CH3COOH、CH3COONa混合溶液:[CH3COO-]+[OH-]<[CH3COOH]+[H+]
-
下列溶液中有关微粒的物质的量浓度关系正确的是( )
A. NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)= c(HRO3-)+2c(RO32﹣)
B. 常温下将物质的量浓度相等的醋酸钠、醋酸两溶液等体积混合,混合后的溶液中,已知c(Na+)>c(CH3COOH),则:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C. 常温下,物质的量浓度和体积都相等的①Na2SO3②Na2SO4③NaHSO4三种溶液中离子总数:①<②<③
D. 常温下,①pH=3的HCl溶液和pH=11的氨水等体积混合液 ②pH=3的HCl溶液 ③pH=11
的氨水中由水电离出的c(H+):①>③>②
-
下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A. 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3,其中c(CO32-)的大小关系为:②>④>③>①
B. pH=2 的H2C2O4溶液与pH=12 的NaOH 溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. 向0.2mo/L 的NaHCO3 溶液中加入等体积0.1mo/L 的NaOH 溶液:c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. 常温下,等浓度的CH3COOH与CH3COONa 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
-
下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A. 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3,其中c(CO32-)的大小关系为:②>④>③>①
B. pH=2 的H2C2O4溶液与pH=12 的NaOH 溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. 向0.2mo/L 的NaHCO3 溶液中加入等体积0.1mo/L 的NaOH 溶液:c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. 常温下,等浓度的CH3COOH与CH3COONa 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
-
下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A. 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3,其中c(CO32-)的大小关系为:②>④>③>①
B. pH=2 的H2C2O4溶液与pH=12 的NaOH 溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. 向0.2mo/L 的NaHCO3 溶液中加入等体积0.1mo/L 的NaOH 溶液:c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. 常温下,等浓度的CH3COOH与CH3COONa 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
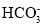 )+c(
)+c(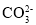 )
)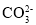 ) + c(
) + c(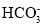 )+ c(H2CO3)
)+ c(H2CO3)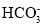 )>c(
)>c(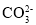 )>c(H2CO3)
)>c(H2CO3)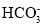 )+3c(H2CO3)=2c(OH-)+c(
)+3c(H2CO3)=2c(OH-)+c(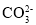 )
)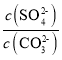 =________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
=________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]

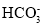 )+c(
)+c(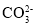 )
)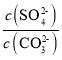 =________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
=________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
