某原电池装置如图所示。
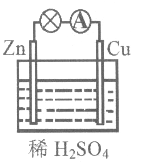
(1)负极的电极反应式是________,该反应属于_______ (填“氧化”或“还原”)反应。
(2)电子由________(填“锌片”或“铜片”)沿导线流出。
(3)当铜表面析出0.224 L氢气(标准状况)时,导线中通过了________mol电子。
高一化学原理综合题中等难度题
某原电池装置如图所示。

(1)负极的电极反应式是________,该反应属于_______ (填“氧化”或“还原”)反应。
(2)电子由________(填“锌片”或“铜片”)沿导线流出。
(3)当铜表面析出0.224 L氢气(标准状况)时,导线中通过了________mol电子。
高一化学原理综合题中等难度题
某原电池装置如图所示。
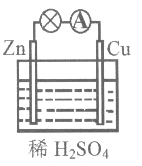
(1)负极的电极反应式是________,该反应属于_______ (填“氧化”或“还原”)反应。
(2)电子由________(填“锌片”或“铜片”)沿导线流出。
(3)当铜表面析出0.224 L氢气(标准状况)时,导线中通过了________mol电子。
高一化学综合题中等难度题查看答案及解析
关于如图所示的铜锌原电池装置,叙述正确的是
A. Zn做正极被氧化
B. Zn做负极被还原
C. 铜做正极, 电极上发生还原反应
D. 铜做正极,电极上发生氧化反应
高一化学单选题简单题查看答案及解析
由铜片、锌片和200mL稀H2SO4组成的原电池中(如图所示装置),请按要求填空: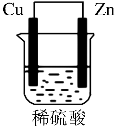
(1) 为正极,发生 反应(“氧化”或“还原”),现象是 ,电极反应式为 ; 为负极,发生 反应(“氧化”或“还原”),现象是 ,电极反应式为 。
(2)H+向 极移动,电子流动方向为 →导线→ (填电极材料)
(3)若锌片只发生电化学反应,则当铜片上共放出3.36L(标准状况)气体时,H2SO4恰好完全消耗。求:
①反应中消耗的锌的质量
②有 个电子通过了导线.
③原稀H2SO4的物质的量浓度是
高一化学填空题中等难度题查看答案及解析
化学电池的发明,是贮能和供能技术的巨大进步。
(1)如图所示装置中,Zn片是_____ (填“正极”或“负极”),Cu片上发生的电极反应为_____。

(2)该装置是典型的原电池装置,可将氧化还原反应释放的能量直接转变为电能,能证明产生电能的实验现象是_____。
(3)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如图:
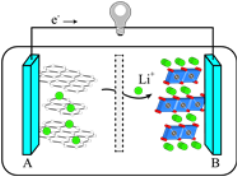
下列说法不正确的是_____(填序号)。
①A为电池的正极
②该装置实现了电能转化为化学能
③电池工作时,电池内部的锂离子定向移动
高一化学填空题中等难度题查看答案及解析
某原电池装置如图所示。

(1)其负极是_________(填“Zn”或“Cu”),发生的是__________(填“氧化”或“还原”)反应,电极反应式为___________________ 。
(2)正极上的现象是________________________________________。
(3)电子由_______________(填“锌片”或“铜片”)沿导线流出。
(4)电池总反应的离子方程式是_________________________________。
高一化学填空题中等难度题查看答案及解析
某原电池装置如图所示。

(1)其负极是_________(填“Zn”或“Cu”),发生的是__________(填“氧化”或“还原”)反应,电极反应式为___________________ 。
(2)正极上的现象是________________________________________。
(3)电子由_______________(填“锌片”或“铜片”)沿导线流出。
(4)电池总反应的离子方程式是_________________________________。
高一化学填空题中等难度题查看答案及解析
某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
|
| Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_____________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________。
高一化学实验题中等难度题查看答案及解析
某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
|
| Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_____________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________。
高一化学实验题中等难度题查看答案及解析
利用氧化还原反应Fe+H2SO4=FeSO4+H2↑设计了一个原电池,如装置图,注明电极名称、反应类型,写出电极反应式。
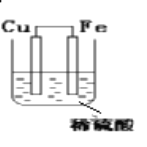
负极(_____):电极反应:___________________________ _________反应
正极(_____):电极反应:___________________________ _________反应
高一化学填空题简单题查看答案及解析

高一化学填空题中等难度题查看答案及解析