-
对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题(用元素符号或化学式回答)。
族
周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
1
①
②
2
③
④
⑤
⑥
3
⑦
⑧
⑨
⑩
(1)在上述元素中,金属性最强的是___,原子半径最大的是___(0族除外)。
(2)用电子式表示⑦和⑩形成的化合物的过程___。
(3)表中元素构成10电子微粒的分子有:___(任写2种)。
(4)⑤和⑨分别与氢原子构成的简单氢化物中沸点最高的是___。
(5)表中元素⑤和⑦可以形成一种淡黄色物质X,写出X的电子式:___,该物质所含化学键类型___,0.1molX与水反应转移电子数为___。
高一化学推断题中等难度题查看答案及解析
-
对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题(用元素符号或化学式回答):
Ⅰ A
Ⅱ A
Ⅲ A
Ⅳ A
Ⅴ A
Ⅵ A
Ⅶ A
0
1
①
②
2
③
④
⑤
⑥
3
⑦
⑧
⑨
⑩
(1)其中原子半径最小的是 元素,没有正化合价的是 元素。
(2)其中非金属元素有 _________种,非金属性最强的是 元素。
(3)其中气态氢化物溶于水呈碱性的是________元素,其气态氢化物的化学式是 。
(4)其中最高价氧化物对应水化物碱性最强的是 元素, 其最高价氧化物对应水化物化学式是 其最高价氧化物对应化物含有的化学键类型是______________。
(5)⑩ 号元素最高正价含氧酸只具有________键
高一化学填空题困难题查看答案及解析
-
表是元素周期表的一部分,请用元素符号、离子符号或相关化学式回答有关问题:
主族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
①
②
③
3
④
⑤
⑥
⑦
⑧
4
⑨
⑩
(1)表中能形成两性氢氧化物的元素在周期表中的位置是________;
(2)写出②的气态氢化物的结构式________;
(3)元素④⑤⑥⑦离子半径由大到小的顺序________;
(4)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是________;④、⑤、⑨三种元素的最高价氧化物的水化物中碱性最强的是________;
(5)⑦和⑩氧化性较强的是________用一个置换反应证实这一结论(写化学方程式)___________________________。
(6)④⑤两元素相比较,金属性较强的是________,可以验证该结论的实验是________;
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质用砂纸打磨后分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质用砂纸打磨后分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
高一化学推断题中等难度题查看答案及解析
-
下表是元素周期表的一部分。
根据①~⑿元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
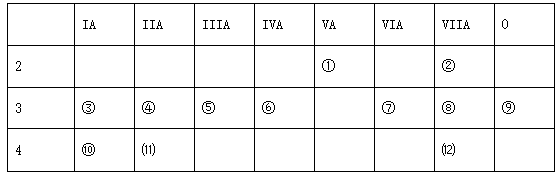
(1)写出下列元素符号:① ,⑥ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。(用化学式填写)
(3)在这些元素中单质的氧化性最强的是 ,还原性最强的是 。化学性质最不活泼的元素是 。(用化学式填写)
(4)画出原子结构示意图:⑾ 。
(5)用电子式表示⑦和⑩形成化合物的过程: 。
(6)⑦和⑧分别形成的气态氢化物的化学式是 、 。其中相对不稳定的是 。
(7)在③与④中,化学性质较活泼的是 ,(填元素符号)
在⑧与⑿中,化学性质较活泼的是 ,(填元素符号)如何证明(用离子方程式表示):
。
高一化学填空题简单题查看答案及解析
-
下表是元素周期表的一部分。
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
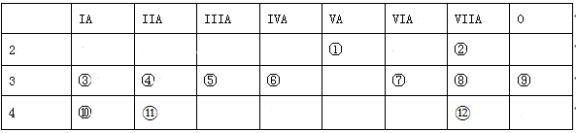
(1)写出下列元素符号:① ,⑥ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,呈两性的氢氧化物是 。(用化学式填写)
(3)在这些元素中单质的氧化性最强的是 ,还原性最强的是 。化学性质最不活泼的元素是 。(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程: 。
(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是 。
高一化学填空题中等难度题查看答案及解析
-
(12分)下表是元素周期表的一部分,请用元素符号或化学式回答有关问题:
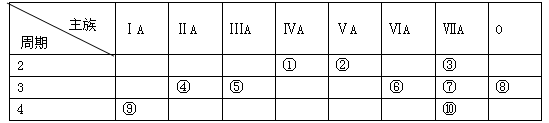
(1)表中化学性质最不活泼的元素是 ,最活泼的金属元素是 ,最活泼的非金属元素是 。
(2)表中能形成两性氧化物的元素是 ,写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式 。
(3)③⑥⑦三种元素原子半径由大到小的顺序是 。
(4)用电子式表示由元素⑨⑦形成化合物的过程: 。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
实验步骤
实验现象与结论
高一化学填空题中等难度题查看答案及解析
-
下表是元素周期表的前四周期,请回答有关问题:(相关问题均用具体化学用语回答)
1
①
2
②
③
④
3
⑤
⑥
⑦
⑧
4
⑨
⑩
(1)④的原子结构示意图为_________;②在元素周期表位置________;上述元素中最高价氧化物的水化物酸性最强的是_________;(填水化物化学式)
(2)⑤的最高价氧化物的水化物和⑥的最高价氧化物反应的离子方程式________________
(3)用电子式表示元素①和⑧形成的化合物的形成过程________________
(4)⑤的最高价氧化物水化物的电子式________________
(5)请设计实验证明⑧与⑩的氧化性强弱________________
高一化学推断题中等难度题查看答案及解析
-
下表是元素周期表的一部分,请回答有关问题:
(1)最活泼的非金属元素是______(用元素符号或化学式表示,下同);碱性最强的是______,该物质存在的化学键类型是______
主族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 2 ① ② ③ 3 ④ ⑤ ⑥ ⑦ ⑧ ⑨
(2)⑤元素与⑧元素形成化合物的电子式是______
(3)③⑦⑧三种元素原子半径由小到大的顺序是______
(4)将⑤⑥两种单质用导线相连后,同时浸入稀硫酸中,⑥这一极发生______(填“氧化”或“还原”)反应.高一化学解答题中等难度题查看答案及解析
-
下表是元素周期表的前四周期,请回答有关问题:(相关均用具体化学用语回答)
1
①
2
②
③
④
3
⑤
⑥
⑦
⑧
4
⑨
⑩
(1)元素⑤⑥⑦的简单离子半径大小顺序__________;②在元素周期表位置________;③的简单氢化物和⑧的氢化物混合形成的化合物电子式__________。
(2)⑤其最高价氧化物水合物和⑥的最高价氧化物反应的离子方程式_______
(3)用电子式表示元素①和⑧形成的化合物的形成过程__________。
(4)④、⑧、⑩的氢化物沸点最高的是__________,原因是__________。
(5)由②和①组成最简单物质与O2和⑨的最高价氧化物对应的水化物的水溶液组成燃料电池,写出电池的负极反应式__________。
高一化学综合题中等难度题查看答案及解析
-
(19分)下表是元素周期表的一部分,回答下列有关问题:(填写元素符号或化学式)
族
周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
2
①
②
3
③
④
⑤
⑥
⑦
⑧
4[]
⑨
⑩
(1)写出下列元素符号:
①________,⑥________,⑦________,⑧________。
(2)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________。
(3)在这些元素中的最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是________ ,呈两性的氢氧化物是________,写出实验室制取①的氢化物的化学方程式 ________
(4)含有元素③的物质的焰色呈________,⑩的单质的保存方法是 ________
(5)在③与④中,化学性质较活泼的是________ ,怎样用化学实验证明?(可用化学方程式说明) ________
在⑧与⑩中,化学性质活泼的是________,怎样用化学实验证明?(可用化学方程式说明)
【解析】考查元素周期表的结构和元素周期律的应用。根据元素在周期表做的位置可判断①是N、②是F、③是Na、④是Mg、⑤是Al、⑥是Si、⑦是S、⑧是Cl、⑨是K、⑩是Br。同主族元素自上而下原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强,金属性逐渐减弱。
高一化学填空题简单题查看答案及解析