25℃时,向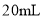
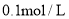
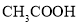 溶液中滴入
溶液中滴入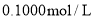
 溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )
溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )
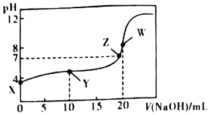
A.若X点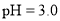 ,则醋酸的电离度约为1%
,则醋酸的电离度约为1%
B.若Y点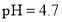 ,则
,则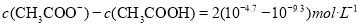
C.Z点溶液中离子浓度: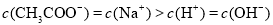
D.若W点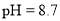 ,则溶液中由水电离出的
,则溶液中由水电离出的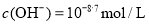
高三化学单选题中等难度题
25℃时,向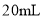
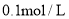
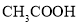 溶液中滴入
溶液中滴入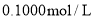
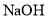 溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )
溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )

A.若X点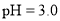 ,则醋酸的电离度约为1%
,则醋酸的电离度约为1%
B.若Y点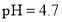 ,则
,则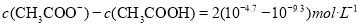
C.Z点溶液中离子浓度: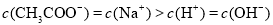
D.若W点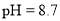 ,则溶液中由水电离出的
,则溶液中由水电离出的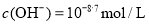
高三化学单选题中等难度题
常温下,pH=12的氢氧化钠溶液pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
A.混合前的醋酸约1%发生电离
B.混合后的溶液中c(Na+)<c(CH3COO-)
C.氢氧化钠和醋酸和浓度不相等
D.混合后的溶液呈中性
高三化学选择题中等难度题查看答案及解析
常温下,pH=12的氢氧化钠溶液pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
A.混合前的醋酸约1%发生电离 B.混合后的溶液中
C.氢氧化钠和醋酸和浓度不相等 D.混合后的溶液呈中性
高三化学选择题中等难度题查看答案及解析
常温下,pH = 12的氢氧化钠和pH = 4的醋酸等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
A.混合前的醋酸约1%发生电离 B.混合后的溶液中c(Na+)=c(CH3COO—)
C.氢氧化钠和醋酸的浓度不相等 D.混合后的溶液呈中性
高三化学选择题简单题查看答案及解析
常温下,向20mL0.1mol·L-1HA溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法错误的是
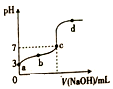
A. HA的电离方程式为HAH++A-
B. HA完全反应时,溶液所对应的点位于c和d之间
C. 滴定到c点时:c(Na+)>c(A-)>c(H+)=c(OH-)
D. 滴定到d点时:n(Na+)+n(H+)-n(OH-)+n(HA)=0.002mol
高三化学选择题中等难度题查看答案及解析
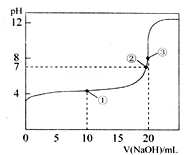
已知常温下,向溶液中,滴入
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)()

A.若A点的,则此温度下醋酸的电离度计算式为
B.B点存在等式关系:
C.若C点加入氢氧化钠溶液amL,则常温下醋酸的电离平衡常数计算式为
D.若D点,则由水电离出的
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
常温下,将盐酸慢慢加入到
浓度为
溶液中,所得溶液pH变化曲线如图所示
忽略体积变化
。下列说法不正确的是
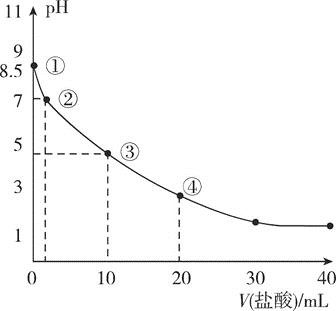
A. 点所示溶液中由水电离产生的
B. 点所示溶液中:
C. 点所示溶液中:
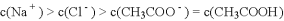
D. 点所示溶液中:
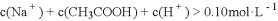
高三化学单选题中等难度题查看答案及解析
室温下,将醋酸慢慢滴入到盛
蒸馏水的烧杯中,烧杯溶液中的
和温度随着加入醋酸体积的变化曲线如图所示,则下列有关说法正确的是
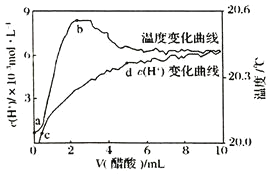
A.段,温度升高,可知醋酸电离过程中
键断裂为放热过程
B.段,
增加,醋酸电离程度增大
C.c点时,加入等体积等浓度的NaOH溶液,则:
D.d点时,
高三化学单选题困难题查看答案及解析
室温下,将醋酸慢慢滴入到盛
蒸馏水的烧杯中,烧杯溶液中的
和温度随着加入醋酸体积的变化曲线如图所示,则下列有关说法正确的是
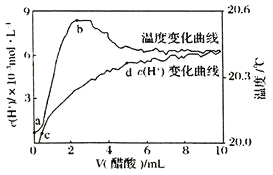
A.段,温度升高,可知醋酸电离过程中
键断裂为放热过程
B.段,
增加,醋酸电离程度增大
C.c点时,加入等体积等浓度的NaOH溶液,则:
D.d点时,
高三化学单选题困难题查看答案及解析
25℃时,向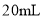
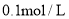
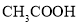 溶液中滴入
溶液中滴入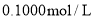
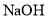 溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )
溶液,忽略温度变化,所得曲线如图所示。下列说法错误的是( )

A.若X点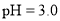 ,则醋酸的电离度约为1%
,则醋酸的电离度约为1%
B.若Y点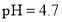 ,则
,则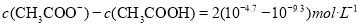
C.Z点溶液中离子浓度: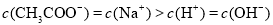
D.若W点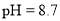 ,则溶液中由水电离出的
,则溶液中由水电离出的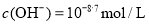
高三化学单选题中等难度题查看答案及解析