-
一定条件下,测得反应3CO(g)+3H2(g) (CH3)2O(g)+CO2(g)达平衡时CO的平衡转化率与温度和压强的关系如图所示(假定过程中不发生其他反应)。温度为T时,向体积为1 L的恒容密闭容器中充入0.4 mol CO和0.4 mol H2,反应达平衡时测得CO2物质的量为0.1 mol。下列说法正确的是( )
(CH3)2O(g)+CO2(g)达平衡时CO的平衡转化率与温度和压强的关系如图所示(假定过程中不发生其他反应)。温度为T时,向体积为1 L的恒容密闭容器中充入0.4 mol CO和0.4 mol H2,反应达平衡时测得CO2物质的量为0.1 mol。下列说法正确的是( )
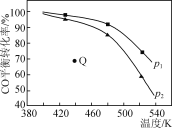
A.该反应的ΔH<0,图中压强p1>p2
B.压强为p2时,图中Q点所示条件下v(正)<v(逆)
C.温度为T时,若向体积为1 L的恒压容器中充入0.4 mol CO和0.4 mol H2,达平衡时CO的转化率大于75%
D.温度为T时,若向原容器中充入0.1 mol CO、0.2 mol(CH3)2O和0.2 mol CO2,则该反应的平衡常数大于104
-
一定条件下的密闭容器中,反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)△H<0达到平衡,要提高CO的转化率,可以釆取的措施是( )
CH3OCH3(g)+CO2(g)△H<0达到平衡,要提高CO的转化率,可以釆取的措施是( )
A. 升高温度 B. 加入催化剂 C. 减小CO2的浓度 D. 增加CO的浓度
-
(1)一定条件下的密闭容器中,反应3H2(g)+3CO(g) CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
a.升高温度 b.加入催化剂 c.减小CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(2)已知反应②2CH3OH(g) CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)= ;该时间内反应速率v(CH3OH)= 。
-
已知:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2(g) ΔH=-247kJ/mol,一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是( )
CH3OCH3(g) + CO2(g) ΔH=-247kJ/mol,一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是( )
A. 低温高压 B. 加入催化剂 C. 体积不变充入氦气 D. 增加CO的浓度
-
放热反应3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g)在一定条件下的密闭容器中达到平衡后,采取下列措施可时CO的转化率提高的组合( )
①升温 ②加压(缩小体积) ③加催化剂 ④减小CO2的浓度 ⑤增大CO的浓度 ⑥增大H2的浓度 ⑦分离出CH3OCH3.
A.①②④⑥⑦
B.③④⑤⑥⑦
C.②④⑥⑦
D.①②③④⑤⑥⑦
-
(1)利用CO、H2制造CH3OCH3有三个途径:
CO(g)+H2(g)═CH3OH(g) △H1=-91kJ•mol-1 平衡常数K1
2CH3OH(g)═CH3OCH3(g)+H2O △H2=-24kJ•mol-1 平衡常数K2
CO(g)+H2O(g)═CO2(g)+H2(g) △H3=-41kJ•mol-1 平衡常数K3
新工艺的总反应式为3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)则该反应的△H=_____,化学平衡常数为K=__(用K1、K2、K3的代数式表示);
(2)一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.此反应在达到平衡时,A的转化率为__;

(3)研究减少有毒气体的排放对改善环境消除雾霾有十分重要的意义。利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)⇌5CO2(g)+I2(s) △H。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图。
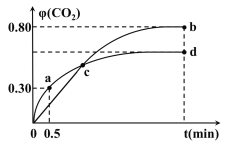
请回答:
①该反应属于__反应(填“放热”或“吸热“);
②从反应开始至a点时的反应速率为v(CO)=___,b点时化学平衡常数Kb=__;
③下列说法不正确的是____(填字母序号)。
a.容器内气体密度不变,表明反应达到平衡状态
b.两种温度下,c点时体系中混合气体的压强相等
c.增大d点的体系压强,CO的转化率不变
d.b点和d点的化学平衡常数:Kb<Kd
-
在密闭容器中,5 mol H2与2 mol CO2发生反应:3H2(g)+C O2(g)
O2(g)  CH3OH(g)+H2O(g)。反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示。下列说法错误的是( )
CH3OH(g)+H2O(g)。反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示。下列说法错误的是( )
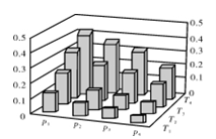
A.P1>P2>P3>P4
B.若T1> T2> T3>T4,则该反应为放热反应
C.甲醇的物质的量分数越高,反应的平衡常数越大
D.缩小容积,可以提高CH3OH在混合物中的质量分数
-
在恒容密闭容器中,反应CO2(g)+ 3H2 (g) CH3OH(g)+H2O(g) △H<0 达到平衡后,改变某条件,下列说法正确的是
CH3OH(g)+H2O(g) △H<0 达到平衡后,改变某条件,下列说法正确的是
A. 升高温度,正反应速率减小,逆反应速率增加,平衡逆向移动
B. 升高温度,可提高CO2转化率
C. 增加H2的浓度,可提高CO2转化率
D. 改用高效催化剂,可增大反应的平衡常数
-
甲醚是一种淸洁燃料,以 =2的比例将混合气体通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)
=2的比例将混合气体通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是
CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是

A. 上述反应△H<0
B. 图中P1<P2<P3
C. 若在P3和316℃时,测得容器中n(H2)=n(CH3OCH3),此时v(正)<v(逆)
D. 若在P3和316℃时,起始时 =3,则达到平衡时,CO转化率小于50%
=3,则达到平衡时,CO转化率小于50%
-
二甲醚(CH3OCH3)常作为甲基化试剂用于生产硫酸二甲酯,CO2催化加氢合成二甲醚的过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH2=-122.5kJ·mol-1
回答下列问题:
(1)2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=______,欲提高该反应中CH3OCH3(g)的平衡产率,理论上应采取的措施是______(填标号)。
A.低压高温 B.高压低温 C.高压高温 D.低压低温
(2)一定温度下,在恒容密闭器容中发生反应Ⅱ,下列能判断反应达到平衡状态的有______(填标号)。
A.v正(CO2)=2v逆(CH3OCH3)
B.气体的压强不再变化
C单位时间每消耗2molCO2,同时产生1molCH3OCH3
D.H2与H2O的物质的量之比为2:1
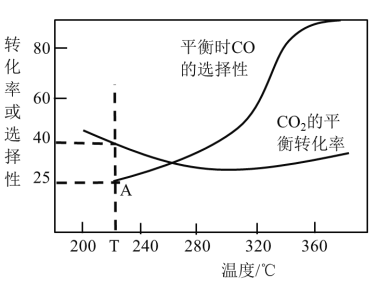
(3)在恒压、CO2和H2的起始量一定条件下,CO2平衡转化率和平衡时CO的选择性(CO的选择性=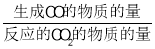 ×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
(4)一定温度下,向容积为2L的恒容密闭器容中充入CO(g)和H2O(g),发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)。CO和H2O的平衡转化率(a)与起始充入的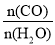 的关系如图所示:
的关系如图所示:
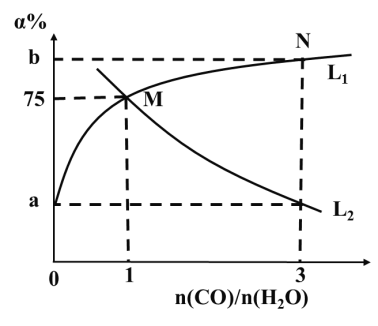
①a:b=______。
②图中表示CO变化趋势的曲线为______(填“L1”或“L2”);该温度下,反应的平衡常数K=______。
 (CH3)2O(g)+CO2(g)达平衡时CO的平衡转化率与温度和压强的关系如图所示(假定过程中不发生其他反应)。温度为T时,向体积为1 L的恒容密闭容器中充入0.4 mol CO和0.4 mol H2,反应达平衡时测得CO2物质的量为0.1 mol。下列说法正确的是( )
(CH3)2O(g)+CO2(g)达平衡时CO的平衡转化率与温度和压强的关系如图所示(假定过程中不发生其他反应)。温度为T时,向体积为1 L的恒容密闭容器中充入0.4 mol CO和0.4 mol H2,反应达平衡时测得CO2物质的量为0.1 mol。下列说法正确的是( )




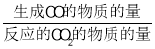 ×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
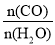 的关系如图所示:
的关系如图所示: