-
下表是元素周期表的一部分,请用元素符号或化学式回答有关问题:

(1)⑧的单质是有毒气体, 它能与强碱稀溶液反应,其离子方程式为_________,③和⑤构成的具有漂白性的化合物,其电子式为______________。
(2)表中能形成两性氧化物的元素是____, 写出该元素的单质与⑩的最高价氧化物的水化物反应的离子方程式__________。
(3)④⑤⑦⑩四种元素简单离子半径由大到小的顺序是_____________。
(4)上述元素的最高价氧化物对应的水化物酸性最强的是______(填写化学式), 非金属气态氢化物还原性最强的是_______(填写化学式)。
-
A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为
红棕色。有关的转化关系如下图所示(反应条件均已略去)。
请回答下列问题:

(1)D的化学式为 ;
(2)反应③的离子方程式为 。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为 。
(4)0.1mol/L的X溶液和0.1mol/L的Y溶液等体积混合,溶液呈________性;(填“酸”、“碱”或“中”)原因是: __________________________________
(用离子方程式说明)
(5)常温下0.1mol/L的Y溶液中c(H+)/c(OH-)=1×10-8,下列叙述正确的是( )
A.该溶液的pH=11;
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol/L的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH值为9;
-
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍。G单质是日常生活中用量最大的金属,易被腐蚀。
试回答下列问题:
(1)A元素的同位素有___________(写原子符号)
(2)实验室制取B的简单氢化物的化学反应方程式为_________________________
(3)C、D、E、F的简单离子半径由大到小的顺序是_________________(用离子符号表示)
(4)用化学事实说名E与F这两种元素非金属性的强弱_____________________(举一例)
(5)下列有关G的说法不正确的是_______
A、铁位于第四周期ⅧB族,在人体内的血红蛋白中含有铁元素
B、过量的铁分别与氯气和稀盐酸反应所得氯化物相同
C、FeCl3、FeCl2、Fe(OH)3都可以通过化合反应制取
D、氢氧化铁与HI溶液仅发生中和反应
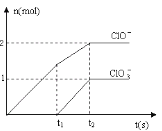
(6)向NaOH溶液中通入一定量的F单质,两者恰好完全反应,生成物中有三种含F的离子,其中两种离子的物质的量与反应时间的曲线如图所示。请写出t2时反应的总的化学方程式________。
-
下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置。试回答下列问题:
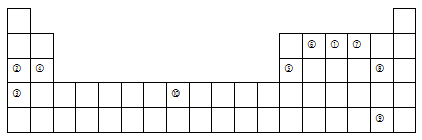
(1)写出表中⑥含有8个中子的原子的化学符号 ,元素⑦的氢化物与⑧的单质反应的离子方程式为 。
(2)元素⑩的核外电子排布式 。
(3) 根据元素周期表来比较④和Cs的金属性,要通过另一种元素作中介或桥梁进行比较, 这种元素是 (填元素符号)。
(4)据报道,美国科学家卡尔·克里斯特于1998年11月根据①合成了一种名为“N5”的物质,由于其极强的爆炸性,又称“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片的电子式为:__________________。
-
现有部分短周期元素的性质或原子结构如表:
| T | 地壳中含量最多的元素 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下,单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | M层比K层少1个电子 |
| W | 其离子是第三周期金属元素的离子中半径最小的 |
根据上述信息进行判断,并回答下列问题:
(1)元素W在元素周期表中的位置是第_____周期第_____族。
(2)元素X的一种同位素可测定文物的年代,这种同位素的符号是________。
(3)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式_____,如何检验某溶液中含该离子_____。
(4)元素Z与元素W相比,金属性较强的是_____(用元素符号表示),下列表述中能证明这一事实的是_____(填字母序号)。
A.Z单质的熔点比W单质的低
B.Z 的化合价比W的低
C.常温下Z单质与水反应的程度很剧烈,而W单质在加热条件下才能与水反应
D.Z最高价氧化物对应的水化物的碱性比 W 的强
(5)由上述元素中的X、Y、Z组成的某剧毒化合物XYZ不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为______。
-
表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:

(1)①的元素符号为______;⑨的原子结构示意图为___________。
(2)第三周期主族元素中,离子半径最小的是____________(用离子符号表示)。
(3)写出⑦最高价氧化物对应水化物的电离方程式:__________。
(4)①②⑧三种元素的最高价氧化物的水化物中酸性最强的是_______ (用化学式表示)。
(5)⑤⑥两种元素相比较,金属性较强的是_______(填元素名称),可以验证这一结论的实验是_____ (填字母)。
A.将在空气中放置已久的这两种元素的块状单质分别放入NaOH溶液中,比较反应的剧烈程度
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应,比较反应的剧烈程度
C.将形状、大小相同的这两种元素的单质分别和热水作用,并滴入酚酞试液,比较反应的剧烈程度
-
(12分,每空3分)已知A为金属单质,C为一种强碱。它们有以下相互转化。试回答:

(1)写出B的化学式 ,D的化学式 。
(2)写出由D转变成H的化学方程式 。
(3)写出向G溶液加入A的有关离子反应方程式 。
-
(10分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
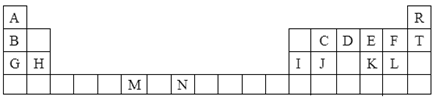
试回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式 。
(2)D的气态氢化物的VSEPR模型为 _ ,其中心原子的杂化类型为__ _ _ _ _ 。
(3)G、H和I的第一电离能数值由大到小的顺序为: (用元素符号作答)。
(4)由A、C、D形成的ACD分子中,含有 个σ键, 个π键。
(5)要证明太阳上是否含有R 元素,可采用的方法是 。
(6)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___________(填元素符号)
②MO=Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是__________(填“极性”或“非极性”)分子。
③在C2H4、CH3Cl、CH2O、CS2、CCl4五种有机化合物中,碳原子采取sp2杂化的分子有___________(填分子式)。
-
(共11分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
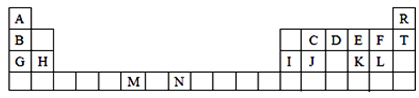
试回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式 。
(2)D的气态氢化物的VSEPR模型为 ,其中心原子的杂化类型为 。
(3)G、H和I的第一电离能数值由大到小的顺序为: (用元素符号作答)。
(4)由A、C、D形成的ACD分子中,含有 个σ键, 个π键。
(5)N晶体的堆积模型是 。
(6)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___(填元素符号;
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是__________(填“极性”或“非极性”)分子;
③在C2H4、CH3Cl、CH2O、CCl4四种化合物中,碳原子采取sp2杂化的分子有_____(填分子式)。
-
图表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
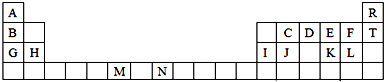
试回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式________.
(2)D的气态氢化物的VSEPR模型为________,其中心原子的杂化类型为________.
(3)G、H和I的第一电离能数值由大到小的顺序为:________(用元素符号作答).
(4)由A、C、D形成的ACD分子中,含有________个σ键,________个π键.
(5)要证明太阳上是否含有R 元素,可采用的方法是________.
(6)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应.请回答下列问题:
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有________(填元素符号)
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是________(填“极性”或“非极性”)分子.
③在C2H4、CH3Cl、CH2O、CS2、CCl4五种有机化合物中,碳原子采取sp2杂化的分子有________(填分子式).








