-
工业上制石英玻璃和光导纤维的重要原料是 ( )
A.Al2O3 B.MgO C.SiO2 D.Si
高二化学选择题简单题查看答案及解析
-
硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(含2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
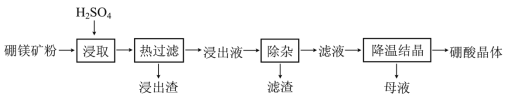
已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0 g、8.7 g、14.8 g、40.2g。Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4。
(1)“浸取”时主要反应的化学方程式为_____________________。
(2)“浸取”后,采用“热过滤”的目的是___________________________。
(3)“浸出液”显酸性,含H3BO3和Mg2+、SO42-,还含有其他杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是__________。H2O2的作用是______(用离子方程式表示)。
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4•H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是_____________。
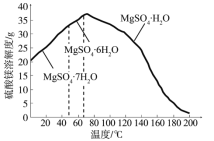
A. 升温结晶 B. 降温结晶 C. 加压升温结晶 D. 降压降温结晶
(5)在实际生产中为了提高原料的综合利用率,可以利用除杂后滤渣作为提炼铝的原料,工艺流程为:
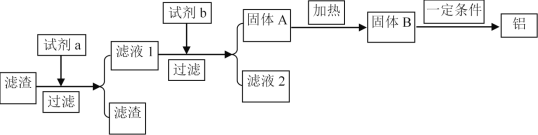
试剂a可选用________(化学式)溶液,若试剂b为AlCl3则由滤液得固体A的离子反应方程式为___________,在实际工业生产中,流程中的一定条件指的是________。
高二化学工业流程中等难度题查看答案及解析
-
下列说法错误的是
A. 工业上利用蛋白质的水解反应产生肥皂和甘油
B. Al2O3、MgO可用作耐高温材料,二氧化硅是生产光纤制品的基本原料
C. 从石油中获得乙烯是工业生产乙烯的主要途径
D. 淀粉和纤维素都是天然高分子化合物,且水解的最终产物相同
高二化学选择题简单题查看答案及解析
-
半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)+2C(s)===Si(s)+2CO(g) ΔH=+682.44 kJ·mol-1,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)===SiCl4(g) ΔH=-657.01 kJ·mol-1
(粗硅)
③SiCl4(g)+2Mg(s)===2MgCl2(s)+Si(s) ΔH=-625.63 kJ·mol-1
(纯硅)
用石英砂生产1.00 kg纯硅的总放热为
A.2.43×104 kJ B.2.35×104 kJ C.2.23×104 kJ D.2.14×104 kJ
高二化学选择题困难题查看答案及解析
-
化学与生活、生产密切相关。下列叙述正确的是
A.酯在碱性条件下的水解反应叫皂化反应
B.橡胶、合成塑料、合成纤维均是人工合成的高分子材料
C.通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2
D.《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐
高二化学单选题简单题查看答案及解析
-
化学与生产、生活、社会密切相关.下列有关说法中,正确的是( )
A. 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
B. SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆
C. 鼓励汽车、家电“以旧换新”,可减少环境污染,发展循环经济,促进节能减排
D. 焰火“脚印”、“笑脸”,使北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”的知识相关,焰色反应是化学变化
高二化学单选题简单题查看答案及解析
-
化学与生产、生活、社会密切相关。下列有关说法中不正确的是
A.侯氏制碱法的工艺过程中应用了物质溶解度的差异
B.SiO2制成的玻璃纤维,可用于制造通讯光缆
C.明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
D.闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺
高二化学选择题简单题查看答案及解析
-
下列叙述,正确的是( )
A. SiO2制成的玻璃纤维,由于导电能力强而被用于制造光缆
B. 浓硫酸可用于干燥H2、H2S等气体,但不能干燥NH3。
C. SO2和Cl2通入品红溶液,品红均褪色,说明两者的漂白原理相同
D. 分别将充满NH3、HCl气体的烧瓶倒置于水中后液面均迅速上升,说明NH3和HCl气体均易溶于水。
高二化学选择题中等难度题查看答案及解析
-
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
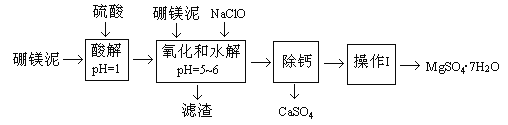
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有_________。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有_________。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式_________。在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为________________。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法_________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃)
40
50
60
70
MgSO4
30.9
33.4
35.6
36.9
CaSO4
0.210
0.207
0.201
0.193
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤_________、_________。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为_________。
高二化学工业流程困难题查看答案及解析
-
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
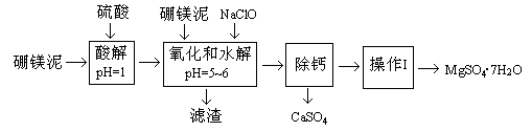
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有 。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式 。
在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃)
40
50
60
70
MgSO4
30.9
33.4
35.6
36.9
CaSO4
0.210
0.207
0.201
0.193
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 、 。
高二化学实验题困难题查看答案及解析