-
半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)+2C(s)===Si(s)+2CO(g) ΔH=+682.44 kJ·mol-1,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)===SiCl4(g) ΔH=-657.01 kJ·mol-1
(粗硅)
③SiCl4(g)+2Mg(s)===2MgCl2(s)+Si(s) ΔH=-625.63 kJ·mol-1
(纯硅)
用石英砂生产1.00 kg纯硅的总放热为
A.2.43×104 kJ B.2.35×104 kJ C.2.23×104 kJ D.2.14×104 kJ
高二化学选择题困难题查看答案及解析
-
半导体工业用石英砂做原料通过下面三个重要反应生产单质硅:

用石英砂生产1.00 kg纯硅,放出的总热量约为( )
A.2.43×104KJ B.2.35×104 kJ C.2.23×104 kJ D.2.14×104 kJ
高二化学选择题中等难度题查看答案及解析
-
制备硅单质时,化学反应如下:(1)SiO2+2C==== Si+2CO↑ (2)Si+2Cl2 ===SiCl4 (3)SiCl4+2H2 ===Si+4HCl。下列对上述三个反应的叙述中,不正确的是:( )
A.(1)(3)为置换反应 B.(1)(2)(3)均为氧化还原反应
C.(2)为化合反应 D.三个反应的反应物中硅元素均被还原
高二化学选择题简单题查看答案及解析
-
关于硅及其化合物的叙述中,不正确的是
A. 硅是良好的半导体材料
B. 制备普通水泥的原料是纯碱、石灰石、石英
C. 可以用焦炭还原二氧化硅生产硅:SiO2+2C
Si+2CO↑
D. HF刻蚀玻璃的反应原理是:SiO2+4HF=SiF4↑+2H2O
高二化学单选题简单题查看答案及解析
-
(6分)工业上利用硅的氧化物制取硅单质,主要反应为:SiO2 + 2C
Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了1 mol C,则生成 mol Si。
高二化学填空题中等难度题查看答案及解析
-
(原创)工业上以沙子为原料制取粗硅,主要反应的化学方程式为2C(s) + SiO2(s) =Si (s) + 2CO(g) △H > 0,对该反应的说法中不正确的是
A.△S>0
B.产物CO 为酸性氧化物
C.高温条件下才能自发进行
D.采用碎沙而非石块的原因可能是加快反应速率
高二化学选择题简单题查看答案及解析
-
工业上粗硅的生产原理为2C+SiO2
Si+2CO↑,下列说法正确的是
A.SiO2是氧化剂 B.SiO2发生氧化反应
C.C表现出氧化性 D.C被还原
高二化学选择题简单题查看答案及解析
-
工业上粗硅的生产原理为2C+SiO2
Si+2CO↑,下列说法正确的是( )
A. C表现出氧化性 B. SiO2发生氧化反应
C. SiO2是氧化剂 D. C被还原
高二化学单选题简单题查看答案及解析
-
工业上制石英玻璃和光导纤维的重要原料是 ( )
A.Al2O3 B.MgO C.SiO2 D.Si
高二化学选择题简单题查看答案及解析
-
硅是人类文明发展的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)工业生产粗硅的反应有:SiO2+2C
Si(粗)+2CO↑,SiO2+3C
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
(2)工业上可以通过如下图所示的流程制取纯硅:
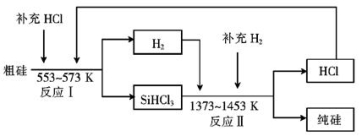
①若反应I为 Si(粗)+3HCl
 SiHCl3+H2,则反应II的化学方程式为 。
SiHCl3+H2,则反应II的化学方程式为 。②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另 一种物质,写出该反应的化学方程式: 。
③设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
高二化学填空题困难题查看答案及解析