合成氨反应在推动人类社会发展中发挥了重要作用。下列有关说法正确的是( )
A.3 mol H2与1 molN2混合反应生成NH3,转移电子的数目为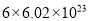
B.反应3H2(g)+N2(g) 2NH3(g)在较高温度下能自发进行,该反应的△H<0
2NH3(g)在较高温度下能自发进行,该反应的△H<0
C.一定条件下反应3H2(g)+N2(g) 2NH3(g)达到平衡时,v正(H2)=v逆(N2)
2NH3(g)达到平衡时,v正(H2)=v逆(N2)
D.反应3H2(g)+N2(g) 2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
高二化学单选题中等难度题
合成氨反应在推动人类社会发展中发挥了重要作用。下列有关说法正确的是( )
A.3 mol H2与1 molN2混合反应生成NH3,转移电子的数目为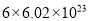
B.反应3H2(g)+N2(g) 2NH3(g)在较高温度下能自发进行,该反应的△H<0
2NH3(g)在较高温度下能自发进行,该反应的△H<0
C.一定条件下反应3H2(g)+N2(g) 2NH3(g)达到平衡时,v正(H2)=v逆(N2)
2NH3(g)达到平衡时,v正(H2)=v逆(N2)
D.反应3H2(g)+N2(g) 2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
高二化学单选题中等难度题
合成氨反应在推动人类社会发展中发挥了重要作用。下列有关说法正确的是( )
A.3 mol H2与1 molN2混合反应生成NH3,转移电子的数目为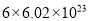
B.反应3H2(g)+N2(g) 2NH3(g)在较高温度下能自发进行,该反应的△H<0
2NH3(g)在较高温度下能自发进行,该反应的△H<0
C.一定条件下反应3H2(g)+N2(g) 2NH3(g)达到平衡时,v正(H2)=v逆(N2)
2NH3(g)达到平衡时,v正(H2)=v逆(N2)
D.反应3H2(g)+N2(g) 2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
2NH3(g)的△H可通过下式估算:△H=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和
高二化学单选题中等难度题查看答案及解析
化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )
A.利用废弃的秸秆生产生物质燃料乙醇
B.医疗上用含乙醇的浓度为75%的酒精消毒
C.利用基本的化学原料生产化学合成药物
D.利用蒸馏法从石油中分离出汽油
高二化学单选题简单题查看答案及解析
化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )
A.利用废弃的秸秆生产生物质燃料乙醇
B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
高二化学单选题简单题查看答案及解析
设NA为阿伏加德罗常数的值,下列说法不正确的是
A.一定条件下,合成氨反应中有0.5molN2发生反应,则反应中转移电子数为3NA
B.10克环己烷与2-丙醇的混合液中,碳元素的质量分数为72%,则其中所含的氧原子数目为NA
C.12g石墨中含有3NA个C-C共价键
D.常温常压下有28g单晶硅晶体,则其中所含的Si﹣Si键数目为2NA
高二化学单选题中等难度题查看答案及解析
用NA表示阿伏加德罗常数的数值,下列说法正确的是
A.一定条件下,1 molN2与足量的氢气反应合成氨,转移的电子数为6 NA
B.常温常压下,4.6 g的NO2和N2O4混合物中,含原子总数为0.3NA
C.1.0L 1.0 mol/LH2SO3水溶液中含有的氢离子数为2NA
D.1.0L PH=13的氢氧化钡溶液中(常温)OH-的数目为0.2NA
高二化学选择题中等难度题查看答案及解析
设NA为阿伏加德罗常数的数值。下列有关叙述正确的是
A. 16g由O2和O3组成的混合气体中的氧原子数为2NA
B. 1molN2与足量H2充分反应生成NH3的分子数为2NA
C. 1mol Fe溶于过量稀硝酸,转移的电子数为3NA
D. 标准状况下,2.24L苯中含有的原子数为1.2NA
高二化学选择题中等难度题查看答案及解析
.(21分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号)________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应的活化能降低,加快反应速率
d.活化分子间所发生的碰撞为有效碰撞
e.降低温度, V正、V逆均减小且V正减小的倍数小于V逆减小的倍数。
f.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡影响规律知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是________(填字母)。
a.容器内的密度保持不变
b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3)
d.混合气体中 c(NH3)不变
e.容器内混合气体的平均摩尔质量保持不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)_____________。
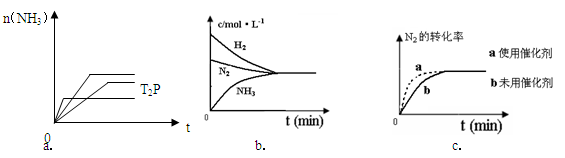
(5)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1mol N2和3 molH2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a_____b(填>、=、<), Q1_____ Q2(填>、=、<), Q1_____92.4(填>、=、<)。
高二化学填空题简单题查看答案及解析
[s1] 合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号)________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是(填字母)。
a.容器内的密度保持不变 b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3) d.混合气体中 c(NH3)不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)_____________。
|
|
|
|
|
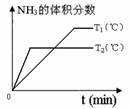
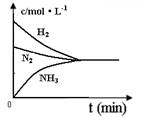
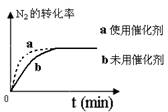
a. b. c.
(5)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1mol N2和3 molH2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;
B中NH3的体积分数为b,放出热量Q2 kJ。则:
a_____b(填>、=、<), Q1_____ Q2(填>、=、<), Q1_____92.4(填>、=、<)。
[s1]24.
高二化学填空题中等难度题查看答案及解析
(12分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号)________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是________(填字母)。
a.容器内的密度保持不变 b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3) d.混合气体中 c(NH3)不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)_____________。
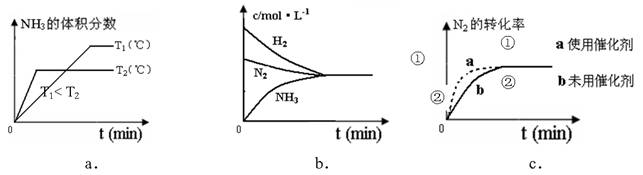
(5)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1mol N2和3 molH2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;
B中NH3的体积分数为b,放出热量Q2 kJ。则:a_____b(填>、=、<), Q1_____ Q2(填>、=、<), Q1_____92.4(填>、=、<)。
高二化学填空题简单题查看答案及解析
合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号)________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是_________________(填字母)。
a.容器内的密度保持不变 b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3) d.混合气体中 c(NH3)不变
高二化学填空题简单题查看答案及解析