-
石膏是一种节能建筑材料。某石膏样品是由二水石膏(CaSO4·2H2O)、半水石膏(CaSO4· H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
①称取8.70 g该石膏试样,在400℃干燥失去全部结晶水,质量变为8.16 g。
②再称取8.70 g的该石膏试样,加入80%的酒精溶液,使CaSO4完全水化成CaSO4· H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
③在②中所得8.97 g试样中加入蒸馏水,使全部的CaSO4· H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
(1)试样中结晶水的质量分数为__________________(用小数表示)。
(2)试样中无水石膏(CaSO4)的物质的量为____________ mol。
(3)试样中三种石膏的物质的量之比为:
n(CaSO4·2H2O)∶n(CaSO4· H2O)∶n(CaSO4)= __________________。
H2O)∶n(CaSO4)= __________________。
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。
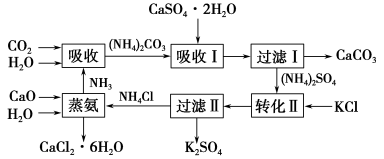
(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要__________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式: ______________________。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有____________(填化学式)等物质,该固体可用作生产水泥的原料。
(4)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是__________。
a.熔点较低(29 ℃熔化) b.能导电
c.能制冷 d.无毒
(5)上述工艺流程中体现的绿色化学理念是____________________________
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。

(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:______________________________________________________________。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有________(填化学式)等物质,该固体可用作生产水泥的原料。
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液。检验滤液中含有CO32-的方法是:_______________________________________________________________。
(5)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
| 温度/℃ | 0 | 20 | 60 |
| K2SO4溶解的量/g | 7.4 | 11.1 | 18.2 |
60 ℃时K2SO4的饱和溶液591 g冷却到0 ℃,可析出K2SO4晶体________g。
(6)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________。
a.熔点较低(29 ℃熔化) b.能导电
c.能制冷 d.无毒
(7)上述工艺流程中体现绿色化学理念的是:________________________________________________________________。
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下在石膏转化为硫酸钾和氯化钙的工艺流程示意图。
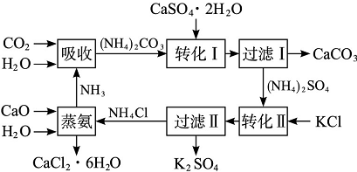
(1)本工艺中所用的原料除CaSO4·2H2O外,还需要____________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:__________________。
(3)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液。检验滤液中含有CO32—的方法是:_______________。
(4)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________。
a.熔点较低(29 ℃熔化) b.能导电 c.易溶于水 d.无毒
(5)上述工艺流程中体现绿色化学理念的是_________________________。
-
(10分)(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4·2H2O)可以降低土壤的碱性。试用化学方程式表示用石膏降低土壤碱性的反应原理________。
(2)习惯上把电解饱和食盐水的工业生产叫做氯碱工业,用化学方程式表示电解饱和食盐水的总反应为________________________。
(3)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是_____________。(填写化学式,只填一种即可)
(4)通过火法冶金炼出的铜是粗铜,不适于电器及其他许多工业使用,必须进行电解精炼。电解时,用________作阴极,________作阳极。
-
化学与生活生产密切相关。下列说法中不正确的是
A. 施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用
B. 夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率
C. 施用适量石膏(CaSO4·2H2O)可降低盐碱地(含较多NaCl、Na2CO3)的碱性
D. 将海水直接电解可获得 Mg及Cl2等单质
-
化学与生活生产密切相关。下列说法中不正确的是
A.施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用
B.夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率
C.施用适量石膏(CaSO4·2H2O)可降低盐碱地(含较多NaCl、Na2CO3)的碱性
D.将海水直接电解可获得 Mg及Cl2等单质
-
为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成分SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8)。设计简要流程如图:

(1)烟道气中SO2与废碱生成沉淀的化学方程式为_____;操作a的名称是_____。
(2)生成CaSO4•2H2O过程中没有涉及到的化学反应类型为_____(填序号)。
A.复分解反应 B.化合反应 C.分解反应 D.氧化反应 E.置换反应
(3)溶液Ⅰ通入空气发生反应的化学方程式为_____。
(4)用惰性电极电解时,阳极生成Na2S2O8的电极反应为_____;在整个流程中可以循环利用的物质是H2O和_____(填化学式)。
(5)一定条件下将S8(s)、O2(g)、NaOH(s)转化过程中的能量关系用如图简单表示。则S8(s)燃烧的热化学反应方程式为_____。
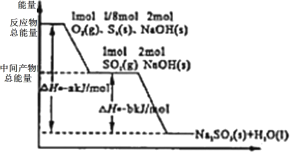
(6)若制取ag Na2S2O8时,阳极有bL氧气(标况)产生。则电解生成的H2体积在标准状况下为_____L。
-
常温下,Ksp(CaS04)=9×l0-6,常温下CaS04在水中的沉淀溶解平衡曲线如图。下列说法正确的是
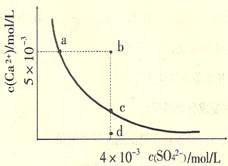
A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42-)对应曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
-
常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图.下列判断错误的是( )
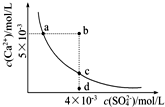
A.a、c两点均可以表示常温下CaS04溶于水所形成的饱和溶液
B.a点对应的Ksp不等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L
D.向d点溶液中加入适量CaCl2固体可以变到c点
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O)∶n(CaSO4)= __________________。






