-
已知在容积为10L固定的密闭容器中充入4molNH3和5molO2发生如下反应:4NH3(g)+5O2(g)  4NO(g)+6H2O(g),5s后,达到平衡并生成1molNO时:
4NO(g)+6H2O(g),5s后,达到平衡并生成1molNO时:
(1)O2的转化率为__________________。
(2)下列能说明该反应已经达到平衡状态的是____________。(填字母选项)
A.容器中气体总质量不变 B.c(O2)不变
C.5v(O2)正 = 4v(NO)逆 D.体系压强不变
(3)降低容器的温度则反应速率______,向该容器中通入Ar,则反应速率_______(选填“增大”、“减小”、“不变”)。
(4)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因是________。(填字母选项)。
A.反应体系温度先升高后降低,所以反应速率是先增大后减小
B.反应物浓度先升高后降低,所以反应速率先增大后减小
C.该反应为放热反应,在反应开始阶段,主要受体系温度升高的影响,反应速率增大;在反应后阶段,主要受浓度减小因素的影响,反应速率减慢
(5)已知对于可逆化学反应mA + nB  pC + qD在一定温度下达到化学平衡时,其平衡常数K的表达式为:
pC + qD在一定温度下达到化学平衡时,其平衡常数K的表达式为: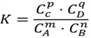 (其中,C为各物质的平衡浓度),则该温度下,上述反应的平衡常数K = ___________________________(用数据表达,列出式子即可)。
(其中,C为各物质的平衡浓度),则该温度下,上述反应的平衡常数K = ___________________________(用数据表达,列出式子即可)。
-
一定条件下体积不变的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
A. 4molNH3和5molO2反应,达到平衡时放出的热量为905.9kJ
B. 平衡时V正(O2)=4/5V逆(NO)
C. 适当增大氧气的浓度可以提高氨气的转化率
D. 降低压强,正反应速率减小,逆反应速率增大
-
(10分)已知在容积固定的密闭容器中充入NH3和O2发生如下反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
(1)下列能说明该反应已经达到平衡状态的是 ;
A.容器中气体总质量不变
B.c(O2)不变
C.υ(O2)=1.25υ(NH3)
D.体系压强不变
E.相同时间内,消耗0.1 mol NH3,同时消耗了0.1 mol NO
(2)向该容器中加入正催化剂,则反应速率 (选填“增大”、“减小”、“不变”,下同),降低容器的温度则反应速率 ,通入Ar,则反应速率 。
(3)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因是 。
A.反应体系温度先升高后降低,所以反应速率是先增大后减小
B.反应物浓度先升高后降低,所以反应速率先增大后减小
C.该反应为放热反应,在反应开始阶段,主要受体系温度升高的影响,反应速率增大;在反应后阶段,主要受浓度减小因素的影响,反应速率减慢
-
在一定条件下,将4molNH3和4molO2混合于固定容积为2L的密闭容器中,发生反应:4NH3(g)+5O2(g)=4X(g)+6H2O(g)。2min后该反应达到平衡,生成3molH2O。则:
(1)X的化学式为___。
(2)O2的转化率为___(O2转化率=已反应的O2的量/O2的总量×100%)。
(3)0~2min内,v(NH3)=___mol·L-1·min-1。
(4)燃料电池是一种高效、环境友好型发电装置。一种燃料电池的电解质溶液为NaOH溶液,负极通入NH3,正极通入空气,产物对环境无污染,则负极的电极反应式为___,电路中每通过1mol电子,消耗标准状况下的空气___(假设空气中O2的含量为20%)L。
-
已知在容积固定的密闭容器中充入NH3和O2发生如下反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
(1)下列能说明该反应已经达到平衡状态的是________;
A.容器中气体总质量不变
B.c(O2)不变
C.υ(O2)=1.25υ(NH3)
D.体系压强不变
E.相同时间内,消耗0.1 mol NH3,同时消耗了0.1 mol NO
(2)向该容器中加入正催化剂,则反应速率________(选填“增大”、“减小”、“不变”,下同),降低容器的温度则反应速率________,通入Ar,则反应速率________。
(3)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因是________。
A.反应体系温度先升高后降低,所以反应速率是先增大后减小
B.反应物浓度先升高后降低,所以反应速率先增大后减小
C.该反应为放热反应,在反应开始阶段,主要受体系温度升高的影响,反应速率增大;在反应后阶段,主要受浓度减小因素的影响,反应速率减慢
-
一定温度下,在一定容积的密闭容器中加入 NH3 和 O2 各 1mol,发生反应: 4NH3(g)+ 5O2(g)  4NO(g) +6H2O(g)。 下列说法中,表明该反应达到化学平衡状态的是
4NO(g) +6H2O(g)。 下列说法中,表明该反应达到化学平衡状态的是
A.气体的密度不再变化
B.NH3 和 NO 的反应速率相等
C.反应速率不再变化
D.NO 和 H2O 浓度比不再变化
-
一定温度下,在一定容积的密闭容器中加入 NH3 和 O2 各 1mol,发生反应: 4NH3(g)+ 5O2(g)  4NO(g) +6H2O(g)。 下列说法中,表明该反应达到化学平衡状态的是
4NO(g) +6H2O(g)。 下列说法中,表明该反应达到化学平衡状态的是
A.气体的密度不再变化
B.NH3 和 NO 的反应速率相等
C.反应速率不再变化
D.NO 和 H2O 浓度比不再变化
-
一定温度下,在一定容积的密闭容器中加入NH3和O2各1mol,发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
A. 反应速率不再变化 B. NH3和NO的反应速率相等
C. 气体的密度不再变化 D. NO和H2O浓度比不再变化
-
反应4NH3(g)+5O2(g) == 4NO(g)+6H2O,在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率 (x)(反应物的消耗速率或产物的生成速率)可表示为
(x)(反应物的消耗速率或产物的生成速率)可表示为
A、 (NH
(NH )=0.010mol·L-1·s-1 B、
)=0.010mol·L-1·s-1 B、 (O
(O )=0.0010 mol·L-1·s-1
)=0.0010 mol·L-1·s-1
C、 (NO)=0.0010 mol·L-1·s-1 D、
(NO)=0.0010 mol·L-1·s-1 D、 (H
(H O)=0.045 mol·L-1·s-1
O)=0.045 mol·L-1·s-1
-
反应4NH3(气)+5O2(气)= 4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为
A.v(NH3)=0.010mol/(L·s) B.v(O2)=0.0010mol/(L·s)
C.v(NO)=0.0010mol/(L·s) D.v(H2O)=0.0045mol/(L·s)
4NO(g)+6H2O(g),5s后,达到平衡并生成1molNO时:
pC + qD在一定温度下达到化学平衡时,其平衡常数K的表达式为:
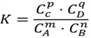 (其中,C为各物质的平衡浓度),则该温度下,上述反应的平衡常数K = ___________________________(用数据表达,列出式子即可)。
(其中,C为各物质的平衡浓度),则该温度下,上述反应的平衡常数K = ___________________________(用数据表达,列出式子即可)。