-
现有三个体积相同的密闭容器,按下图所示投料,并在T℃条件下开始反应,其中容器I保持恒压100kPa。已知:分压=总压×物质的量分数,对于2NO2(g) N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是
N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是
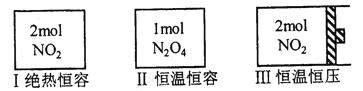
A. 达平衡时,容器Ⅱ中N2O4转化率小于50%
B. 达平衡时,容器Ⅰ中N2O4分压比容器Ⅲ中的大
C. 达平衡时,容器Ⅰ中N2O4的体积分数比容器Ⅱ中的大
D. 若起始时向容器Ⅲ中充入2molN2O4、2molNO2,达到平衡前v(正)<v(逆)
-
一定条件下存在反应:2SO2(g)+ O2 (g) 2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是

A.容器I、Ⅲ中平衡常数相同
B.容器II、Ⅲ中正反应速率相同
C.容器Ⅱ、中的反应达平衡时, SO3的体积分数:II > III
D.容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
-
在相同温度和体积均为1L的三个密闭容器中,保持温度和容积不变,以三种不同的投料方式进行反应,平衡时有关数据如下[已知相同条件下2SO2(g)+O2(g)⇌2SO3(g) △H=-196kJ/mol],下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 起始投入量 | 2molSO2和1molO2 | 2molSO3 | 2molSO2和2molO2 |
| 反应放出或吸收的 热量(kJ) | Q1 | Q2 | Q3 |
| 平衡时SO3的物质的量 | n1 | n2 | n3 |
| 平衡转化率 | α1 | α2 | α3 |
| 平衡时压强 | p1 | p2 | p3 |
A.Q1=Q2>Q3 B.n2>n1>n3 C.α1+α2=1 D.p1>p2>p3
-
在相同温度和体积均为1L的四个密闭容器中,保持温度和容积不变,以四种不同的投料进行反应。平衡时有关数据如下
(已知相同条件下:2SO2+O2 2SO3 △H =-196.6kJ/mol)。
2SO3 △H =-196.6kJ/mol)。
| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始投入量 | 2molSO2+1molO2 | 1molSO2+0.5molO2 | 2molSO3 | 2molSO2+2molO2 |
| 反应放出或 吸收的热量(kJ) | a | b | c | d |
| 平衡时c(SO3)(mol/L) | e | f | g | h |
下列关系正确的是
A. a=c;e=g B. a>2b;e>2f C. a>d;e>h D. c+98.3e=196.6
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同): N2(g)+3H2(g) 2NH3(g) △H<0,相关数据如下表所示:
2NH3(g) △H<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | lmol N2、3molH2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol/L | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol/(L·min) | v甲 | v乙 | v丙 |
下列说法正确的是
A. V甲> V丙 B. K乙>K丙 C. c乙>c甲 D. V甲= V丙
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g) 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
| 反应物的转化率 | a甲 | a乙 | a丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时AB3的反应速率/mol·L-1·min-1 | V甲 | v乙 | v丙 |
下列说法正确的是( )
A. K乙<K丙 B. c乙=c丙 C. a甲 +a乙<1 D. v甲=v丙
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A.V甲>V丙 B.K乙<K丙 C.c乙>c甲 D.v甲=v丙
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A.V甲>V丙 B.K乙>K丙 C.c乙>c甲 D.v甲=v丙
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g) 2NH3(g) △H<0相关数据如下表所示下列说法正确的是
2NH3(g) △H<0相关数据如下表所示下列说法正确的是
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1molN2、3mol的H2 | 2mol的NH3 | 2mol的NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应平衡常数K=c2(NH3)/c(N2)∙c3(H2) | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度(mol/L) | C甲 | C乙 | C丙 |
| 平衡时NH3的反应速率(mol/L∙min) | v甲 | v乙 | v丙 |
A.V甲>V乙 B.K乙>K丙 C.c乙>c甲 D.υ甲=υ丙
-
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始浓度和起始容积相同,一定条件下发生反应: 。相关数据如表所示:下列说法正确的是( )
。相关数据如表所示:下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料n |  、 、
| 
| 
|
| 平衡时容器体积 | 
| 
| 
|
| 反应的平衡常数K | 
| 
| 
|
| 平衡时 的浓度 的浓度 | 
| 
| 
|
| 平衡时 的反应速率 的反应速率 | 
| 
| 
|
A. B.
B. C.
C. D.
D.
N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是

