-
(10分)许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同条件下发生的还原反应如下:
①酸性:MnO4-+5e-+8H+→Mn2++4H2O;
②中性:MnO4-+3e-+2H2O→MnO2+4OH-
③碱性:MnO4-+e-→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e-→Mn2++2H2O
(1)MnO2与稀盐酸不能制取氯气,其原因是___________________________________。
(2)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是_______。(选填编号)
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(3)写出将SO2通入KMnO4溶液中所发生反应的离子方程式,并配平:
________________________________________________________________________。
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,已知产物中K2SO4和S的物质的量之比为3∶2。完成并配平该反应的化学方程式:
□KMnO4+□K2S+□__________→□K2MnO4+□K2SO4+□S↓+□__________,反应若生成5.44 g硫单质,反应过程中转移电子的物质的量为__________________。
高二化学填空题困难题查看答案及解析
-
高锰酸钾在不同的条件下发生的反应如下:
① MnO4-+5e-+8H+=Mn2++4H2O ②MnO4-+3e-+2H2O=MnO2↓+4OH-
(1)从上述两个反应中可以看出高锰酸根离子被还原的产物受溶液的 影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 → .
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法不正确的是 。
A.氧化性,PbO2>KMnO4 B.还原性:PbO2>KMnO4 C.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比 为3 : 2,完成下列化学方程式(横线上填系数,括号内填物质):
① KMnO4+ K2S+ ( ) = K2MnO4 + K2SO4+ S↓+ ( )。
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 。
高二化学填空题困难题查看答案及解析
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+-Mn2++CO2↑+H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
组别
10%硫酸体积/mL
温度/℃
其他物质
A
2mL
20
B
2mL
20
10滴饱和MnSO4溶液
C
2mL
30
D
1mL
20
V1 mL蒸馏水
E
0.5mL
20
V2 mL蒸馏水
(1)完成上述实验方案设计,其中:V1= ______ ,V2= ______ ;
(2)如果研究温度对化学反应速率的影响,使用实验 ______ 和 ______ .
(3)甲同学在做A组实验时,发现反应开始时速率较慢,随后加快.他分析认为高锰酸钾与 草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,你猜想还可能是 ______ ;
Ⅱ.乙同学利用如图测定反应速率
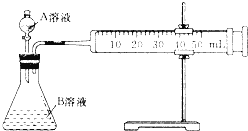
回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ______ ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 ______ 仪来记录数据.
高二化学简答题中等难度题查看答案及解析
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+-Mn2++CO2↑+H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
组别
10%硫酸体积/mL
温度/℃
其他物质
A
2mL
20
B
2mL
20
10滴饱和MnSO4溶液
C
2mL
30
D
1mL
20
V1 mL蒸馏水
E
0.5mL
20
V2 mL蒸馏水
(1)完成上述实验方案设计,其中:V1= ______ ,V2= ______ ;
(2)如果研究温度对化学反应速率的影响,使用实验 ______ 和 ______ .
(3)甲同学在做A组实验时,发现反应开始时速率较慢,随后加快.他分析认为高锰酸钾与 草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,你猜想还可能是 ______ ;
Ⅱ.乙同学利用如图测定反应速率
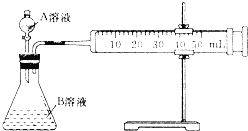
回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ______ ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 ______ 仪来记录数据.
高二化学综合题中等难度题查看答案及解析
-
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:
关于茉莉醛的下列叙述错误的是
A.在加热和催化剂作用下,能被氢气还原
B.能被高锰酸钾酸性溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与氢溴酸发生加成反应
高二化学选择题中等难度题查看答案及解析
-
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:

关于茉莉醛的下列叙述错误的是
A. 在加热和催化剂作用下,能被氢气还原
B. 能被高锰酸钾酸性溶液氧化
C. 在一定条件下能与溴发生取代反应
D. 不能与氢溴酸发生加成反应
高二化学单选题中等难度题查看答案及解析
-
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:
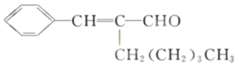
关于茉莉醛的下列叙述错误的是
A. 在加热和催化剂作用下,能被氢气还原
B. 能被高锰酸钾酸性溶液氧化
C. 在一定条件下能与溴发生取代反应
D. 不能与氢溴酸发生加成反应
高二化学单选题中等难度题查看答案及解析
-
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:

关于茉莉醛的下列叙述错误的是 ( )
A.在加热和催化剂作用下,能被氢气还原
B.能被酸性高锰酸钾溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与氢溴酸发生加成反应
高二化学选择题简单题查看答案及解析
-
(4分)加碘食盐中加入的碘酸钾是一种白色结晶粉末,其溶解度受温度影响很大,且随温度的升高而逐渐增大,常温下很稳定,在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物等还原性物质发生反应。
(1)为检验某食盐中是否含有KIO3,某同学取食盐样品完全溶解于水中,然后加入用盐酸酸化的淀粉KI溶液,结果溶液呈蓝色,则反应的离子方程式为________;
(2)KIO3也可用电解的方法制得,其原理是以石墨为阳极,以不锈钢为阴极,在一定温度和电流下电解KI溶液。总反应方程式为KI+3H2O=KIO3+3H2↑,则两极的电极反应式分别为:阴极________,阳极________
高二化学填空题简单题查看答案及解析
-
加碘食盐中加入的碘酸钾是一种白色结晶粉末,其溶解度受温度影响很大,且随温度的升高而逐渐增大,常温下很稳定,在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物等还原性物质发生反应.
(1)为检验某食盐中是否含有KIO3,某同学取食盐样品完全溶解于水中,然后加入用盐酸酸化的淀粉KI溶液,结果溶液呈蓝色,则反应的离子方程式为______;
(2)KIO3也可用电解的方法制得,其原理是以石墨为阳极,以不锈钢为阴极,在一定温度和电流下电解KI溶液.总反应方程式为KI+3H2O=KIO3+3H2↑,则两极的电极反应式分别为:阴极______,阳极______.高二化学解答题中等难度题查看答案及解析