-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+-Mn2++CO2↑+H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| A | 2mL | 20 | |
| B | 2mL | 20 | 10滴饱和MnSO4溶液 |
| C | 2mL | 30 | |
| D | 1mL | 20 | V1 mL蒸馏水 |
| E | 0.5mL | 20 | V2 mL蒸馏水 |
(1)完成上述实验方案设计,其中:V1= ______ ,V2= ______ ;
(2)如果研究温度对化学反应速率的影响,使用实验 ______ 和 ______ .
(3)甲同学在做A组实验时,发现反应开始时速率较慢,随后加快.他分析认为高锰酸钾与 草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,你猜想还可能是 ______ ;
Ⅱ.乙同学利用如图测定反应速率
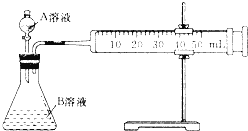
回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ______ ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 ______ 仪来记录数据.
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+-Mn2++CO2↑+H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| A | 2mL | 20 | |
| B | 2mL | 20 | 10滴饱和MnSO4溶液 |
| C | 2mL | 30 | |
| D | 1mL | 20 | V1 mL蒸馏水 |
| E | 0.5mL | 20 | V2 mL蒸馏水 |
(1)完成上述实验方案设计,其中:V1= ______ ,V2= ______ ;
(2)如果研究温度对化学反应速率的影响,使用实验 ______ 和 ______ .
(3)甲同学在做A组实验时,发现反应开始时速率较慢,随后加快.他分析认为高锰酸钾与 草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,你猜想还可能是 ______ ;
Ⅱ.乙同学利用如图测定反应速率
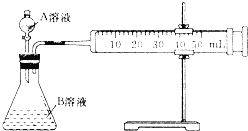
回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ______ ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 ______ 仪来记录数据.
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4—+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
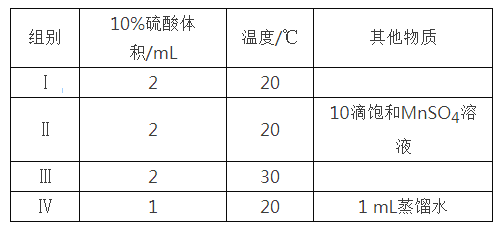
(1)写出该反应的离子方程式______________________,该反应中每生成1molCO2 转移电子数为________ 。
(2)如果研究催化剂对化学反应速率的影响,使用实验_______和________(用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验________和_________。
(3)对比实验I和IV,可以研究________对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是______________________。
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO +H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)
用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如表所示:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为______________________。
(2)如果研究催化剂对化学反应速率的影响,使用实验____________和________(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验________和________。
(3)对比实验Ⅰ和Ⅳ,可以研究____________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是______________________________________________________________。
-
(10分)草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO4- + H2C2O4 + H+ — Mn2+ + CO2↑+ H2O(未配平)
现用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| I | 2 mL | 20 | |
| II | 2 mL | 20 | 10滴饱和MnSO4溶液 |
| III | 2 mL | 30 | |
| IV | 1 mL | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为 。
(2)如果研究催化剂对化学反应速率的影响,使用实验 和 (用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(3)对比实验I和IV,可以研究________对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是 。
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H 2C2O4+H+--Mn2++CO2↑+H2O(未配平) 用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H 2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2mL | 20 | |
| Ⅱ | 2mL | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2mL | 30 | |
| Ⅳ | 1mL | 20 | 1mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,使用实验________ 和________(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验________和________.
(2)对比实验Ⅰ和Ⅳ,可以研究________对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是________.
-
已知草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。
(1)草酸的电离方程式为 。
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+ H2C2O4+ → Mn2+ + CO2↑+ H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是 。
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
| 组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
| 1 | 30 | 10 | 10 | 20 | 40 |
| 2 | 30 | 20 | 20 | 0 | t |
| 3 | 30 | | | 15 | |
①对比实验1和3要研究改变反应物浓度对化学反应速率的影响,请完成表格中横线。
②实验2中溶液褪色时间t 为
A.>40 B.=40 C.<40 D.无法判断
-
配平下列反应方程式:
(1)酸性KMnO4溶液能合H2C2O4(草酸)溶液褪色,反应离子方程式为:
____MnO4-+___H2C2O4+___H+=___Mn2++___CO2↑+___H2O
(2)淀粉碘化钾溶液在酸性环境中过一段时间后会褪色,反应离子方程式为:
___I-+___O2+___H+═___I2+___H2O
-
草酸溶液能使酸性KMnO4溶液褪色,其离子方程式为:
MnO4-+H2C2O4+H+→CO2↑+Mn2++__(未配平)。关于此反应的叙述正确的是
A.该反应的还原产物是CO2
B.该反应右框内的产物是OH-
C.配平该反应后,H+计量数是6
D.1molMnO4-在反应中失去5mol电子
-
已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化: MnO4-+C2O42-+H+→Mn2++CO2↑+H2O(未配平) MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
⑴配平:________MnO4-+________C2O42-+________H+―________Mn2++________CO2↑+________H2O
⑵0.0200mol·L-1KMnO4标准溶液应置于________(选填“甲”或“乙”)滴定管中;判断滴定终点的依据是;
⑶你能否帮助该研究小组求得软锰矿中MnO2的质量分数________(选填“能”或“否”)。若回答“能”,请给出计算结果;若回答“否”,试说明原因________;
⑷若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是________。
A.滴定前尖嘴部分有一气泡,滴定终点时消失;B.溶液转移至容量瓶中,未将烧杯、玻棒洗涤;C.滴定前仰视读数,滴定后俯视读数;D.定容时,俯视刻度线;E.锥形瓶水洗之后未用待测液润洗。


