-
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,对二氧化硫的排放有了大大的改善。已知SO2可以用Fe( NO3)3溶液吸收, 0.1mol/L的Fe(NO3)3 溶液的pH=2。某学习小组据此展开如下相关探究:
【探究I】铜与浓硫酸的反应探究:
(l)取12.8g铜片于三颈烧瓶中,通N2一段时间后再加入20 mL 18 mol•L-1的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀,充分反应后,烧瓶中仍有铜片剩余。
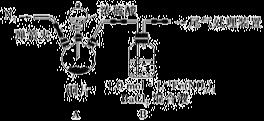
①该小组同学认为烧瓶中除有铜片剩余外还应有较多的硫酸剩余,其原因是: ___________________ 。
②该小组同学欲通过测定产生气体的量来求余酸的物质的量,设计了多种实验方案。下列方案不可行的是______ 。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量硫酸酸化的高锰酸钾溶液后,再加入足量的BaCl2溶液,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
【探究II】装置B中产生沉淀的原因探究:
(2)加入浓硫酸之前先通N2一段时间,其目的是____ 。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列猜想(不考虑各因素的叠加):
猜想1: 装置A中的白雾进入B参与反应
猜想2:SO2被Fe3+氧化为SO42-
猜想3: 。
(4)甲同学认为只要在装置A、B间增加洗气瓶C,就可以排除装置A中白雾影响,则C中盛放的试剂是 。
(5)乙同学取出少量装置B中清液,加入几滴酸性高锰酸钾,发现紫红色褪去,据此认为猜想2成立。你是否同意其结论?并说明理由: 。
【思考与交流】
(6)实验结束后,若使烧瓶中铜片继续溶解,下列方案(必要时可加热)可行的是 。
A.打开弹簧夹,通入O2 B.由分液漏斗加入H2O2溶液
C.由分液漏斗加入NaNO3溶液 D.由分液漏斗加入Na2SO4溶液
-
太原市自2016年11月1日零时起,将汽车用油全部更换为”国V标准”车用燃料,进而 改善太原市空气质量。下列物质中,不会造成空气污染的是

A. NO B. SO2 C. CO2 D. 粉尘
-
太原市自2016年11月1日零时起,将汽车用油全部更换为”国V标准”车用燃料,进而 改善太原市空气质量。下列物质中,不会造成空气污染的是

A. NO B. SO2 C. CO2 D. 粉尘
-
2016年年底,中国石油全部完成国V标准车用汽柴油质量升级,以减少空气污染。下列物质中,不会造成空气污染的是
A. NO B. CO2 C. SO2 D. 粉尘
-
车用乙醇汽油是把乙醇和汽油按一定比例混合形成的一种新型汽车燃料,经多项检测结果表明,它不但不影响汽车的行驶性能,而且还可以减少有害气体的排放量,在美国、巴西等国早已推广使用。下列有关乙醇汽油的说法正确的是
A.乙醇汽油是一种纯净物
B.乙醇汽油作燃料不会产生碳的氧化物等有害气体,其优点是可以减小环境的污染
C.乙醇和汽油都作溶剂,也可相互溶解
D.乙醇和乙二醇( )互为同系物
)互为同系物
-
2001年5月,中国宣布将推广“车用乙醇汽油”,乙醇汽油就是在汽油里加入适量乙醇混合而成的一种燃料。下列叙述错误的是
A. 乙醇汽油是一种新型的化合物
B. 汽车使用乙醇汽油能减小有害气体的排放
C. 工业常用裂化的方法提高汽油的产量
D. 用玉米、高梁发酵可以制得乙醇
-
乙醇汽油是普通汽油与燃料乙醇调和而成的,它可以有效改善油的性能和质量,除低CO、碳氢化合物等主要污染物的排放。乙醇的燃烧热是1366.8 kJmol-1。燃烧1 mol这种乙醇汽油生成液态水,放出的热量为Q kJ。测得该汽油中乙醇与汽油的物质的量之比为1:9。有关普通汽油(CxHy)燃烧的热化学方程式正确的是 A.CxHy(l)+(x+y/4)O2(g)=xCO2(g)+y/2H2O(l) ΔH=(-Q+1366.8) kJmol-1
B.CxHy(l)+(x+y/4)O2=xCO2(g)+y/2H2O(l) ΔH=-9Q/10 kJmol-1
C.CxHy(l)+(x+y/4)O2(g)=xCO2(g)+y/2H2O(l) ΔH=-9Q/110 kJmol-1
D.CxHy(l)+(x+y/4)O2(g)=xCO2(g)+y/2H2O(l)ΔH=(-10Q/9+151.9) kJmol-1
-
SO2和NO2是主要的大气污染物。下列措施不能有效防止大气污染的是( )
A. 将机动车尾气排放标准从国家Ⅱ号标准提高到国家Ⅲ号标准
B. 采用强氧化剂将SO2氧化为SO3再排放到大气中
C. 采用原煤脱硫技术,降低燃煤中硫的含量
D. 向燃煤中加入适量石灰石,减少燃烧产物中SO2的含量
-
(8分)接触法制硫酸排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前设法进行综合利用。某硫酸厂每天排放的1万米3(已换算成标准状况)尾气中含0.2%(体积百分数)的SO2。
(1)若用生石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克生石膏?
(2)若用氨水处理,最少需要标况下的氨气多少升?最多需要标准状况下的氨气多少升?
-
当前粮食价格的不断上涨与前几年许多国家大力推广粮食生产车用乙醇汽油存在一定的联系,车用乙醇汽油是由乙醇与汽油按一定比例混合而成的。下列说法中不正确的是
A.汽油是以石油为原料加工而成的
B.乙醇可以由粮食中的淀粉转化而成
C.推广车用乙醇汽油可节省石油资源,减轻大气污染,改善大气环境
D.乙醇是一种不可再生能源


