-
室温下,有2种溶液0.01 mol·L-1 NH3·H2O和0.01 mol·L-1 NH4Cl,下列操作可以使2种溶液中c(NH4+)都增大的是( )
A. 通入少量HCl气体 B. 加入少量H2O
C. 加入少量NaOH固体 D. 升高温度
高一化学单选题中等难度题查看答案及解析
-
在室温下,下列五种溶液:①0.1mol/L NH4Cl②0.1mol/L CH3COONH4 ③0.1mol/LNH4HSO4④0.1mol/L NH3•H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3•H2O。
请根据要求填写下列空白:
(1)溶液①呈_____性(填“酸”、“碱”或“中”),其原因是________(用离子方程式表示)。
(2)比较②③溶液中,c(NH4+)的大小关系是②______③(填“>”“<”或“=”)。
(3)在溶液④中,_____ 离子的浓度为0.1mol/L;NH3•H2O和_____离子的物质的量浓度之和为0.2mol/L。
(4)室温下,测得溶液②的pH=7,则CH3COO-的水解程度_____(填“>”“<”或“=”)NH4+-的水解程度。CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)_____c(NH4+)(填“>”“<”或“=”)。
高一化学填空题中等难度题查看答案及解析
-
2008年5月我国汶川发生地震灾害,假若你是卫生防疫人员,为配制0.01 mol·L-1的KMnO4消毒液,下列操作导致所配溶液浓度偏大的是( )
A.未等溶液冷却至室温就转移到容量瓶中
B.定容时,仰视刻度线
C.溶解搅拌时有液体飞溅
D.容量瓶未干燥,有少量蒸馏水
高一化学选择题简单题查看答案及解析
-
2008年5月我国汶川发生地震灾害,假若你是卫生防疫人员,为配制0.01mol•L-1的KMnO4消毒液,下列操作导致所配溶液浓度偏大的是( )
A.未等溶液冷却至室温就转移到容量瓶中
B.定容时,仰视刻度线
C.溶解搅拌时有液体飞溅
D.容量瓶未干燥,有少量蒸馏水高一化学选择题中等难度题查看答案及解析
-
将浓度均为0.01 mol/L 的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
(资料)
该“碘钟实验”的总反应:H2O2 +2S2O32-+2H+=S4O62-+2H2O
反应分两步进行:
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:……
(1)反应B的离子方程式是______。对于总反应,I-的作用相当于______。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是______。
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ。(溶液浓度均为0.01 mol/L)
试剂
序号 用量(mL)
H2O2
溶液
H2SO4
溶液
Na2S2O3
溶液
KI溶液
(含淀粉)
H2O
实验Ⅱ
5
4
8
3
0
实验Ⅲ
5
2
x
y
z
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是30 min、实验Ⅲ是40 min。
①实验Ⅲ中,x、y、z所对应的数值分别是______。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是______。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。
(溶液浓度均为0.01 mol/L)
试剂
序号 用量(mL)
H2O2
溶液
H2SO4
溶液
Na2S2O3
溶液
KI溶液(含淀粉)
H2O
实验Ⅳ
4
4
9
3
0
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:_____________________。
高一化学实验题中等难度题查看答案及解析
-
将浓度均为0.01 mol/L 的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
(资料)
该“碘钟实验”的总反应:H2O2 +2S2O32-+2H+=S4O62-+2H2O
反应分两步进行:
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:……
(1)反应B的离子方程式是______。对于总反应,I-的作用相当于______。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是______。
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ。(溶液浓度均为0.01 mol/L)
试剂
序号 用量(mL)
H2O2
溶液
H2SO4
溶液
Na2S2O3
溶液
KI溶液
(含淀粉)
H2O
实验Ⅱ
5
4
8
3
0
实验Ⅲ
5
2
x
y
z
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是30 min、实验Ⅲ是40 min。
①实验Ⅲ中,x、y、z所对应的数值分别是______。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是______。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。
(溶液浓度均为0.01 mol/L)
试剂
序号 用量(mL)
H2O2
溶液
H2SO4
溶液
Na2S2O3
溶液
KI溶液(含淀粉)
H2O
实验Ⅳ
4
4
9
3
0
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:_____________________。
高一化学实验题中等难度题查看答案及解析
-
将浓度均为0.01 mol/L的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
(资料)该“碘钟实验”的总反应:H2O2+2S2O32-+2H+=S4O62-+2H2O
反应分两步进行:
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:……
(1)反应B的离子方程式是______。对于总反应,I-的作用相当于_____。
(2)为证明反应A、B的存在,进行实验Ⅰ。
A.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色
B.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是_____。
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ。(溶液浓度均为0.01 mol/L)
用量(mL)
试剂序号
H2O2溶液
H2SO4溶液
Na2S2O3溶液
KI溶液(含淀粉)
H2O
实验Ⅱ
5
4
8
3
0
实验Ⅲ
5
2
x
y
z
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是30 min、实验Ⅲ是40 min。
①实验Ⅲ中,x、y、z所对应的数值分别是_____、_____、_____。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是_____。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。(溶液浓度均为0.01 mol/L)
用量(mL)
试剂序号
H2O2溶液
H2SO4溶液
Na2S2O3溶液
KI溶液(含淀粉)
H2O
实验Ⅳ
4
4
9
3
0
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:______。
高一化学实验题中等难度题查看答案及解析
-
强酸和强碱稀溶液的中和热可表示为:H+(aq)+OH-(aq)===H2O(l);ΔH=-57.3kJ·mol-1。已知①HCl(aq)+NH3·H2O(aq)===NH4Cl(aq)+H2O(l);ΔH=-akJ·mol-1 ②HCl(aq)+NaOH(s)===NaCl(aq)+H2O(l);ΔH=-bkJ·mol-1 ③HNO3(aq)+KOH(aq)===KNO3(aq)+H2O(l);ΔH=-ckJ·mol-1则a、b、c三者的大小关系为( )
A. a>b>c B. b>c>a C. a=b=c D. 无法比较
高一化学选择题简单题查看答案及解析
-
强酸和强碱稀溶液的中和热可表示为:
H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ/mol
已知:①HCl(aq)+NH3·H2O(aq) =NH4Cl(aq)+H2O(l) ΔH =-a kJ/mol
②HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l) ΔH=-bkJ/mol
③Ba(OH)2(aq)+H2SO4(aq) = BaSO4(s)+2H2O(l) ΔH=-ckJ/mol
则a、b、c三者的大小关系判断错误的是
A. 2a=2b=c B. a<57.3 C. b>57.3 D. c>114.6
高一化学单选题中等难度题查看答案及解析
-
下列实验装置或操作与实验目的不相符的是
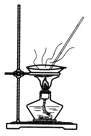


A.除去水中的泥沙
B.用Ca(OH)2和NH4Cl制取NH3
C.用自来水制取蒸馏水
D.配制100 mL0.1 mol·L−1 NaCl溶液
A. A B. B C. C D. D
高一化学单选题简单题查看答案及解析