-
某化学课外活动小组计划使用NaOH溶液制取简易消毒液,反应原理为:C12+2NaOH === NaC1O+NaCl+H2O。实验室里有已配制好的NaOH溶液,所贴标签为4.0 mol·L-1。
(1)这种溶液_____________mL才能与2.24 L氯气(STP)恰好完全反应。
(2)配制250 mL 4.0 mol·L-1NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量。
b.称量氢氧化钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容 量瓶。
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。
①所需称量的氢氧化钠固体的质量是_______________。
②上述步骤的正确操作顺序是____________________________。
③上述实验需要的仪器除烧杯、玻璃棒,托盘天平外,还需要____________、_______________。
高一化学实验题简单题查看答案及解析
-
已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O;3Cl2+6NaOH=5NaCl+NaC1O3+3H2O。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液。经测定ClO-与ClO3-的物质的量之比为4:1,则溶液中NaCl与NaClO的物质的量之比为( )
A. 9:4 B. 11:2 C. 5:1 D. l:l
高一化学选择题困难题查看答案及解析
-
(1)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
其反应原理为(用离子方程式表示): 。
(2)在实验室里用浓盐酸与高锰酸钾反应来制取少量的氯气,反应的化学方程式为:
2KMnO4+16HCl(浓) ═ 2KCl+ 2MnCl2+5Cl2↑+8H2O
反应物中,氧化剂是 ;化合价升高的元素是________。
反应中HCl的作用是 。
(3)某同学帮助水质检测站配制230 mL 0.1 mol·L-1 NaOH溶液以备使用:该同学应选用 (仪器名称)称取NaOH固体________g;
(4)取上述配制的NaOH溶液 mL才能与0.224 L氯气(STP)恰好完全反应。
高一化学填空题中等难度题查看答案及解析
-
某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
(1)其反应原理为:(用化学方程式表示)________________________________________。
(2)某同学帮助水质检测站配制500 mL0.4 mol.L-1 NaOH 溶液以备使用
①该同学应称取NaOH固体_______g
②配制该溶液时使用的仪器除托盘天平、药匙、烧杯、玻璃棒外,还必须用到的
仪器有____________、____________。
(3)实验时下图所示操作的先后顺序为 _____________________(填编号)。

(4)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积多少而变化的是____________(填选项字母)。
a.溶液中NaOH的物质的量 b.溶液的浓度
c.溶液中OH-的数目 d.溶液的密度
(5)下列操作中,会造成所配溶液浓度偏低的是_______(填选项字母)。
a.没有洗涤烧杯和玻璃棒 b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水 d.摇匀后发现液面低于刻度线,又滴加蒸馏水
高一化学实验题困难题查看答案及解析
-
某工厂制取漂白液的化学原理为:Cl2+2NaOH═NaCl+NaClO+H2O,在该反应中,氯元素没有呈现出的化合价是( )
A. +2 B. +1 C. 0 D. ﹣1
高一化学单选题简单题查看答案及解析
-
下列反应中,从金属钠价态角度考虑明显与其他选项不同的是()
A. 2NaOH + Cl2 = NaC1O+ NaCl+ H2O
B. 2Na+2H2O=2NaOH+H2↑
C. 2Na2O2+2H2O=4NaOH+O2↑(其中Na2O2中氧元素为负一价)
D. CO2 + NH3 + NaCl+ H2O= NaHCO3↓+NH4Cl
高一化学选择题中等难度题查看答案及解析
-
漂粉精是一种常用的消毒剂,工业上将氯气通入石灰乳[Ca(OH)2]制取漂粉精.
(1)写出工业上制取氯气的化学方程式:______ 2NaOH+H2↑+Cl2↑或2NaCl2Na+Cl2↑
高一化学解答题中等难度题查看答案及解析
-
流行性感冒期间,某同学将食盐溶解于水,通直流电电解(2NaCl+2H2O
2NaOH+H2↑+Cl2↑),并将生成的Cl2与NaOH溶液反应得消毒液.该消毒液的有效成分是
A.NaOH B.NaClO C.NaCl D.Cl2
高一化学选择题简单题查看答案及解析
-
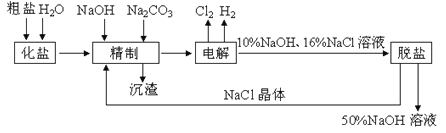
氯碱厂电解饱和食盐水制取NaOH的化学反应方程式为:2NaCl + H2O
2NaOH + H2↑+ Cl2↑,工艺流程示意图如下:
下表是NaCl和MaOH在水中的溶解度
温度
物质
0℃
20℃
40℃
60℃
80℃
100℃
NaCl
35.7g
36g
36.6g
37.3g
38.4g
39.8g
NaOH
42g
109g
129g
174g
314g
347g
依据示意图和表,完成下列填空:
(1)工业食盐中含CaCl2、MgCl2等杂质。除去Ca2+、Mg2+过程发生反应的化学反应方程式为_____。
(2)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是________(填字母序号)。
①Ba(NO3)2 ②BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_______(少选多选都不计分)。
A.先加NaOH,后加Na2CO3,再加钡试剂 B.先加Na2CO3,后加钡试剂,再加NaOH
C.先加钡试剂,后加NaOH,再加Na2CO3 D.先加NaOH,后加钡试剂,再加Na2CO3
(5)用制得的 NaOH固体配制 240 mL0.2mol/L NaOH 溶液。
①配制时,必須使用的玻璃仪器有______________________。
②某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。
烧杯的实际质量为________________g。
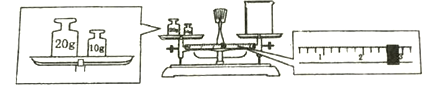
③在配制过程中,其他操作都是正确的,下列情况对所配制的NaOH珩液的浓度偏高有_____。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水
C.定容时俯视刻度线 D.定容时仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
④下图是该同学转移溶液的示意图,图中的错误是_____________。
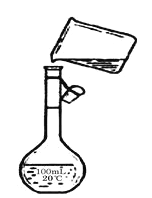
高一化学简答题困难题查看答案及解析
-
制取漂白液的化学方程式是:Cl2+2NaOH=NaCl+NaClO+H2O,该反应的氧化剂与还
原剂物质的量之比为
A.1:1 B.1:2 C. 2:1 D. 3:2
高一化学选择题中等难度题查看答案及解析