-
“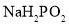 还原法”制备高纯度氢碘酸和亚磷酸钠
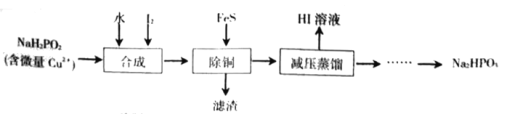
还原法”制备高纯度氢碘酸和亚磷酸钠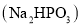 的工业流程如图。
的工业流程如图。
已知:ⅰ.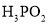 为一元弱酸
为一元弱酸
ⅱ.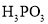 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: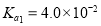 ,
,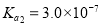
ⅲ.25℃时: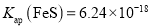 ,
,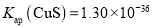
回答下列问题:
(1)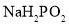 属于______(填“正盐”或“酸式盐”)。
属于______(填“正盐”或“酸式盐”)。
(2)“合成”过程,主要氧化产物为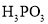 ,相应的化学方程式为______。
,相应的化学方程式为______。
(3)“除铜”过程发生的反应为 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数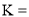 ______。
______。
(4)常温下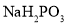 的
的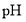 ______7(填“>”、“=”或“<”)。
______7(填“>”、“=”或“<”)。
(5)常温下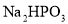 溶液呈碱性的原因为(用离子方程式表示)______。
溶液呈碱性的原因为(用离子方程式表示)______。
-
(1)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的pH= ,此酸的电离平衡常数K= ,由HA电离出的H+的浓度约为水电离出的H+的浓度的 倍。
(2)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶剂。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,向其中加入少量KOH溶液时,发生反应的离子方程式是 。
②现将0.04mol﹒L-1HA溶液和0.02mol﹒L-1NaOH溶液等体积混合,得到缓冲溶液。
a、若HA为HCN,该溶液显碱性,则溶液中c(Na+) c(CN-)(填“<”、“=”或“>”)。
b、若HA为CH3COOH,该溶液显酸性,溶液中所有的离子按浓度由大到小排列的顺序是 。
-
次磷酸(H3PO2)是一种具有强还原性的一元弱酸,工业上常利用H3PO2和AgNO3溶液反应进行化学镀银,已知该反应中氧化剂与还原剂的物质的量之比为4:1,则下列说法中不正确的是( )
A. H3PO2中磷元素的化合价为+1 B. H3PO2的电离方程式为H3PO2 H++H2PO2-
H++H2PO2-
C. H3PO2被AgNO3氧化成了H3PO4 D. NaH2PO2、NaH2PO4、Na2HPO4均为酸式盐
-
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度大于第二步电离程度,第二步电离程度远大于第三步电离程度…… 今有HA、H2B、H3C三种一元、二元、三元弱酸,根据“较强酸十较弱酸盐=较强酸盐十较弱酸”的反应规律,它们之间能发生下列反应:
①HA+HC2-(少量)=A-+H2C- ②H2B(少量)+2A- =B2-+2HA ③H2B(少量)+H2C-=HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是___________________。
(2)判断下列反应的离子方程式中正确的是(填写标号)____________。
A.H3C+3A-=3HA+C3- B.HB-+A-=HA+B- C.H3C+B2-=HB-+H2C-
(3)完成下列反应的离子方程式。
A.H3C+OH-(过量)_______________________;
B.HA(过量)+C3-__________________________。
-
六氟磷酸钠(NaPF6)极易溶于水,可溶于乙醇、丙酮等有机溶剂,可作高能钠电池的电解质。工业上以氟磷灰石[Ca5(PO4)3F]、NaCl为主要原料,制备六氟磷酸钠的工艺流程如下:
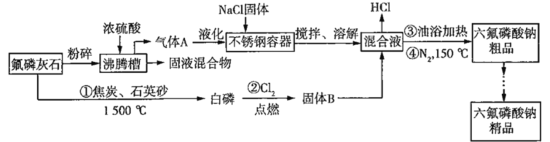
已知:HF的熔点为-83 ℃,沸点为19.5 ℃。回答下列问题:
(1)氟磷灰石粉碎的目的是_______________。
(2)HF液化时产生的二聚物(HF)2能发生微弱的电离,与NaCl反应生成NaHF2,请写出该二聚物的电离方程式:________。
(3)为避免废水NaH2PO4的污染,常在其中加入石灰,将磷元素全部转化成磷酸钙,进行回收利用。已知常温下Ksp[Ca3(PO4)2]=1.96×10-29,当处理后的废水c(Ca2+)=1.0×10-5 mol/L时,则溶液中c(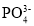 )=___________mol/L。
)=___________mol/L。
(4)操作③油浴加热目的是________。
(5)反应①中除生成白磷(P4)外,还产生SiF4和一种还原性气体,写出该反应的化学方程式:______。
(6)六氟磷酸钠粗品的提纯:将六氟磷酸钠粗品(杂质主要是微量铁盐)溶于一定量乙醇中,加入适量5%的NaOH甲醇溶液,使溶液保持碱性,离心将不溶杂质除去。通过______(填操作方法)将溶剂回收,减压条件下结晶,得到NaPF6·H2O,干燥得到无水盐。
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性,下列有关说法正确的是
A. H3PO2溶于水的电离方程式为:H3PO2  3H++PO23-
3H++PO23-
B. H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C. 将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的氧化产物为H3PO4
D. 用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2--4e-+2H2O=O2+6H++PO23-
-
(12分)已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
今有HA、H2B、H3C三种一元、二元、三元弱酸,
根据“较强酸 + 较弱酸盐 = 较强酸盐 + 较弱酸”的反应规律,它们之间能发生下列反应:
① HA + HC2-(少量)= A- + H2C-;
② H2B(少量)+2A- = B2- + 2HA;
③ H2B(少量)+ H2C- = HB- + H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是_________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_____,最难结合质子的是_____。
(3)完成下列反应的离子方程式
④ H3C + A-:_____________________;⑤ HB- + A-:______________________;
⑥ H3C + B2-:_____________________。
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.H3PO2溶于水的电离方程式为:H3PO2 3H++PO23-
3H++PO23-
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的氧化产物为H3PO4
D.用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2-4e-+2H2O =O2↑+4H+
-
磷是重要的元素,能形成多种含氧酸。回答下列问题:
(1)次磷酸(H3PO2)是一元酸,其电离常数的值K=9×103。向10mL0.1 mol•L-1H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液,写出反应的离子方程式_________,c(Na+)+(H2PO2-)+c(H3PO2)=______(忽略混合后溶波体积的变化)。
(2)亚磷酸(H3PO3)是二元弱酸, 25℃时亚磷酸的电离常数的值为K1=1×10-2、k2=2.6×10-7,则NaH2PO3溶液显性_____(填“酸”“碱”或“中”),原因是____(结合化学用语及数据计算进行解释)
(3)已知HF的电离常数的值为K=3.6×10-4,将足量HF溶液和Na2HPO3溶液反应,其离子方程式为______。
(4)亚磷酸具有强还原性。化学实验小组利用滴定法测定某亚磷酸溶液的浓度,取25.00mL的亚磷酸溶液放入锥形瓶中,用0.10 mol•L-1的高锰酸钾溶液进行滴定,反应的离子方程式是5H3PO3+ 2MnO4-+6H+ = 5H3PO4+ 2Mn2+ +3H2O。
三次滴定实验的数据分别如下:
| 实验编号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.50 | 22.50 |
| 2 | 1.50 | 24.50 |
| 3 | 1.00 | 22.00 |
①亚磷酸溶液的物质的量浓度为______。
②关于该实验下列说法正确的是______(填写序号)。
a 取亚磷酸溶液的滴定管,洗涤后未润洗,导致结果偏低
b 盛高锰酸钾溶液的滴定管滴定前有气泡,滴定后无气泡,导致结果偏高
c 滴定过程中眼睛只注视滴定管中液面变化,并做好记录
d 锥形瓶未干燥底部有水,会导致结果偏低
-
H2O2在工业、农业、医药上都有广泛的用途.
(1)H2O2是二元弱酸,写出第一步的电离方程式__,第二步的电离平衡常数表达式Ka2=_________.
(2)许多物质都可以做H2O2分解的催化剂.一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化).下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是________.
①I - ②Fe3+ ③Cu2+ ④Fe2+
(3)H2O2是一种环境友好的强氧化剂.电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+等)制备硫酸镍的一种流程如下:

①第(ⅰ)步,加入H2O2反应的离子方程式_________________.
②为测定NiSO4•nH2O的组成,进行如下实验:称取2.627g样品,配制成250.00mL溶液.准确量取配制的溶液25.00mL,用0.04000mol•L﹣1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2﹣=NiY2﹣+2H+),消耗EDTA标准溶液25.00mL.则硫酸镍晶体的化学式为__________________.
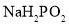 还原法”制备高纯度氢碘酸和亚磷酸钠
还原法”制备高纯度氢碘酸和亚磷酸钠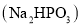 的工业流程如图。
的工业流程如图。
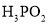 为一元弱酸
为一元弱酸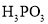 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: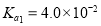 ,
,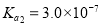
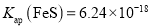 ,
,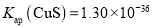
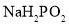 属于______(填“正盐”或“酸式盐”)。
属于______(填“正盐”或“酸式盐”)。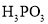 ,相应的化学方程式为______。
,相应的化学方程式为______。 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数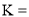 ______。
______。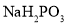 的
的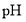 ______7(填“>”、“=”或“<”)。
______7(填“>”、“=”或“<”)。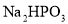 溶液呈碱性的原因为(用离子方程式表示)______。
溶液呈碱性的原因为(用离子方程式表示)______。
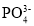 )=___________mol/L。
)=___________mol/L。