-
N2H4(联氨又称肼)一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________________。
(2)N2H4是火箭升空需要高能的燃料,工业上利用N2和H2可以合成联氨(N2H4)等。已知:
N2(g)+2O2(g)= N2O4 (l) △H=-19.5kJ·mol-1
2H2(g)+O2(g) =2H2O(g) △H =-483.6 kJ·mol-1
2N2H4(1) +N2O4(l)= 3N2(g)+4H2O(g) △H = -1048.9 kJ·mol-1
写出N2和H2合成液态联氨(N2H4)的热化学方程式______________________________。火箭升空经常用联氨和N2O4反应作为火箭推进剂,其主要原因为______________________________。
(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH--4e-═O2↑+2H2O,则阴极的电极反应式为___________________。有人提出,可以设计反应2CO= 2C+O2(△H >0)来消除CO的污染。请判断上述反应是否能自发进行并说明理由_____________________________。
高三化学综合题中等难度题查看答案及解析
-
N2H4(联氨又称肼)一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,它是一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)推测有关N2H4的性质,下列说法正确的是
A.具有高度吸湿性、可燃性
B.有微弱的氨味,与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯
C.N2H4的水溶液呈弱碱性,
D.联氨的水溶液既有氧化性又有还原性,酸性溶液以氧化性为主,还原产物是N2,碱性溶液以还原性为主,氧化产物是NH4+
E.高温加热时分解为氮气、氢气和氨气。
(2)请写出N2H5+的电子式:__________________________
(3)在高锰酸钾催化剂存在下,尿素(CO(NH2)2)和次氯酸钠-氢氧化钠溶液反应制得联氨,它和水能按任意比例互相混溶,形成稳定的水合肼N2H4·H2O写出反应的离子方程式:______________________
(4)发射卫星可用肼为燃料,用NO2作氧化剂,二者发生反应生成氮气和水蒸气。已知:
N2(g)+2O2(g)=2NO2 (g) H=+67.7kJ•mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1,
写出气态肼和NO2反应的热化学方程式__________。
(5)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,负极电极反应式是____________________________
高三化学填空题中等难度题查看答案及解析
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为 ,其中氮的化合价为 。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 。
(3)①2O2(g)+N2(g)==N2O4(l) △H1
②N2(g)+2H2(g)==N2H4(l) △H2
③O2(g)+2H2(g)==2H2O(g) △H3
④2N2H4(l)+N2O4(l)==3N2(g)+4H2O(g) △H4=-1048.9kJ-mol-1
上述反应热效应之间的关系式为△H4= ,联氨和N2O4可作为火箭推进剂的主要原因为 。
(4)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为 (已知:N2H4+H+
N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2S03处理水中溶解的O2相比,联氨的优点是 。
高三化学填空题简单题查看答案及解析
-
化学在生产和日常生活中有着重要的作用,下列有关说法不正确的是
A.硅酸钠的水溶液俗称水玻璃,可用作木材防火剂
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中
D.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水
高三化学选择题简单题查看答案及解析
-
化学在生产和日常生活中有着重要的作用,下列说法不正确的是
A. 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂
B. “地沟油”经过加工处理后,可以用来制肥皂
C. 用聚乙烯塑料代替聚乳酸塑料可减少白色污染
D. 利用粮食酿酒经过了淀粉
葡萄糖
乙醇的化学变化过程
高三化学选择题中等难度题查看答案及解析
-
化学在生产和日常生活中有着重要的作用,下列有关说法不正确的是( )
A.硅酸钠的水溶液俗称水玻璃,可用作木材防火剂
B.“地沟油”经过加工处理后,可以用来制肥皂
C.含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中
D.Fe2O3常用于生产红色油漆和涂料
高三化学选择题简单题查看答案及解析
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
(1)肼(N2H4)是一种良好的火箭燃料,拉希格法是制备肼的传统方法,该方法是在5℃条件下,NaClO与NH3反应生成NH2Cl与NaOH,然后在140℃左右的条件下,将上述反应后混合物与氨混合,反应生成肼。上述两步反应中,氧化产物是______________(写化学式)。
(2)机动车尾气已成为城市大气的主要污染源,机动车尾气中的主要有害物质为氮的氧化物。目前科技工作者正在探索用甲烷等燃料气体将氮氧化物还原为N2和水,涉及到的反应有:
CH4(g)+4NO2(g)
4NO(g)+CO2(g)+2H2O(g) ΔH1=−574 kJ·mol−1
CH4(g)+2NO2(g)
CO2(g)+2H2O(g)+N2(g) ΔH2=−867 kJ·mol−1
写出CH4还原NO生成N2的热化学方程式:____________________________。
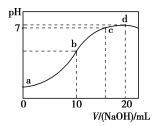
(3)变质的蔬菜类食物中含有亚硝酸盐,一定温度下,形成该盐的亚硝酸(HNO2)的电离常数Ka=4.0×10−4。在20 mL 0.01 mol·L−1的亚硝酸中逐滴滴加0.01 mol·L−1的NaOH溶液,测得混合液的pH变化如图,则图中a点的值为______,b点溶液呈酸性,其原因是__________________,d点溶液呈碱性,原因是______________________________。(已知lg2≈0.3)
(4)工业合成氨的反应原理为:N2(g)+ 3H2 (g)
2NH3(g) ΔH=a kJ·mol−1。保持反应体系的容积不变,在其中加入一定量的H2和N2,体系中各物质浓度随时间变化如图所示:
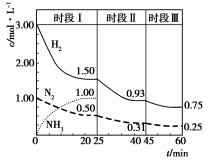
①若上述反应体系的容积为2 L,则0~20 min时间内,ν(H2)= ______________,该过程中放出的热量为94.4 kJ,则a=______________。
②25 min时将NH3从反应体系中完全分离出去,45 min时改变温度,在原图中画出25 min~60 min的NH3浓度变化曲线。
高三化学填空题中等难度题查看答案及解析
-
化学在生产和生活中有着重要的应用。下列叙述中,不正确的是
A.次氯酸钠溶液可用于杀菌消毒
B.推广使用燃煤脱硫技术,防治SO2污染环境
C.纯碱可用于生产普通玻璃,也可用来除去物品表面的油污
D.“辽宁舰”上用于舰载机降落拦阻索的是一种特种钢缆,属于新型无机非金属材料
高三化学选择题中等难度题查看答案及解析
-
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl
实验一: 制备NaClO溶液(实验装置如图所示)
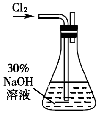
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有 (填标号)
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应化学程式是 。
(3)利用中和滴定反应原理测定反应后锥形瓶中混合溶液的NaOH的浓度。取一定量锥形瓶内混合溶液稀释一定倍数后,加入适量的H2O2溶液后,再滴加2-3滴甲基橙试液,用0.100mol/L盐酸滴定。需要加入H2O2除去ClO-的原因是 。
实验二: 制取水合肼。(实验装置如图所示)
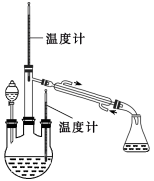
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108-114℃馏分(已知:N2H4·H2O易被NaClO氧化,高温易分解)
(4)分液漏斗中的溶液是 (填标号)。
A.CO (NH2) 2溶液 B.NaOH和NaClO混合溶液
选择的理由是 。
蒸馏时需要减压,原因是 。
实验三: 测定馏分中肼含量。
称取馏分5.000g,加入适量NaHCO3固体,加水配成1000mL溶液,移出10.00mL,用0.1000mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。
滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是能与在滴定过程中产生的 反应。
(6)实验测得消耗I2溶液的平均值为16.40mL,馏分中水合肼(N2H4·H2O)的质量分数为 。
高三化学实验题极难题查看答案及解析
-
硫代硫酸钠是一种重要的化工产品。某兴趣小组制备硫代硫酸钠晶体
的实验装置如下图所示(省略夹持装置):
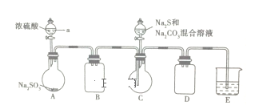
主要实验步骤为:①检查装置气密性,按图示加入试剂;②先向C中烧瓶加入
和
混合溶液,再向A中烧瓶滴加浓硫酸;③待
和
完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作后得到产品。
已知:i
是无色透明晶体,易溶于水,其稀溶液与
溶液混合无沉淀生成;ii向
和
混合溶液中通入
可制得
所得产品常含有少量
和
。
回答下列问题:
(1)仪器a的名称是____________;B、D装置的作用是_____________。
(2)上述实验步骤③中的操作主要有_______________、冷却结晶、过滤、洗涤、干燥;E中的试剂是_____________。
(3)为检验产品中是否含有
和
,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:
取适量产品配成稀溶液,滴加足量
溶液,有白色深沉生成,向沉淀中滴加足量的_________,若____________(填实验现象),则可以确定产品中含有
和
。
(4)为减少装置C中生成
的量,在不改变原有装置的基础上对实验步骤②需进行改进,具体操作是_________________;写出制备
的总反应的化学方程式:___________________________。
高三化学实验题中等难度题查看答案及解析