-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为 ,其中氮的化合价为 。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 。
(3)①2O2(g)+N2(g)==N2O4(l) △H1
②N2(g)+2H2(g)==N2H4(l) △H2
③O2(g)+2H2(g)==2H2O(g) △H3
④2N2H4(l)+N2O4(l)==3N2(g)+4H2O(g) △H4=-1048.9kJ-mol-1
上述反应热效应之间的关系式为△H4= ,联氨和N2O4可作为火箭推进剂的主要原因为 。
(4)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为 (已知:N2H4+H+ N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2S03处理水中溶解的O2相比,联氨的优点是 。
-
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为__________,其中氮的化合价为______。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的离子方程式____________。
(3)联氨和N2O4可作为火箭推进剂,其反应的产物均无污染。其氧化产物和还原产物之比为 _______。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为______________。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为_________,其中氮的化合价为__________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为______________。
(3)①2O2(g)+N2(g)= N2O4(l) △H1
②N2(g)+2H2(g)= N2H4(g) △H2
③O2(g)+ 2H2(g)=2H2O(g) △H3
④2 N2H4(g)+ N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=_________,联氮和N2O4可作为火箭推进剂的主要原因为__________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_________(已知:N2H4+H+=== N2H5+ 的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为______________。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加人联氨溶液,观察到的现象是_______________。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是_________。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________________(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是___________。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是___________。
-
氮的氢化物种类繁多,其中联氨(又称肼,N2H4,无色油状液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为__________________,其中氮的化合价为 _________。
(2) ①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________。
(3)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并且有气泡产生,写出该反应的化学方程式__________________。
(4)联氨还可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2_____kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是__________。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,HCN中C的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=_________,联氨和N2O4可作为火箭推进剂的主要原因为__________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨在水中第一步电离反应的平衡常数值为______________(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 _。联氨可用于处理高压锅炉水中的氧气,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 _。
-
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,HCN中C的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨在水中第一步电离反应的平衡常数值为___________________(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为__________________。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为__________________。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是______________________________。联氨可用于处理高压锅炉水中的氧气,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是_____________________________________________。
-
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________________(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
-
肼(分子式 N2H4,沸点 113.5℃)是一种良好的火箭燃料,是一种易溶 于水和醇类等有机溶剂的无色油状液体。在工业上有重要用途。实验室可用如下 装置(略去部分夹持装置)模拟利用氨气和次氯酸钠合成肼的过程。

(1)装置 A 可用来制备 Cl2,装置 B 中饱和食盐水的作用是_____,当合成肼的反应结束时关闭止水夹 K1,装置 B 可以观察到的实验现象_____。
(2)装置 C 中长玻璃导管 b 与装置 B 中的_____(填仪器名称)的作用相同。
(3)装置 E 中可用熟石灰和氯化铵制备 NH3,反应的化学方程式为_____
(4)当反应一段时间,关闭两个止水夹,打开装置 C 中分液漏斗的活塞,将溶液 全部滴入集气瓶中,反应生成肼。反应的离子方程式为_____。 有同学说装置 D 没有什么作用,若去掉装置 D,对实验是否有影响?请说明理由:___________。
(5)将足量的 Cl2 与含有 0.4mol NaOH 的水溶液反应,分液漏斗中液体全部滴入 C 中,并向 C 中通入标准状况下的 13.44L NH3,从 C 中蒸馏分离得到 3.6g 液态肼, 则该实验中肼的实验产率为___。
-
肼是一种应用广泛的化工原料,又称联氨。具有很高的燃烧热,可用作火箭和燃料电池的燃料。肼是一种强还原剂,易被氧化生成氮气,可用来去除锅炉水和热水加热系统中的氧,以减少腐蚀。储存时应与氧化剂,食用化学品分开存放,切忌混储。工业采用尿素[CO(NH2)2]为原料,与次氯酸钠氢-氢氧化钠溶液反应制得肼。某学习小组的同学设计以下实验制备肼:
(1)按照图18甲所示的装置完成实验一:将生成的气体通入到盛有____的锥形瓶中,瓶中发生反应的离子方程式是_________________。
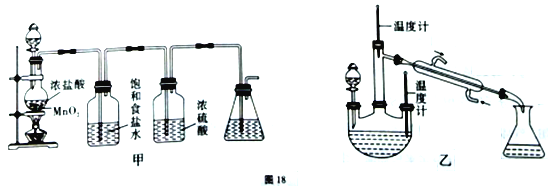
(2)按照图乙所示的装置进行实验二: 将实验一制得的溶液注入____中(填仪器名称),控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中充分反应,这样操作的理由是_________。加热蒸馏三颈烧瓶内的溶液,收集108~114℃的馏分。
(3)N2H4(肼)可作制药的原料,也可作火箭的燃料。肼能与酸反应,已知N2H6Cl2溶液呈弱酸性。在水中存在如下反应:
a.N2H62++H2O N2H5++H3O+ 平衡常数为K1
N2H5++H3O+ 平衡常数为K1
b.N2H5++H2O N2H4+H3O+ 平衡常数为K2
N2H4+H3O+ 平衡常数为K2
相同温度下,K1>K2,其主要原因有两个:
第一: 电荷因素,N2H5+的水解程度小于N2H62+;
第二:________________。
(4)气态肼在催化剂作用下分解只产生两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝。在密闭容器中发生上述反应,平衡体系中肼的体积分数与温度关系如图19所示:
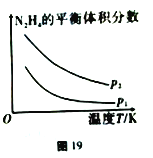
①p1_____p2(填“<”“>”或“=”,后同),该反应的△H____0。
②肼还可以制备肼—碱性燃料电池,氧化产物为稳定的对环境友好的物质。该电池负极的电极反应式为______________。
N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。


