-
(6分)红磷(P)和白磷(P4)均为磷的同素异形体。已知:
P4 ( 白s ) + 5O2 ( g ) = P4O10 ( s ) △H = -2983.2 kJ/mol
P (红 s ) + 5/4O2 ( g ) = 1/4P4O10 ( s ) △H = -738.5 kJ/mol
写出白磷转化为红磷的热化学方程式 ,由此可知,红磷比白磷 。(填“稳定”或“不稳定”)
高二化学填空题中等难度题查看答案及解析
-
(1)已知:P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ/mol
P(红磷,s)+5/4O2(g)=1/4 P4O10(s) ΔH=-738.5kJ/mol
则白磷转化为红磷的热化学方程式为 ;由此说明红磷的稳定性比白磷 。
(2)明矾[KAl(SO4)2·12H2O]水溶液呈 (填“酸”、“碱”或“中”)性;明矾还能净水,用离子方程式解释其原因为 。
(3)电解池的能量转化形式为 ,原电池反应 (填“一定”或“不一定”)自发。
(4)pH=3的盐酸和pH=3的醋酸溶液各稀释至其体积的100倍,稀释后盐酸的pH (填“大于”、“小于”或“等于”)醋酸的pH;常温时pH=x的盐酸和pH=y的NaOH溶液以1︰10的体积比混合,反应后溶液恰好呈中性,则x、y满足的关系是 。
高二化学填空题中等难度题查看答案及解析
-
(1)已知:P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ/mol
P(红磷,s)+5/4O2(g)=1/4 P4O10(s) ΔH=-738.5kJ/mol
则白磷转化为红磷的热化学方程式为________;由此说明红磷的稳定性比白磷________。
(2)明矾[KAl(SO4)2·12H2O]水溶液呈________(填“酸”、“碱”或“中”)性;明矾还能净水,用离子方程式解释其原因为________。
(3)电解池的能量转化形式为________,原电池反应________(填“一定”或“不一定”)自发。
(4)pH=3的盐酸和pH=3的醋酸溶液各稀释至其体积的100倍,稀释后盐酸的pH________(填“大于”、“小于”或“等于”)醋酸的pH;常温时pH=x的盐酸和pH=y的NaOH溶液以1︰10的体积比混合,反应后溶液恰好呈中性,则x、y满足的关系是________。
高二化学填空题中等难度题查看答案及解析
-
红磷(P)和白磷(P4)均为磷的同素异形体。已知:
P4(s)+5O2(g)=P4O10(s) △H=-2983.2kJ/mol
P(s)+5/4O2(g)=1/4P4O10(s) △H=-738.5kJ/mol
写出白磷转化为红磷的热化学方程式_____________,由此可知,红磷比白磷___________。(填“稳定”或“不稳定”)
高二化学填空题中等难度题查看答案及解析
-
红磷(P)和白磷(P4)均为磷的同素异形体。已知:
P4(s)+5O2(g)=P4O10(s) △H=-2983.2kJ/mol
P(s)+5/4O2(g)=1/4P4O10(s) △H=-738.5kJ/mol
写出白磷转化为红磷的热化学方程式 ,由此可知,红磷比白磷 。(填“稳定”或“不稳定”)
高二化学填空题中等难度题查看答案及解析
-
(1)P4(白磷,s)+5O2(g)══ P4O10(s) ΔH=-2983.2kJ/mol
P(红磷,s)+5/4O2(g)══ 1/4 P4O10(s) ΔH=-738.5kJ/mol
则白磷转化为红磷的热化学方程式为________,
相同状况下,红磷的稳定性比白磷________(填“强”、“弱”或“无法判断”)
(2)在原电池中,通常较活泼的金属做________极,发生________反应;
电解池中,与电源正极相连的极是________极,发生________反应。
(3)右图所示水槽中试管内有一枚铁钉,放置数天后观察:
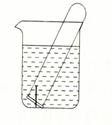
①若试管内液面上升,发生________腐蚀,正极反应式为________。
②若试管内液面下降,发生________腐蚀,正极反应式为________。
高二化学填空题中等难度题查看答案及解析
-
已知:P4 (s、白磷) + 5O2 (g) = P4O10 (s) ΔH = a kJ/mol
P (s、红磷) + 5/4 O2(g) = 1/4P4O10(s) ΔH = b kJ/mol
试写出白磷转化为红磷的热化学方程式。
高二化学选择题中等难度题查看答案及解析
-
已知:P4(s、白磷)+5O2(g)= P4O10(s) △H =-2983.2 kJ/mol,4P(s、红磷)+5O2(g)=P4O10(s) △H =-2954 kJ/mol,那么,1mol红磷转变成相应物质的量白磷时,应是( )
A. 吸收29.2kJ热量 B. 放出29.2kJ热量 C. 放出7.3kJ热量 D. 吸收7.3kJ热量
高二化学单选题中等难度题查看答案及解析
-
已知:P4(s、白磷)+5O2(g)= P4O10(s) △H = -2983.2 kJ / mol
4P(s、红磷)+5O2(g)= P4O10(s) △H = -2954 kJ / mol
那么,1mol红磷转变成相应物质的量白磷时,应是 ( )
A.吸收29.2kJ热量 B.放出29.2kJ热量
C.放出7.3kJ热量 D.吸收7.3kJ热量
高二化学选择题简单题查看答案及解析
-
已知:P4(s.白磷)+5O2(g)= P4O10(s) △H =-2983.2 kJ·mol-1
4P(s.红磷)+5O2(g)= P4O10(s) △H =-2954 kJ·mol-1
那么,1mol红磷转变成相应物质的量白磷时,应是
A.吸收29.2 kJ热量 B.放出29.2 kJ热量
C.放出7.3 kJ热量 D.吸收7.3 kJ热量
高二化学选择题简单题查看答案及解析