-
《天工开物》中对制造染料“蓝靛”的叙述如下:“凡造淀,叶与茎多者入窖,少者入桶与缸。水浸七日,其汁自来。每水浆一石,下石灰五升,搅冲数十下,淀信即结。水性定时,淀沉于底…其掠出浮沫晒干者曰靛花。”文中涉及的实验操作有
①溶解②搅拌③升华④蒸发⑤分液
A.①②③ B.①②⑤ C.①②④ D.②③④
高二化学单选题中等难度题查看答案及解析
-
对中国古代著作涉及化学的叙述,下列说法错误的是( )
A.《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油
B.《菽园杂记》有海水提取食盐的记载:“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”.过程中“灰”的作用是吸附
C.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3
D.《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2
高二化学单选题简单题查看答案及解析
-
《天工开物》中记载“铁器淬与胆矾水中,即成铜色也”,该过程中涉及的反应类型为
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
高二化学单选题简单题查看答案及解析
-
纵观古今,化学与生活皆有着密切联系。下列说法错误的是( )
A.《本草图经》在绿矾项载:“盖此矾色绿,味酸,烧之则赤…”。因为绿矾能电离出H+,所以有“味酸”.
B.《天工开物》记载:“凡白土曰垩土,为陶家精美器用”。陶是一种传统硅酸盐材料
C.“水声冰下咽,沙路雪中平”描述的是水的三态变化:“冰,水为之,而寒于水”,说明冰转化为水吸热
D.唐未《真元妙道要略)中有云:“以硫黄、雄黄合硝石并蜜烧之;焰起,烧手面及烬屋舍者”,文中描述的是黑火药的制作过程
高二化学单选题中等难度题查看答案及解析
-
“有机”一词译自“Organic”,词源解释为“属于、关于或者源自生物的”。下列关于有机化学的说法错误的是
A.3D打印技术用于有机合成,可以促进工艺的精准化和简易化
B.1828年,维勒用氰酸铵合成了尿素,实现了实验室中无机物到有机物的转化
C.宣德青花瓷所用青料“苏麻离青”属于低锰高铁类钴料,是纯天然有机材料
D.我国非遗中以板蓝根、蓝靛等为染料的扎染工艺是经验性利用有机化合物的典范
高二化学单选题中等难度题查看答案及解析
-
氯苯染料、医药工业用于制造苯酚、硝基氯苯、苯胺、硝基酚等有机中间体,橡胶工业用于制造橡胶助剂。其合成工艺分为气相法和液相法两种,实验室模拟液相法(加热装置都已略去)如下图,在C三口烧瓶中加入50.0mL苯(含催化剂FeCl3):
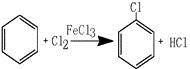
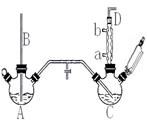
有关物质的性质:
名称
相对分子质量
沸点/(℃)
密度/(g/mL)
苯
78
78
0.88
氯苯
112.5
132.2
1.1
邻二氯苯
147
180.4
1.3
回答下列问题:
(1)A反应器是利用实验室法制取氯气,反应原理为(写化学反应方程式):_________________,装置中中空导管B的作用是__________________
(2)把干燥的氯气通入装有干燥苯的反应器C中制备氯苯,C的反应温度不宜过高,原因为①温度过高,反应得到二氯苯;②_____________,D出口的主要尾气成分有________.
(3)提纯粗产品过程如下:
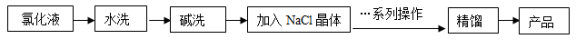
①净化过程中加入NaCl晶体的目的是吸水干燥,系列操作为___________
②为了确定所得产品为氯苯,而非二氯苯,可对产品进行分析,下列方法可行的是____
A、质谱法 B、红外光谱法 C、滴定法
(4)实验中最终得到产品14.7mL,产率为_______,产率不高的原因可能是:_____ ___
(5)苯气相氧氯化氢法制氯苯:空气、氯化氢气混合物温度210℃,进入氯化反应器,在迪肯型催化剂(CuCl2FeCl3附在三氧化铝上)存在下进行氯化,反应方程式为:_____________
高二化学实验题极难题查看答案及解析
-
下列对文献记载理解错误的是
A.《本草纲目》中记载:“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”。“取碱浣衣”与酯的水解有关
B.《天工开物》中记载:“人践着短褐、枲裳,冬以御寒,夏以蔽体,其质造物之所具也。属草木者,为枲、麻、苘、葛,属禽兽与昆虫者为裘褐、丝绵。各载其半,而裳服充焉矣”。文中的“枲、麻、苘、葛”主要成分属于糖类
C.东晋葛洪《肘后备急方》中治疟验方“青蒿一握,以水二升渍,绞取汁,尽服之”。用“绞取汁”属于萃取过程
D.《泉州府志》物产条载:“初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”文中“盖泥法”的原理类似于活性炭吸附
高二化学单选题中等难度题查看答案及解析
-
硝基苯是制造染料的重要原料,某同学在实验室里用如图所示装置制取硝基苯,主要步骤如下:
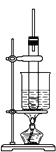
①在大试管里将2 mL浓硫酸和1.5 mL浓硝酸混合,摇匀,冷却到50~60 ℃以下;然后逐滴加入1 mL苯,边滴边振荡试管。
②按图连接好装置,将大试管放入60 ℃的水浴中加热10分钟。
完成下列填空:
(1)指出上图中的错误:__________、____________。
(2)向混合酸中加入苯时,“逐滴加入”“边滴边振荡试管”的目的是__________________________。
(3)反应一段时间后,混合液明显分为两层,上层主要物质是________(填物质名称)。把反应后的混合液倒入盛有冷水的烧杯里,搅拌,可以看到________(填字母)。
a.水面上是含有杂质的硝基苯
b.水底有苦杏仁味的液体
c.烧杯中的液态有机物只有硝基苯
d.有无色、油状液体浮在水面
(4)为了获得纯硝基苯,实验步骤:①水洗、分液;②将粗硝基苯转移到盛有__________的烧杯中洗涤、用__________(填仪器名称)进行分离;③__________;④干燥;⑤__________。
高二化学填空题中等难度题查看答案及解析
-
氯乙酸(ClCH2COOH)常用作制造各种染料、除锈剂等。实验室采用乙酸氯化法(Cl2和冰醋酸共热可制得氯乙酸,伴随有醋酸的多氯代物生成)合成氯乙酸的装置如下图(加热装置省略)。

请回答下列问题:
(1)仪器a的名称为______________(填仪器名称)。
(2)装置A中发生反应的离子方程式为_________________________________________。
(3)仪器组装完成,关闭分液漏斗活塞和止水夹K2,打开K1,向装置B中长颈漏斗中注入液体至形成一段水柱,若__________________________,则气密性良好。
(4)装置B的作用之一是观察Cl2的生成速率,则B中盛放的液体为_____________。实验结束时,关闭分液漏斗活塞和止水夹K1,此时装置B的作用是_________________________。
(5)通过佛尔哈德法可以测定氯乙酸产品中氯元素的质量分数,实验步骤如下:
Ⅰ.取0.284g粗 产品于锥形瓶中,加入足量NaOH溶液,煮沸,完全水解后加稀硝酸调至酸性。
Ⅱ.向锥形瓶中加入0.4200mol·L-1的AgNO3溶液10.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2.00mL硝基苯,用力摇动,使沉淀表面被硝基苯覆盖。
Ⅳ.加入指示剂,用0.0200mol·L-1NH4SCN标准溶液滴定过量Ag+至终点,消耗10.00mLNH4SCN溶液。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12。
①滴定选用的指示剂是_______ (填代号)。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是_____________________________,若无此操作所测氯元素的质量分数将会_______ (填“偏大”、“偏小” 或“不变”)。
③粗产品中氯元素的质量分数为 _________________。
高二化学综合题中等难度题查看答案及解析
-
Na2S可用于制造硫化染料、沉淀水体中的重金属等。
(1)Na2S溶液中S2-水解的离子方程式为_________。
(2)室温时,几种重金属离子的硫化物的溶度积常数如下表:
金属硫化物
FeS
PbS
CuS
HgS
Ksp
6.3×10-18
1.0×10-28
6.3×10-36
1.6×10-52
①向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是____。
②用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×10-6mol/L],则应满足溶液中c(S2-)≥_____mol/L。
③反应Cu2+(aq)+FeS(s)
Fe2+(aq)+CuS(s)的平衡常数K=_______。
(3)测定某Na2S和NaHS混合样品中两者含量的实验步骤如下:
步骤1.准确称取一定量样品于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容。
步骤2.准确移取25.00mL上述溶液于锥形瓶中,加入茜素黄GG-百时香酚蓝混合指示剂,用0.2500mol/L盐酸标准溶液滴定(Na2S+HCl=NaHS+NaCl)至终点,消耗盐酸24.00mL;向其中再加入5mL中性甲醛(NaHS+HCHO+H2O→NaOH+HSCH2OH)和3滴酚酞指示剂,继续用0.2500mol/L盐酸标准溶液滴定(NaOH+HCl=NaCl+H2O)至终点,又消耗盐酸34.00mL。
计算原混合物中Na2S与NaHS的物质的量之比(写出计算过程)___________。
高二化学综合题中等难度题查看答案及解析