-
周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:
(1)b、c、d中第一电离能最大的是____________(填元素符号),e的价层电子排布图为_________。
(2)a和b形成的二元共价化合物中,分子空间构型为_________;a与其他元素形成的分子中既含有极性共价键、又含有非极性共价键的化合物是__________(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_________(任写一种);酸根呈三角锥结构的酸是___________(填化学式)。
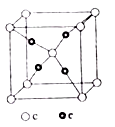
(4)e和c形成的一种离子化合物的晶体结构如图1所示,则e离子的电荷为__________。
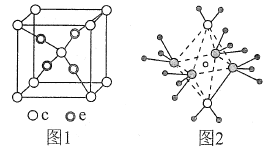
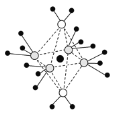
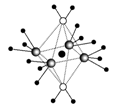
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中,阴离子为__________,阳离子中存在的化学键类型有____________;该化合物加热时首先失去的组分是____________,判断理由是___________________。
-
周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)e的价层电子排布式为__________。b、c、d三种元素中第一电离能最大的是_____(填元素名称);
(2)a和其他四种元素形成的二元共价化合物分子中既含有极性共价键、又含有非极性共价键的化合物是 __________(填化学式,写出两种);
(3)这五种元素的原子中有的能形成含氧酸,三角锥结构的酸是__________(填化学式);酸根是___________
(4)写出由这五种元素中的某些原子构成的,与3个c原子构成的分子互为等电子体的微粒_____(填化学式,写出两种)。
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,c的最外层电子数为其内层电子数的3倍,b3-与C2-核外电子排布相同, d与c同族;e的最外层只有1个电子,次外层全充满。下列说法错误的是
A. a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为sp3
B. b、c、d中电负性最大的是d
C. e的价层电子排布图为
D. 这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,该晶体结构中的作用力有离子键、极性键、配位键
-
(20分)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示图为___________ .
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________;分子中既含有极性共价键、又含有非极性共价键的化合物是_________; (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是__________;酸根呈三角锥结构的酸是___________。(填化学方式)
(4)c和e形成的一种离子化合物的晶体结构如图1,则e离子的电荷为_________。
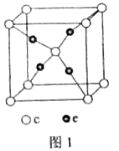
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。

该化合物中,阴离子为________,阳离子中存在的化学键类型有__________
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有一个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能由大到小的顺序是:________________(填元素符号),e的价层电子轨道示意图为__________________________________, e的焰色反应为亮绿色,请用原子结构的知识解释原因_____________________________
(2)a和b、c、d、e形成的二元共价化合物有很多种,其中有一分子呈三角锥形,该分子的中心原子的杂化方式为__________;其中有两种分子,既含有极性共价键、又含有非极性共价键的化合物是_____________________(填化学式).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的两种酸是_____;请从物质结构与性质的关系解释,这两种酸酸性强弱的原因是______________________________
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d第一电离能大小关系为___________________,e的外围电子排布图为_____________________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________;分子中既含有极性共价键,又含有非极性共价键的化合物是_____________(填化学式,写两种)。
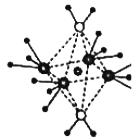
(3)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如下图所示)。该化合物中阴离子为__________,阳离子中存在的化学键类型有________________;
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是__(填元素符号),e的价层电子轨道示意图为__ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为___;分子中既含有极性共价键,又含有非极性共价键的化合物是___(填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是__;酸根呈三角锥结构的酸是___。(填化学式)
(4)e和c形成的一种离子化合物的晶体结构如图,则e离子的电荷为__。
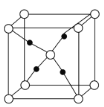
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图所示)。该化合物中阴离子为__,阳离子中存在的化学键类型有__;该化合物加热时首先失去的组分是__,判断理由是___。
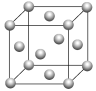
(6)用晶体的X—射线衍射法对e的测定得到以下结果:e的晶胞为面心立方最密堆积(如下图),已知该晶体的密度为9.00g·cm-3,晶胞中该原子的配位数为________;e的原子半径为________cm(阿伏加德罗常数为NA,要求列式,下同)。晶胞中原子的体积占晶胞体积的百分率为__________。
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:
b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________________。
-
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)e的价层电子排布图为______________________;
(2)a和其它元素形成的二元共价化合物中,分子中既含有极性共价键、又含有非极性共价键的化合物是_________________(填化学式,写出两种);
(3)NO3-的价层电子对数是_____________;这些元素形成的含氧酸中,酸根呈三角锥结构的酸是______________;(填化学式)
(4)e和c形成的一种离子化合物的晶体结构如图1,顶点和体心均为c,则e离子的化合价为________。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为_________,阳离子中存在的化学键类型有_________;该化合物加热时首先失去的组分是_____________,判断理由是___________________;
-
[化学——选修3:物质结构与性质]
X、Y、Z、W、Q为前四周期的五种元素,且原子序数依次增大。已知X、Y、Z、W均为非金属元素,XW2分子与Y3-为等电子体,元素W和元素Z为同族元素,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是___(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因___________________________________。
(2)XW2的电子式为______________。
(3)Q的价电子排布式为_____________,Y3-的分子构型为______________。
(4)下列关于WZ2结构的说法正确的是___________(填序号)。
a.WZ2为直线形非极性分子 b.WZ2为直线形极性分子
c.WZ2中W为sp3杂化 d.WZ2中W为sp2杂化
(5) W有两种常见的含氧酸,较高价的酸性比较低价的______,理由______________。
(6)α-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23≈140.6)
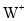 最外层有18个电子。回答下列问题:
最外层有18个电子。回答下列问题: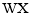 容易转化为
容易转化为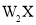 的原因是_____。
的原因是_____。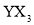 单分子是________(填“极性”或“非极性”)分子;固体
单分子是________(填“极性”或“非极性”)分子;固体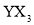 的三聚体环状结构如图所示。该结构中
的三聚体环状结构如图所示。该结构中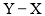 键有两类,其中键长较长的是_________(填字母)。
键有两类,其中键长较长的是_________(填字母)。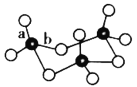
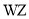 难溶于水但易溶于氨水,其原因是__________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为____________,
难溶于水但易溶于氨水,其原因是__________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为____________,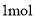 该阳离子含有________
该阳离子含有________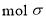 键。
键。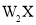 的晶胞结构如图所示。
的晶胞结构如图所示。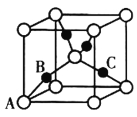
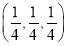 。则C原子的坐标参数为________。
。则C原子的坐标参数为________。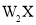 的晶胞参数为
的晶胞参数为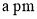 ,晶体密度为
,晶体密度为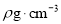 ,
,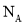 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则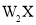 的摩尔质量为__________
的摩尔质量为__________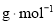 (用代数式表示)。
(用代数式表示)。








