-
现有一种铜和铁的混合物样品。某学生取10.0g此样品置于烧瓶中,将80.0mL稀硫酸分四次加入烧瓶并做相关记录。有关数据记录如下:
加硫酸的次数序号
加入硫酸的体积/mL
剩余固体的质量/g
1
20.0
7.20
2
20.0
4.40
3
20.0
2.00
4
20.0
2.00
⑴请写出铁和稀硫酸反应的离子反应方程式
⑵请计算所用硫酸溶液中硫酸的物质的量浓度。
高二化学计算题中等难度题查看答案及解析
-
(6分)现有一种铜和铁的混合物样品。为测定该样品中铁的含量,某学生取10.0 g此样品置于烧瓶中,将80.0 mL稀硫酸分四次加入烧瓶并做相关记录。
有关数据记录如下表:
加硫酸的序号
加入硫酸的体积/mL
剩余固体的质量/g
1
20.0
7.20
2
20.0
4.40
3
20.0
2.00
4
20.0
2.00
试计算:
(1)此样品中铁的质量分数。
(2)所用硫酸溶液溶质的物质的量浓度。
高二化学计算题简单题查看答案及解析
-
铁粉和铜粉混合物23.2g,逐滴加入4.00 mol·L-1的硫酸溶液,充分反应后剩余固体质量随加入硫酸溶液体积变化如下表:
硫酸溶液体积/mL
20.0
40.0
60.0
80.0
剩余固体质量/g
18.72
14.24
9.76
6.40
请回答:
(1)混合物中铁与铜的物质的量之比n(Fe)∶n(Cu)=_____________;
(2)在反应后的体系中,再加入4.00 mol·L-1H2O2溶液50.0mL,并加入足量的稀硫酸,充分反应后溶液中存在的各金属离子的物质的量分别是多少?___________________________。(计算结果保留三位有效数字)
高二化学简答题中等难度题查看答案及解析
-
实验室可利用如图实验装置合成对氨基苯磺酸。实验步骤如下:
①在一个250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放入冷水中冷却,小心地加入18 mL浓硫酸。
②将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5 h。
③将反应液冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出,过滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品。
④将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),过滤,收集产品,晾干。(说明:100 mL水在20℃时可溶解对氨基苯磺酸10.8 g,在100℃时可溶解66.7 g)
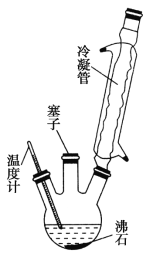
试回答下列问题。
(1)装置中冷凝管的作用是___________________。
(2)步骤②中采用油浴加热,下列说法正确的是__________(填序号)。
A.用油浴加热的好处是反应物受热均匀,便于控制温度
B.此处也可以改用水浴加热
C.实验装置中的温度计可以改变位置,也可使其水银球浸入在油中
(3)步骤③用少量冷水洗涤晶体的好处是______________________。
(4)步骤④中有时需要将“粗产品用沸水溶解,冷却结晶,过滤”的操作进行多次,其目的是_________________________________。
每次过滤后均应将母液收集起来,进行适当处理,其目的是__________________________________。
高二化学实验题中等难度题查看答案及解析
-
已知下列数据:
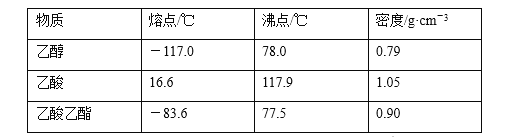
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
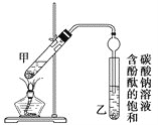
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥、蒸馏。最后得到纯净的乙酸乙酯。
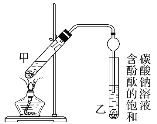
(1)反应中浓硫酸的作用是_________。
(2)写出制取乙酸乙酯的化学方程式:_________。
(3)上述实验中饱和碳酸钠溶液的作用是________。
(4)步骤②为防止加热过程中液体爆沸,该采取什么措施__________。
(5)欲将乙试管中的物质分离以得到乙酸乙酯,必须使用玻璃的仪器有____;分离时,乙酸乙酯应从仪器_____(填“下口放”或“上口倒”)出。
(6)通过分离后饱和碳酸钠中有一定量的乙醇,拟用图回收乙醇,回收过程中应控制温度是_____;找出图中的错误_____。

高二化学实验题中等难度题查看答案及解析
-
已知下列数据:
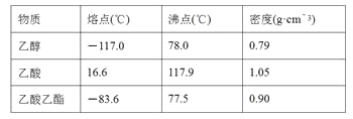
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
(1)配制①中混合溶液的方法为____________;反应中浓硫酸的作用是________________;写出制取乙酸乙酯的化学方程式:____________。
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)_________。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是_______;步骤③所观察到的现象是_________;欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有________;分离时,乙酸乙酯应从仪器________________(填“下口放”或“上口倒”)出。
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如下表:
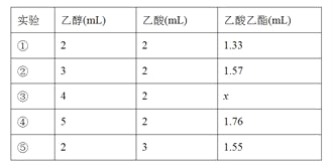
表中数据x的范围是__________________;实验①②⑤探究的是_____________。
高二化学实验题中等难度题查看答案及解析
-
已知下列数据:

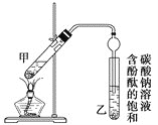
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
(1)配制①中混合溶液的方法为____________;反应中浓硫酸的作用是________________;写出制取乙酸乙酯的化学方程式:____________。
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)_________。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是_______;步骤③所观察到的现象是_________;欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有________;分离时,乙酸乙酯应从仪器________________(填“下口放”或“上口倒”)出。
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如下表:

表中数据x的范围是__________________;实验①②⑤探究的是_____________。
高二化学实验题中等难度题查看答案及解析
-
下列有关化学反应速率的说法正确的是( )
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.10.0 mL 2 mol·L ﹣1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
高二化学单选题简单题查看答案及解析
-
现有3.58gNa2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896ml(设气体全部逸出,下同)。回答下列问题:
(1)其中________过量。
(2)固体混合物中Na2CO3和NaHCO3的物质的量之比为________。
(3)取xg上述Na2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加40.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为448ml,则x的值可能为________。
(4)取xg上述Na2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加40.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为yml,当2.864≤x<14.32时,y与x的函数关系式是y=________。
高二化学填空题中等难度题查看答案及解析
-
(12分)乙醚极易挥发、微溶于水、是良好的有机溶剂。乙醇与浓硫酸的混合物在不同温度下反应能生成乙烯或乙醚。某实验小组用下图装置制取乙醚和乙烯。
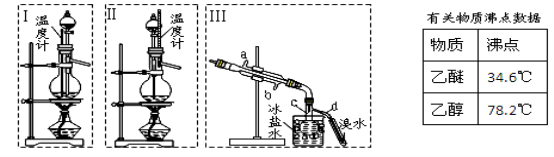
1.制乙醚:在蒸馏烧瓶中先加入10 mL乙醇,慢慢加入10 mL浓硫酸,冷却,固定装置。加热到140℃时,打开分液漏斗活塞,继续滴加10 mL乙醇,并保持140℃,此时烧瓶c中收集到无色液体。
(1)Ⅰ和Ⅱ是反应发生装置,应该选择 (选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连。
(2)乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是
。
2.Ⅲ中水冷凝管的进水口是 (选答“a”或“b”)。冰盐水的作用是 。
3.有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险。该同学设
计了以下几种装置与导管d连接,你认为合理的是(选填编号) 。
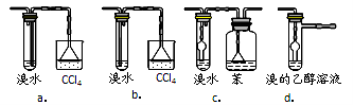
4.反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色。写出实验过程中有气体生成化学方程式(写两个方程式) ; 。
5.实验中收集到的乙醚产品中可能含有多种杂质。某同学设计了以下提纯方案:
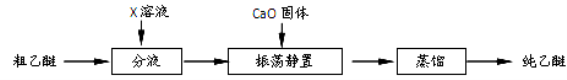
(1)分液步骤除去产品中的酸性杂质,则X可以是 。
(2)蒸馏操作可除去的杂质是 。
高二化学实验题中等难度题查看答案及解析