-
(12分)化合物KaFeb(C2O4)c·dH2O(其中铁为正三价)是重要的光化学试剂。通过下述实验确定该晶体的组成。
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2+8H2O
(1)草酸(H2C2O4)为二元弱酸,其一级电离的方程式为 。草酸的Ka1约为Ka2的1000倍,可能的原因是 。
(2)滴定终点观察到的现象为 。
(3)通过计算确定样品的组成(写出计算过程)。
-
实验室模拟用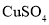 溶液和
溶液和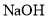 溶液混合制备
溶液混合制备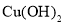 ,再将所得
,再将所得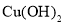 与
与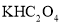 溶液混合,可制备草酸合铜酸钾晶体
溶液混合,可制备草酸合铜酸钾晶体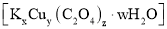 。通过下述实验确定该晶体的组成。
。通过下述实验确定该晶体的组成。
步骤Ⅰ 称取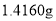 样品,放入锥形瓶,加入适量
样品,放入锥形瓶,加入适量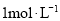 稀硫酸,微热使样品溶解,再加入
稀硫酸,微热使样品溶解,再加入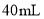 水加热,用
水加热,用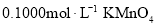 溶液滴定至终点,消耗
溶液滴定至终点,消耗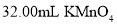 溶液。
溶液。
步骤Ⅱ 将步骤Ⅰ的溶液充分加热,使淡紫红色消失,溶液最终显示蓝色。冷却后,调节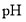 并加入过量
并加入过量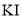 固体,与
固体,与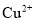 反应生成
反应生成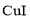 沉淀和
沉淀和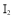 ,以淀粉作指示剂,用
,以淀粉作指示剂,用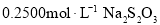 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗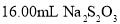 标准溶液。
标准溶液。
已知: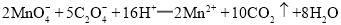 ;
;
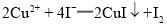 ;
;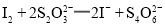
回答下列问题:
(1)室温下,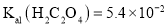 ,
,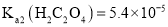 ,
,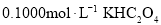 溶液
溶液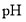 ________7(填“>”或“<”或“=”)。
________7(填“>”或“<”或“=”)。
(2)步骤Ⅱ中滴定终点的现象为________。
(3)步骤Ⅱ中若消耗的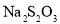 标准溶液的体积偏大,可能的原因有________(填字母)。
标准溶液的体积偏大,可能的原因有________(填字母)。
A.滴定前未将待测溶液充分加热
B.锥形瓶水洗后未干燥
C.装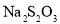 标准溶液的滴定管水洗后未润洗
标准溶液的滴定管水洗后未润洗
D.滴定时锥形瓶中有液体溅出
(4)通过计算确定该晶体的化学式(写出计算过程)。
________________________
-
三草酸合铁(III)酸钾Kx[Fey(C2O4)z]•nH2O可用于摄影。为确定其组成进行如下实验:
步骤1:准确称取该晶体0.9820g,配成溶液,平均分成10份。
步骤2:取一份溶液,酸化,加热,用SnCl2-TiCl3将Fe3+全部还原为Fe2+,再加0.0100mol•L-1KMnO4至恰好反应,将C2O42-全部氧化成CO2,Fe2+全部氧化成Fe3+,消耗KMnO4体积28.00mL。
步骤3:另取一份溶液,酸化,加入0.0100mol•L-1KMnO4至恰好反应完全,将C2O42-全部氧化成CO2,消耗KMnO4体积24.00mL。(已知:MnO4-还原产物为Mn2+,上述实验数据为多次实验有效数据平均值)
下列判断正确的是
A.取溶解后待测液少许,先加少量氯水,再加KSCN产生血红色溶液,则有Fe2+
B.步骤3的离子方程式为:5C2O42-+2MnO4-+8H2O =10CO2 ↑+2Mn2++16OH-
C.x:z = 1:2
D.该晶体的化学式为:K3[Fe(C2O4)3]•3H2O
-
三草酸合铁(III)酸钾Kx[Fey(C2O4)z]•nH2O可用于摄影。为确定其组成进行如下实验:
步骤1:准确称取该晶体0.9820g,配成溶液,平均分成10份。
步骤2:取一份溶液,酸化,加热,用SnCl2-TiCl3将Fe3+全部还原为Fe2+,再加0.0100mol•L-1KMnO4至恰好反应,将C2O42-全部氧化成CO2,Fe2+全部氧化成Fe3+,消耗KMnO4体积28.00mL。
步骤3:另取一份溶液,酸化,加入0.0100mol•L-1KMnO4至恰好反应完全,将C2O42-全部氧化成CO2,消耗KMnO4体积24.00mL。(已知:MnO4-还原产物为Mn2+,上述实验数据为多次实验有效数据平均值)
下列判断正确的是
A. 取溶解后待测液少许,先加少量氯水,再加KSCN产生血红色溶液,则有Fe2+
B. 步骤3的离子方程式为:5C2O42-+2MnO4-+8H2O =10CO2 ↑+2Mn2++16OH-
C. x:z = 1:2
D. 该晶体的化学式为:K3[Fe(C2O4)3]•3H2O
-
草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,试回答下列问题:
(1)写出滴定实验中所发生反应的化学方程式:_______________
(2)实验中KMnO4溶液应装在____式滴定管中,滴定终点的判断依据是________________
(3)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1
(4)若滴定终点读数时目光俯视,则计算出的x值可能___________(填偏大、偏小、无影响)
-
草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
试回答下列问题:
(1)实验中不考虑铁架台等夹持仪器外,需要的仪器有(填序号)___________,还缺少的仪器有(填名称)____________。
A.托盘天平(带砝码,镊子) B.滴定管 C. 100mL容量瓶 D.烧杯E.漏斗 F.锥形瓶 G.玻璃棒 H.烧瓶
(2)实验中KMnO4溶液应装在____式滴定管中,滴定终点的判断依据是_________________
(3)若在滴定前没有用amol·L-1的KMnO4溶液对滴定管进行润洗,则所测得的x值会___________(偏大、偏小、无影响)。
(4)若滴定终点读数时目光仰视,则计算出的x值可能_______________(填偏大、偏小、无影响)。
(5)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1 。
-
草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,
试回答下列问题:
(1)写出滴定实验中所发生反应的离子方程式:_________________________________________________________
(2)实验中KMnO4溶液应装在___________式滴定管中,滴定终点的判断依据是_______________________________
(3)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1
(4)若滴定终点读数时目光俯视,则计算出的x值可能_______________(填“偏大”、“偏小”、“无影响”)
(5)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是______(填选项字母)。
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
-
在实验室利用胆矾晶体和烧碱溶液制备氧化铜固体,其实验操作可分解为如下几步:①混合;②过滤;③加热分解;④溶解;⑤洗涤。就此实验完成下列填空:
(1)正确操作步骤的顺序是________(填序号)。
(2)步骤②中所用到的玻璃仪器有________。
(3)在实验中多次用到玻璃棒,其作用有三个,是______、_____、______。
-
草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下述实验:①称取Wg草酸晶体配成100.0mL水溶液 ②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为amol/L KMnO4溶液滴定。滴定时,所发生的反应为:
2KMnO4 +5H2C2O4 +3H2SO4=K2SO4 +10CO2+2MnSO4 +8H2O 回答下列问题:
(1)实验①中,为配制准确物质的量浓度的草酸溶液,所需用到的仪器是天平(含砝码)、烧杯、药匙、胶头滴管和 _______、 __________ 。
(2)实验②中,滴定时,KMnO4溶液应装在_______式滴定管中(填“酸”或“碱”)
(3)若滴定用的KMnO4溶液因久置而部分变质,浓度偏低,则实验结果所测定的x值将_____(填“偏高”,“偏低”,“无影响”)。
(4)在滴定过程中起指示剂作用的是______,当KMnO4溶液与草酸反应后,怎样判断滴定终点____________________________________________________________________________.
(5)若达到滴定终点时,共用去amol/LKMnO4溶液VmL,则实验测得所配草酸溶液的物质的量浓度为_______;由此计算出草酸晶体中的x值是__________。(结果用a,v, W表示)
-
下述实验装置与其对应的实验描述正确的是
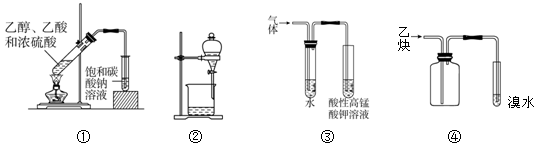
A.实验①用于制备比较纯净的乙酸乙酯
B.实验②用于分离甘油与水的混合物
C.实验③用于验证溴乙烷在氢氧化钠、乙醇溶液中发生消去反应产生的乙烯气体
D.实验④收集乙炔并验证它与溴水发生加成反应
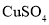 溶液和
溶液和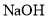 溶液混合制备
溶液混合制备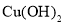 ,再将所得
,再将所得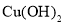 与
与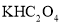 溶液混合,可制备草酸合铜酸钾晶体
溶液混合,可制备草酸合铜酸钾晶体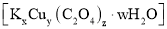 。通过下述实验确定该晶体的组成。
。通过下述实验确定该晶体的组成。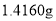 样品,放入锥形瓶,加入适量
样品,放入锥形瓶,加入适量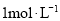 稀硫酸,微热使样品溶解,再加入
稀硫酸,微热使样品溶解,再加入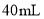 水加热,用
水加热,用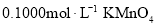 溶液滴定至终点,消耗
溶液滴定至终点,消耗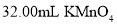 溶液。
溶液。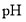 并加入过量
并加入过量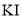 固体,与
固体,与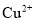 反应生成
反应生成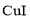 沉淀和
沉淀和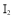 ,以淀粉作指示剂,用
,以淀粉作指示剂,用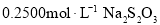 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗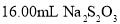 标准溶液。
标准溶液。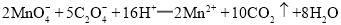 ;
;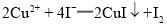 ;
;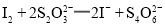
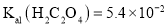 ,
,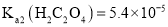 ,
,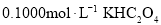 溶液
溶液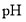 ________7(填“>”或“<”或“=”)。
________7(填“>”或“<”或“=”)。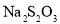 标准溶液的体积偏大,可能的原因有________(填字母)。
标准溶液的体积偏大,可能的原因有________(填字母)。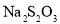 标准溶液的滴定管水洗后未润洗
标准溶液的滴定管水洗后未润洗