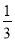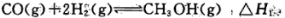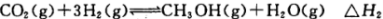-
新技术的开发应用,不仅有利于改善环境质量,而且能充分开发“废物”的潜在价值。回答下列问题:
(1)用烟道气与氢气来合成甲醇涉及到如下几个反应:
①CO(g)+2H2(g)=CH3OH(g) ΔH=-91kJ·mol-1
②2CO2(g)=2CO(g)+O2(g) ΔH=+566kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
④CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=___________kJ·mol-1。
(2)在容积均为2L的两个恒容密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g),有关数据如下:
CO2(g)+H2(g),有关数据如下:
| 容器 | 温度/℃ | 起始量 | 达到平衡 |
| CO/mol | H2O/mol | H2/mol | CO转化率 | 所需时间/min |
| 1 | 800 | 2 | 1 | | 
| 3 |
| 2 | 800 | 1 | 2 | n | x | |
①800°C时该反应的平衡常数K=____________。
②容器2中x=_______,n=_______。
(3)反应(NH4)2CO3+H2O+CO2 2NH4HCO3可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
2NH4HCO3可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
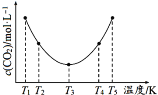
①ΔH______0(填“>”“<”或“=”)。T1~T2区间,c(CO2)变化的原因是______。
②已知常温下NH3·H2O的电离常数K=1.8×10-5,碳酸的电离常数K1=4.4×10-7、K2=4.7×10-11,则恰好完全反应时所得的NH4HCO3溶液中c(H+)______c(OH-)(填“>”“<”或“=”)。
③在图中所示五种温度下,该反应的平衡常数最大的温度是______。
-
(1)甲醇是可再生能源,具有开发应用的广阔前景,回答下列问题:
一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是________(填序号).
A.每消耗1mol CO的同时生成2molH2 B.混合气体总物质的量不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.生成CH3OH的速率与消耗CO的速率相等
②CO的平衡转化率(α)与温度、压强的关系如图所示.A、B两点的平衡常数K(A)________K(B)(填“>”、“=”或“<”).

(2)已知25℃合成氨反应中,1mol N2完全转化为NH3时释放的能量为92.4 kJ。现将1mol N2和3mol H2混合置于2L密闭容器中,反应进行到2s末测得NH3为0.4mol。回答下列问题:
① 该反应的热化学方程式是________ ;
② 该反应达到平衡后,升高温度平衡向________ (填“正反应方向”、“逆反应方向”)移动;加入催化剂平衡________(填“正”、“逆”、 “不”)移动;
③ 前2s内v(H2)是________。
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是 (填序号).
A.每消耗1mol CO的同时生成2molH2 B.混合气体总物质的量不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.生成CH3OH的速率与消耗CO的速率相等
②CO的平衡转化率(α)与温度、压强的关系如下图所示。

A、B两点的平衡常数K(A) K(B)(填“>”、“=”或“<”).
③某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,
CO的转化率= ,此温度下的平衡常数K= (保留两位有效数字).
-
(18分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)分析该反应并回答下列问题:
①平衡常数表达式为K=__________________。
②下列各项中,不能够说明该反应已达到平衡的是________(填序号)。
A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)下图是该反应在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是________。
A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
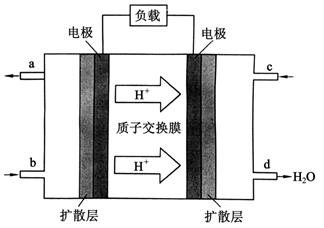
①该电池工作时,b口通入的物质为______________,c口通入的物质为_____________。
②该电池正极的电极反应式为:________。
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有_____________NA个电子转移。
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)⇌CH3OH(g).
(1)分析该反应并回答下列问题:
①平衡常数表达式为K=________.
②下列各项中,不能够说明该反应已达到平衡的是________(填序号).
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗2mol CO,同时生成1mol CH3OH
e.恒温、恒容条件下,容器内的气体密度不发生变化
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H________0(填“>”、“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”
(3)某温度下,向容积为1 L的密闭反应器中充入0.50 mol CO和0.90 mol H2,当反应器中的气体压强不再变化时测得CO的转化率为80%,则该温度下反应CO(g)+2H2(g)⇌CH3OH(g)平衡常数为________.
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)⇌CH3OH(g).

(1)分析该反应并回答下列问题:
①平衡常数表达式为K=________.
②下列各项中,不能够说明该反应已达到平衡的是________(填序号).
A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2mol CO,同时生成1mol CH3OH
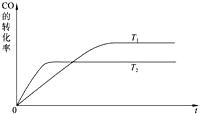
(2)如图1是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H________0(填“>”、“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”).
③若容器容积不变,下列措施可增加甲醇产率的是________.
A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,b口通入的物质为________,c口通入的物质为________.
②该电池正极的电极反应式为:________.
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,有________NA个电子转移.
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:CO(g)+2H2(g)  CH3OH(g)
CH3OH(g)
(1)分析该反应并回答下列问题:
①该反应的平衡常数表达式为K=____________。
②下列选项能判断该反应达到平衡状态的依据有__________(填序号)。
A.2v(正)(H2)= v(逆)(CO)
B.一定条件下,单位时间内消耗2molH2的同时生成 1mol CH3OH
C.恒温、恒容时,容器内的压强不再变化
D.恒温、恒容时,容器内混合气体的密度不再变化
E.混合气体的平均相对分子质量不随时间而变化
(2))下图是该反应在不同温度下CO转化率随时间的变化曲线:
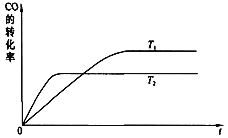
①该反应的△H________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1 ________ K2(填“>”、“<”或“=”)。
(3)某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为________________。
(4)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式________________________。
(5)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
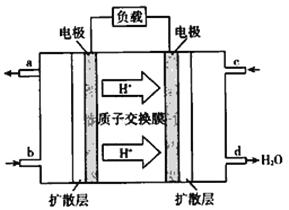
①该电池工作时,b口通入的物质为__________(填 化学式,下同),c 口通入的物质为__________。 ②该电池正极的电极反应式为_______________。
-
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:CO(g)+2H2(g)  CH3OH(g)
CH3OH(g)
(1)分析该反应并回答下列问题:
①该反应的平衡常数表达式为K=____________。
②下列选项能判断该反应达到平衡状态的依据有__________(填序号)。
A.2v(正)(H2)= v(逆)(CO)
B.一定条件下,单位时间内消耗2molH2的同时生成 1mol CH3OH
C.恒温、恒容时,容器内的压强不再变化
D.恒温、恒容时,容器内混合气体的密度不再变化
E.混合气体的平均相对分子质量不随时间而变化
(2))下图是该反应在不同温度下CO转化率随时间的变化曲线:
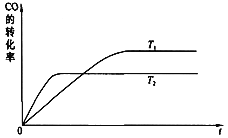
①该反应的△H________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1 ________ K2(填“>”、“<”或“=”)。
(3)某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为________________。
(4)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式________________________。
(5)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为__________(填 化学式,下同),c 口通入的物质为__________。 ②该电池正极的电极反应式为_______________。
-
能源短缺是人类社会面临的重大问题,世界各国都在努力寻找新能源,探求绿色能源的开发。甲醇是一种可再生能源,是一种污染性较小,热值较大的能源,因而具有广泛的开发价值和良好的应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: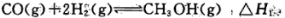
反应Ⅱ: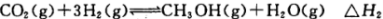
①上述反应符合“原子经济”原则的是_________(填“I’’或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)

由表中数据判断△H1_________0(填“>”、“=”或“<”),说明生成物的总能量一定_______(填“>”、“=”或“<”)反应物的总能量。
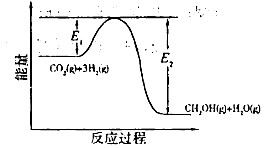
③反应Ⅱ反应历程如下图,回答下列问题;在反应体系中加入催化剂,反应速率增大,E1、E2和△H2的变化是:E1_________、E2_________、△H2_________(填“增大”“减小”“不变”)。
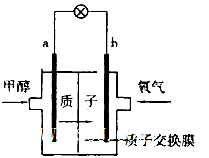
(2)最新研制的一种新型甲醇电池示意图如图,电池的两极分别充人甲醇和氧气(池内为酸性介质)。则电池工作时____________(填a或b)为正极,a极的电极反应式为______________。
-
应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知:①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) ΔH=-38.19 kJ·mol-1
则表示 CH3OH的燃烧热的热化学方程式为___________ 。
(2)在一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)  CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
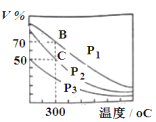
①该反应的反应热 ΔH________ 0(填“>”或“<”), 在_______ (填“高温”、“低温” )下易自发,压强的相对大小与 p1_______ p2(填“>”或“<”)。
②压强为 p2,温度为300℃时,该反应的化学平衡常数的计算表达式为 K=_______。
③下列各项中,不能说明该反应已经达到平衡的是_______。
A.容器内气体压强不再变化 B.υ(CO):υ(H2)=1:2
C.容器内的密度不在变化 D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证 H2浓度不变的情况下,增大容器的体积,平衡_______。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
 CO2(g)+H2(g),有关数据如下:
CO2(g)+H2(g),有关数据如下: 2NH4HCO3可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图:
2NH4HCO3可用于捕捉空气中的CO2,为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测定CO2气体的浓度,得到的曲线图如图: