-
工业上从海水中提取金属镁,工艺流程如图:
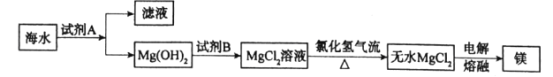
(1)试剂A为____(填名称,下同),试剂B为____。
(2)为探究制得的金属镁与金属铜、钛的金属活动性强弱,某兴趣小组将打磨过的钛片投入硫酸铜溶液中,一段时间后在钛片的表面析出红色固体,则钛和铜的金属活泼性:Ti____Cu(填“>”,“<”或“=”),上述反应的离子方程式为____。(已知Ti在化合物中一般显+4价)。为比较镁与钛的金属活泼性强弱,该兴趣小组设计原电池如图所示:
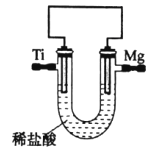
若Mg片不断溶解,Ti片上有无色气泡产生,则可证明Ti____Mg(填“>”、“<”或“=”)。请写出该电池的负极的电极反应式:____。
-
海洋资源的利用具有广阔前景.
(1)如图是从海水中提取镁的简单流程.

工业上常用于沉淀Mg2+的试剂A是______(填物质名称),Mg(OH)2转化为MgCl2的离子方程式是______.
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带 海带灰
海带灰 滤液
滤液

 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______.
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______.
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:
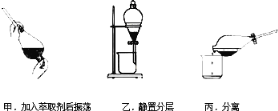
甲、乙、丙3步实验操作中,不正确的是______(填“甲”、“乙”或“丙”).
-
海洋资源的利用具有广阔前景.
(1)如图是从海水中提取镁的简单流程.
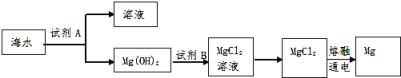
工业上常用于沉淀Mg2+的试剂A是______(填物质名称),Mg(OH)2转化为MgCl2的离子方程式是______.
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带 海带灰
海带灰 滤液
滤液

 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______.
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______.
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:
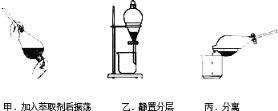
甲、乙、丙3步实验操作中,不正确的是______(填“甲”、“乙”或“丙”).
-
金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3).从不同途径获得镁的流程如图所示:
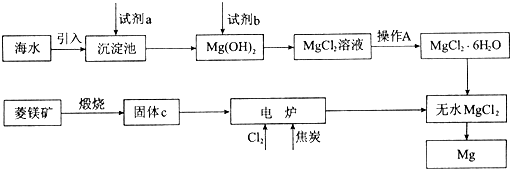
回答下列问题:
(1)试剂a的化学式是______.
(2)加入试剂b发生反应的离子方程式是______.
(3)操作A是蒸发浓缩、冷却结晶、______.
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是______ MgCl2+CO
-
(7分)金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
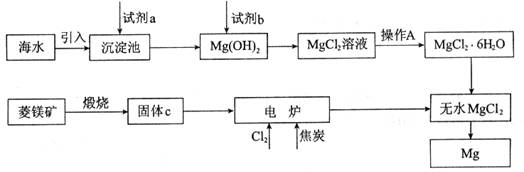
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
-
下列有关工业生产的叙述不正确的是
A.用海水淡化后的浓缩海水作原料提取溴
B.在太阳能资源相对充足的沿海地区建造海水淡化厂
C.利用“海水→氯化钠→金属钠→氢氧化钠”的工艺流程生产烧碱
D.利用“海水→氢氧化镁→氯化镁→金属镁”的工艺流程生产金属镁
-
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
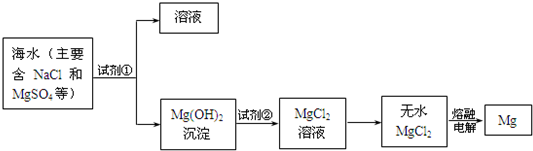
试回答下列问题:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用______(填试剂名称),反应的离子方程式为_____;
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是______;
(3)试剂②可以选用______;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式______.
-
南通有较长的海岸线, 海水资源的利用具有广阔的前景。工业上从海水中提取Br2与Mg 的流程如图:
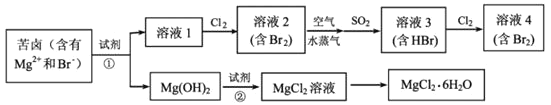
(1)写出一种海水淡化的方法:_______________。
(2)用电子式表示 MgCl2的形成过程:____________ 。
(3)工业上用MgCl2 制取 Mg 一般常用的方法是________。
A.电解法 B.还原剂还原法 C.热分解法 D.铝热法
(4)提取溴的过程中,经过2次Br-⟶Br2转化的目的是 ___________ 。
(5)反应①,SO2被Br2氧化为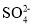 ,则该反应中消耗的n(SO2):n(Br2)= __;反应②的离子方程式为 __________。
,则该反应中消耗的n(SO2):n(Br2)= __;反应②的离子方程式为 __________。
(6)用下面提供的试剂,设计简单的实验证明Br 的非金属性比 I 强。(已知Br2 和I2溶在水中浓度较稀时都呈黄色)。__________。(可选择的试剂:溴水、碘水、KI 溶液、四氯化碳、氯水、淀粉溶液。)
-
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。如图是工业上提镁的流程。
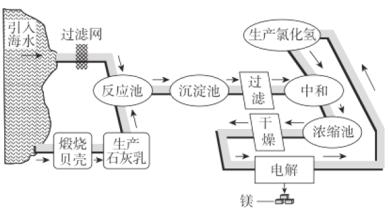
(1)电解熔融MgCl2制金属镁的化学方程式是________。
(2)“反应池’→……→‘中和’”过程的主要作用:①除去海水中的其他杂质;②________。
(3)“中和”时,Mg(OH)2与盐酸发生反应的离子方程式是________。
(4)在上述流程中,可循环使用的物质是________。
-
(8分)海水是资源的宝库,海水淡化可获得淡水和浓海水。浓海水中主要含有的离子有Na+、 Mg2+ 、Cl﹣、SO42﹣。从浓海水中提取金属镁的一段工艺流程如图所示:
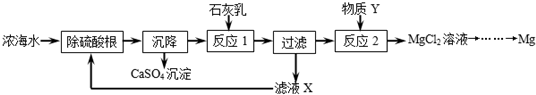
(1)补全由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中所需的条件或反应物:

(2)写出反应2的化学方程式:____________________。
(3)操作流程中可循环使用的物质是___________(填化学式)。










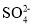 ,则该反应中消耗的n(SO2):n(Br2)= __;反应②的离子方程式为 __________。
,则该反应中消耗的n(SO2):n(Br2)= __;反应②的离子方程式为 __________。
