(7分)
(1)NF3分子中N原子的杂化轨道类型为__________,该分子的空间构型为________
(2)[Cu(NH3)4]SO4属于配合物,其中 原子提供孤对电子。配合物 Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,Fe(CO)5晶体属于 (填晶体类型)。
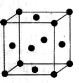
(3)金属铜晶体的晶胞结构如图所示(面心立方晶胞):若该晶胞边长为dnm,铜的相对原子质量为64,阿伏加德罗常数为NA,则该晶体的密度为 g/cm3(列表达式)
高二化学填空题中等难度题
(7分)
(1)NF3分子中N原子的杂化轨道类型为__________,该分子的空间构型为________
(2)[Cu(NH3)4]SO4属于配合物,其中 原子提供孤对电子。配合物 Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,Fe(CO)5晶体属于 (填晶体类型)。
(3)金属铜晶体的晶胞结构如图所示(面心立方晶胞):若该晶胞边长为dnm,铜的相对原子质量为64,阿伏加德罗常数为NA,则该晶体的密度为 g/cm3(列表达式)

高二化学填空题中等难度题
(7分)
(1)NF3分子中N原子的杂化轨道类型为__________,该分子的空间构型为________
(2)[Cu(NH3)4]SO4属于配合物,其中 原子提供孤对电子。配合物 Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,Fe(CO)5晶体属于 (填晶体类型)。
(3)金属铜晶体的晶胞结构如图所示(面心立方晶胞):若该晶胞边长为dnm,铜的相对原子质量为64,阿伏加德罗常数为NA,则该晶体的密度为 g/cm3(列表达式)

高二化学填空题中等难度题查看答案及解析
下列分子中,中心原子杂化轨道类型相同,分子的空间构型也相同的是
A.BeCl2、CO2B.H2O、SO2C.SO2、CH4D.NF3、CH2O
高二化学选择题简单题查看答案及解析
根据价层电子对互斥理论及原子轨道的杂化理论判断NF3分子的空间构型和中心原子的杂化方式为()
A. 直线形sp杂化 B. 三角形 sp2杂化
C. 三角锥形 sp2杂化 D. 三角锥形 sp3杂化
高二化学单选题中等难度题查看答案及解析
根据价层电子对互斥理论及原子轨道的杂化理论判断NF3分子的空间构型和中心原子的杂化方式为()
A.直线形 sp杂化 B.三角形 sp2杂化
C.三角锥形 sp2杂化 D.三角锥形 sp3杂化
高二化学单选题中等难度题查看答案及解析
根据价层电子对互斥理论及原子的杂化轨道理论判断NF3分子的空间构型和中心原子的杂化方式为( )
A. 直线形 sp杂化 B. 三角形 sp2杂化
C. 三角锥型 sp2杂化 D. 三角锥型 sp3杂化
高二化学单选题中等难度题查看答案及解析
下列关于粒子结构的描述正确的是
A.NF3和BF3是中心原子杂化类型相同的极性分子
B.CH2Cl2和C2H4是空间构型不同的非极性分子
C.在SiO2晶体中,Si原子与Si—O键数目比为1︰2
D.CF4和CO2是含极性键的非极性分子
高二化学单选题中等难度题查看答案及解析
下列关于粒子结构的描述正确的是
A.NF3和BF3是中心原子杂化类型相同的极性分子
B.CH2Cl2和C2H4是空间构型不同的非极性分子
C.在SiO2晶体中,Si原子与Si—O键数目比为1︰2
D.CF4和CO2是含极性键的非极性分子
高二化学选择题中等难度题查看答案及解析
氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3的沸点由高到低的顺序是 ,这三种化合物中N原子的杂化类型是 ,分子的空间构型是 。
(2)氮和磷同主族,科学家目前合成了N4分子,该分子中N-N键的键角为 。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-互为等电子体的分子 。
(4)Fe2+、Cu2+、Co3+等过渡金属离子都能与叠氮化物、氰化物形成配合物。Fe2+的核外电子排布式为 ;配合物[Co(N3)(NH3)5]SO4中Co3+的配位数为 。
(5)NaN3与KN3相比,NaN3的晶格能 KN3的晶格能(填“>”、“=”或“<”)。
高二化学填空题困难题查看答案及解析
NF3分子中的中心原子采取sp3杂化,下列有关叙述正确的是( )
A. NF3分子的空间构型为三角锥形
B. NF3分子的空间构型为平面三角形
C. NF3分子的N—F键夹角与CH4分子中的C—H键的夹角相等
D. NF3分子是非极性分子
高二化学选择题中等难度题查看答案及解析
计算下列分子或离子中的价电子对数,并根据已学填写下表
| 物质 | 价电子 对数 | 成键电 子对数 | 孤电子 对数 | 中心原子杂 化轨道类型 | 杂化轨道/电子 对空间构型 | 轨道 夹角 | 分子空 间构型 | 键角 |
| CO2 | ||||||||
| BF3 | ||||||||
| CH4 | ||||||||
| H2O | ||||||||
| NH3 | ||||||||
| PCl3 |
高二化学填空题简单题查看答案及解析