-
无水AlCl3是一种重要的有机合成催化剂,该物质在183℃时升华,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水AlCl3,实验装置如下图所示。请回答:
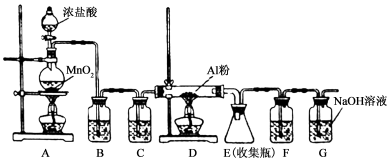
(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是________。
a.加入MnO2粉末
b.点燃A中酒精灯
c.加入浓盐酸
d.点燃D处酒精灯
(2)写出A装置中发生反应的化学方程式___________________________________。
(3)装置B中的试剂是__________。该装置存在安全隐患,请指出 。
(4)装置F中试剂为 ,甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果。这种药品可以是 ,其作用是 。
-
(9分)无水AlCl3是一种重要的有机合成催化剂,该物质在183℃时升华,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水AlCl3,实验装置如下图所示。

请回答下列问题:
(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是________。
a.加入MnO2粉末 b.点燃A中酒精灯 c.加入浓盐酸 d.点燃D处酒精灯
(2)写出A装置中发生反应的离子方程式___________________________________。
(3)装置B中的试剂是__________。该装置存在安全隐患,请指出 。
(4)甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果。这种药品可以是____。
(5)E中得到少量白色粉末,打开软木塞后可明显观察到锥形瓶中有白雾生成,用化学方程式表示其原因____________________________________________。
-
氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝(无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾).可用下列装置制备.
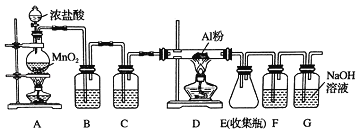
(1)装置B中盛放_____溶液,其作用是_____.F中的是_____溶液,其作用是_____.用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为_____.

(2)装置A实验开始时,先检查装置气密性,接下来的操作依次是_____(填序号).
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
(3)制备反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学提出很多实验方案,其中方案之一为让残留的液体与足量Zn反应,测量生成的H2体积.装置如右图所示(夹持器具已略去).
①使Y形管中的残余清液与锌粒反应的正确操作是将_____转移到_____中.
②反应完毕,每间隔1分钟读取气体体积、气体体积逐渐减小,直至不变.气体体积逐次减小的原因是_____(排除仪器和实验操作的影响因素)。
-
氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝(无水AlCl3 (183℃升华) 遇潮湿空气即产生大量白雾)。可用下列装置制备。
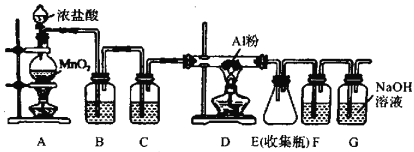
(1)装置B中盛放____溶液,C和F中装的是同一种试剂,该试剂为________________。
(2)装置A 的圆底烧瓶中发生反应的化学方程式为_______________________________。
(3)实验步骤:如图连接装置后,先检验装置气密性,再装药品,然后点燃___________(填“A”或“C”) 处酒精灯,当____ (填实验现象) 时,再点燃___________(填“A”或“C”)处酒精灯。
(4)装置G 的作用是__________________,写出G 中反应的离子方程式_____________________。
(5)甲同学认为装置D和E中间的细玻璃导管换成粗的玻璃导管为什么?___________________________________________________。
-
氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝(无水AlCl3 (183℃升华) 遇潮湿空气即产生大量白雾)。可用下列装置制备。
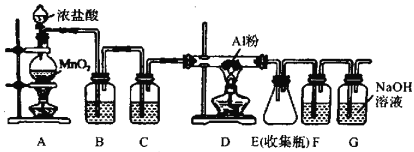
(1)装置B中盛放____溶液,C和F中装的是同一种试剂,该试剂为________________。
(2)装置A 的圆底烧瓶中发生反应的化学方程式为_______________________________。
(3)实验步骤:如图连接装置后,先检验装置气密性,再装药品,然后点燃___________(填“A”或“C”) 处酒精灯,当____ (填实验现象) 时,再点燃___________(填“A”或“C”)处酒精灯。
(4)装置G 的作用是__________________,写出G 中反应的离子方程式_____________________。
(5)甲同学认为装置D和E中间的细玻璃导管换成粗的玻璃导管为什么?___________________________________________________。
-
氯气在工业上有着重要的用途,某兴趣小组在实验室中用下列装置模拟工业上用氯气制备无水氯化铝(183℃时升华,遇潮湿空气即产生大量白雾)。

 请回答下列问题:
请回答下列问题:
(1)装置 B 中盛放饱和食盐水,其作用是 。F 中盛放的是 ,其作用是 。用一件仪器装填适当试剂后也可起到 F 和 G 的作用,所装填的试剂为 。
(2)装置 A 实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
A.往烧瓶中加入 MnO2 粉末 B.加热 C.往烧瓶中加入浓盐酸
(3)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学 提出很多实验方案,其中方案之一为让残留的液体与足量 Zn 反应,测量生成的 H2体积。 装置如图所示(夹持器具已略去)。反应完毕,每间隔 1 分钟读取气体体积、气体体积逐渐减小,直至不变。气体体积逐次减小的原因是 (排除仪器和实验操作的影响因素)。
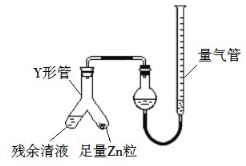
(4)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量 ClO2 生成;ClO2 沸点为 10 ℃,熔点为−59 ℃,液体为红色;Cl2 沸点为−34 ℃,液态为黄绿色。设计最简单的实验验证 Cl2中含有 ClO2: 。
-
无水AlCl3(183℃升华)遇潮湿空气即变质,同时产生大量白雾,实验室可用下列装置制备。

(1)反应前,装置A中盛放浓盐酸的仪器名称是_____。
(2)反应时,装置A中发生反应的化学方程式是_____。
(3)装置B中盛放的是饱和NaCl溶液,作用是_____。
(4)装置F中试剂的作用是_____。
(5)装置G用于吸收多余Cl2,反应的离子方程式是_____。
-
无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
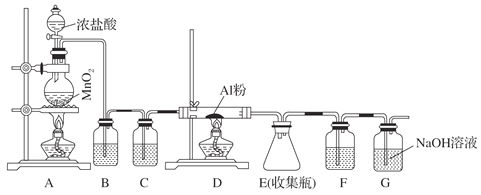
(1)其中装置A用来制备氯气,写出其离子反应方程式:_____________________________。
(2)装置B中盛放饱和NaCl溶液,该装置的主要作用是_____________________________。
(3)G为尾气处理装置,其中反应的化学方程式:___________________________________。
(4)制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:与足量AgNO3溶液反应,称量生成的AgCl质量。此方案__________(填“可行”,“不可行”)并说明理由__________________________________________________。
-
Ⅰ. 无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝的试剂瓶久置于潮湿空气中,会自动爆炸并产生大量白雾.氯化铝常作为有机合成和石油工业的催化剂,并用于处理润滑油等.工业上由金属铝和氯气作用或由无水氯化氢气体与熔融金属铝作用制得.
某课外兴趣小组在实验室中,通过下图装置制取少量纯净的无水氯化铝.
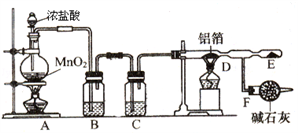
(1)A装置中发生反应的离子方程式为_____________________________;
(2)B、C装置中应盛放的试剂分别为______、______;
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,对实验产生的不良后果是___.
(4)F装置所起的作用______.
Ⅱ. 有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32﹣、SO42﹣等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图1所示:

(1)在原溶液中一定存在的离子有______;
(2)第③实验中,若取原溶液100mL,滴加NaOH溶液的物质的量浓度为0.5mol•L﹣1 ,且生成沉淀的量与加入NaOH 的量如图2所示,则该溶液中所含阳离子的浓度为_____mol•L﹣1.
-
(9分)无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝的试剂瓶久置于潮湿空气中,会自动爆炸并产生大量白雾。氯化铝常作为有机合成和石油工业的催化剂,并用于处理润滑油等。工业上由金属铝和氯气作用或由无水氯化氢气体与熔融金属铝作用制得。



某课外兴趣小组在实验室中,通过下图装置制取少量纯净的无水氯化铝。
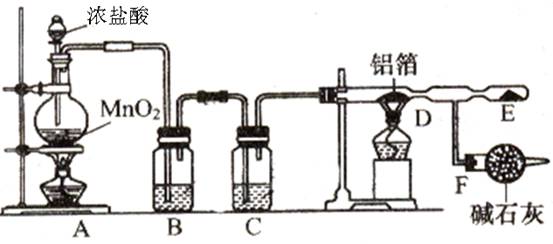
(1)A装置中发生反应的化学方程式为;
(2)B、C装置中应盛放的试剂名称分别为________、________;
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是________;
(4)F装置所起的作用是________。













