电化学降解NO3-的原理如图所示。下列说法中正确的是
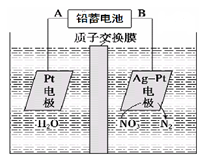
A.铅蓄电池的A极为负极,电极材料为Pb
B.铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4
C.该电解池的阴极反应为2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g
高三化学选择题中等难度题
电化学降解NO3-的原理如图所示。下列说法中正确的是

A.铅蓄电池的A极为负极,电极材料为Pb
B.铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4
C.该电解池的阴极反应为2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g
高三化学选择题中等难度题
电化学降解NO3-的原理如图所示。下列说法中正确的是

A.铅蓄电池的A极为负极,电极材料为Pb
B.铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4
C.该电解池的阴极反应为2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g
高三化学选择题中等难度题查看答案及解析
电化学降解NO3-的原理如图所示。下列说法中不正确的是

A.铅蓄电池的A极为正极,电极材料为PbO2
B.铅蓄电池工作过程中负极质量增加
C.该电解池的阴极反应为:2NO3-+ 6H2O + 10eˉ = N2↑ + 12OHˉ
D.若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(Δm左-Δm右)为10.4g
高三化学选择题中等难度题查看答案及解析
电化学降解NO3-的原理如图所示。下列说法中不正确的是
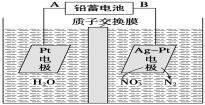
A.铅蓄电池的A极为正极,电极材料为PbO2
B.铅蓄电池工作过程中负极质量增加
C.该电解池的阴极反应为:2NO3-+ 6H2O + 10eˉ = N2↑ + 12OHˉ
D.若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(Δm左-Δm右)为10.4g
高三化学选择题中等难度题查看答案及解析
电化学降解NO3-的原理如图所示。下列说法中不正确的是
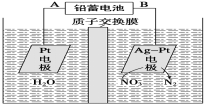
A.铅蓄电池的A极为正极,电极材料为PbO2
B.铅蓄电池工作过程中负极质量增加
C.该电解池的阴极反应为:2NO3-+ 6H2O + 10eˉ = N2↑ + 12OHˉ
D.若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(Δm左-Δm右)为10.4g
高三化学选择题中等难度题查看答案及解析
电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理如图所示,下列说法不正确的是( )
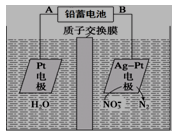
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的阴极反应式为:2NO3- + 12H+ + 10e- = N2↑ + 6H2O
C.该电解池的总反应方程式为:2H2O + 4NO3- 2N2↑+ 5O2↑ + 4OH-
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
高三化学选择题困难题查看答案及解析
电化学降解法可用于治理水中硝酸盐的污染,其工作原理如图所示。下列说法正确的是( )

A. A极为负极,电子从铂电极流向该极
B. Pt电极上发生还原反应
C. Ag-Pt电极发生的反应是:2NO3-+12H++10e-=N2↑+6H2O
D. 电解一段时间后,两池减少的质量一样多
高三化学选择题困难题查看答案及解析
电化学降解法可用于治理水中硝酸盐的污染。降解NO3—的原理如图所示。下列说法不正确的是( )
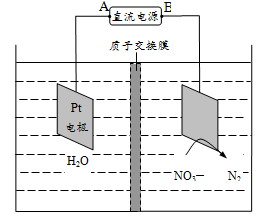
A.直流电源A为正极、B为负极
B.电解过程中质子从Pt电极向Ag-Pt电极移动
C.在阴极发生的电极反应:2NO3+10e-+12H+=N2↑+ 6H2O
D.当电解过程转移2mol电子时,阴极室质量减少5.6g
高三化学选择题中等难度题查看答案及解析
电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,下列说法不正确的是
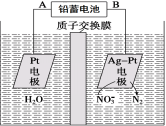
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的总反应方程式为:2H2O + 4NO3- 2N2↑+ 5O2↑ + 4OH-
C.该电解池的阴极反应式为:2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
高三化学选择题中等难度题查看答案及解析
用电解法处理含硝(NO3-)废水的原理如图所示。下列说法错误的是
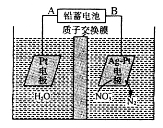
A.铅蓄电池的A极为正极,电极材料为PbO2
B.铅蓄电池放电时负极质量增加
C.该电解池的阴极反应为:2NO3-+12H++10e-==N2↑十6H2O
D.若电路中流过2 mol电子,则阳极室溶液质量减少32g(忽略气体的溶解)
高三化学选择题中等难度题查看答案及解析
用电解法处理含硝(NO3-)废水的原理如图所示。下列说法错误的是
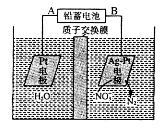
A.铅蓄电池的A极为正极,电极材料为PbO2
B.铅蓄电池放电时负极质量增加
C.该电解池的阴极反应为:2NO3-+12H++10e-==N2↑十6H2O
D.若电路中流过2 mol电子,则阳极室溶液质量减少32g(忽略气体的溶解)
高三化学选择题中等难度题查看答案及解析