-
【化学——选修2:化学与技术】联合生产是实现节能减排的重要措施,工业上合成氨和硝酸的联合生产具有重要意义。下面是工业上合成氨的简易流程:

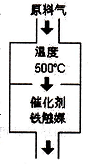
(1)设备A内部结构如右下图所示,其名称是________ ,其中发生的化学反应方程式为_________;生产中原料气必须进行脱硫,目的是____________。选择500℃进行反应的主要原因是___________;
(2)设备B的名称是冷凝塔,图中a和b是两个通水口,其中入水口是 (填“a”或“b”)。
(3)氮气和氢气的混合气体通过压缩机压缩的原因是________________________________。
(4)生产出来的NH3可以用来生产硝酸。其中在氨气催化氧化过程中,不同温度下生成产物可能有所不同,温度对氨氧化产物产率的影响如下图所示;当温度大于900℃时,NO的产率下降的主要原因是__________________。

(5)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其它损耗)的 %(保留两位有效数字)。
-
联合生产是实现节能减排的重要措施,工业上合成氨和硝酸的联合生产具有重要的意义。下面是工业上合成氨的简易流程:

(1)设备A中含有电加热器,触媒和热交换器,设备A的名称是______________,其中发生的化学反应方程式为_________________________________________________;
(2)设备B的名称是_______________,其中m和n是两个通水口,入水口是___________(填“m” 或“n”);不宜从相反方向通水的原因是__________________________________;
(3)设备C的作用是_______________________________________________。
(4)原料气中往往含有CO等杂质,在进行反应前要先净化,净化的原因是_________。
(5)氮气和氢气的混合气体通过压缩机压缩的原因是____________________________。
(6)生产出来的NH3可以用来生产硝酸。在制备硝酸的过程中,由于二氧化氮不能一次性被水完全吸收,因此生成的气体须经过多次氧化、吸收的循环操作,使其充分转化为硝酸(不考虑生产过程中的其它损失)。
①从理论上分析,要使氨气完全转化为硝酸,则原料中氧气和氨气物质的量的投料比至少为________。
②如果按理论上的原料比将原料放在特定条件的密闭容器中进行反应,所有物质不与外界交换,则最后所得溶液的质量分数为____________________。(保留三位有效数字)
-
党的十八大报告中首次提出“美丽中国”的宏伟目标。节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施,下图是几种工业生产的联合生产工艺:
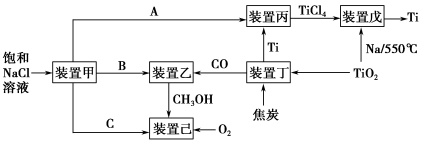
请回答下列问题:
(1)装置甲为电解池,根据图示转化关系可知:A为____________(填化学式),阴极反应式为____________。
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是_________________________________________________
装置戊进行反应时需要的环境为________(填字母序号)。
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)CH3OH(g) ΔH<0。
①该反应在不同温度下的化学平衡常数(K)如下表:
符合表中的平衡常数x的数值是________(填字母序号)。
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO) | c(H2) | c(CH3OH) |
| 0 min | 0.8 mol·L-1 | 1.6 mol·L-1 | 0 |
| 2 min | 0.6 mol·L-1 | y | 0.2 mol·L-1 |
| 4 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
| 6 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
反应从2 min到4 min之间,H2的平均反应速率为________。反应达到平衡时CO的转化率为________。反应在第2 min时改变了反应条件,改变的条件可能是________(填字母序号)。
A.使用催化剂 B.降低温度
C.增加H2的浓度
(4)装置己可以看作燃料电池,该燃料电池的负极反应式为____________ ________________________________________________。
-
节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施,下图是几种工业生产的联合生产工艺:
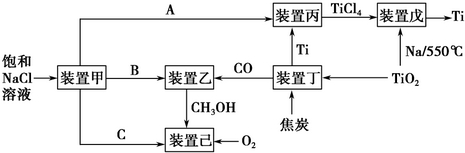
请回答下列问题:
(1)装置甲为电解池(惰性电极),根据图示转化关系可知:A为__________(填化学式),阴极反应式为__________。
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是__________装置戊进行反应时需要的环境为__________(填字母序号).
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)=CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
符合表中的平衡常数x的数值是__________(填字母序号).
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO)/mol•L-1 | c(H2)/mol•L-1 | c(CH3OH)/mol•L-1 |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
反应从2min到4min之间,H2的平均反应速率为__________,反应达到平衡时CO的转化率为__________,反应在第2min时改变了反应条件,改变的条件可能是__________(填字母序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度
-
【化学——选修2:化学与技术】(15分)研究化肥的合成、废水的处理等有现实的重要意义。
(1)硝酸铵的生产方法是采用硝酸与氨气化合,工业合成氨是一个放热反应,因此低温有利于提高原料的转化率,但实际生产中却采用400~500℃的高温,其原因是__________________;工业生产中,以氨气为原料合成硝酸,写出工业生产硝酸的最后一步的化学方程式________________________________。
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:

已知CO+H2O CO2+H2①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的
CO2+H2①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的
物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?_____________________。
(3)将工厂废气中产生的SO2通过下列流程,可以转化为有应用价值的硫酸钙等。

①写出反应Ⅰ的化学方程式:_________________________________。
②生产中,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是_____________。
③检验经过反应Ⅲ得到的氨态氮肥中 所用试剂是_______________________。
所用试剂是_______________________。
(4)工业上利用氯碱工业产品治理含二氧化硫的废气。下图是氯碱工业中电解饱和食盐水的原理示意图。

①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是____________________。
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是_________________。
-
【化学——选修2:化学与技术】研究化肥的合成、废水的处理等有现实的重要意义。
(1)硝酸铵的生产方法是采用硝酸与氨气化合,工业合成氨是一个放热反应,因此低温有利于提高原料的转化率,但实际生产中却采用400~500℃的高温,其原因是 ;工业生产中,以氨气为原料合成硝酸,写出工业生产硝酸的最后一步的化学方程式_____________。
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
已知:CO+H2O CO2+H2
CO2+H2
①甲厂以焦炭和水为原料;
②乙厂以天然气和水为原料;
③丙厂以石脑油(主要成分为C5H12)和水为原料。
按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?_____________________。
(3)将工厂废气中产生的SO2通过下列流程如图1,可以转化为有应用价值的硫酸钙等。
①写出反应Ⅰ的化学方程式: 。
②生产中,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是____________ 。
③检验经过反应Ⅲ得到的氨态氮肥中SO42﹣所用试剂是_______________________。

(4)工业上利用氯碱工业产品治理含二氧化硫的废气。图2是氯碱工业中电解饱和食盐水的原理示意图。
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是____________________。
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是_________________。
-
【化学选修2:化学与技术】
无论从能耗,还是环境,现代工业工艺往往采用联合生产的方式。工业合成氨、硝酸、纯碱可以进行联合生产。请回答下列有关问题:
(1)工业中,从合成塔出来的混合气体成分是_____________(填化学式),在进入分离器之前,需进入___________(填工业设备名称)。
(2)15mol氮气和3mol氢气在密闭容器中反应生成的氨气的物质的量_________(选填字母代号)。
a.小于2mol b.等于2mol c.大于2mol 小于15mol d.等于15mol
(3)氨气在工业制备硝酸生产中的作用是__________(用化学方程式表示):硝酸工业生产中的尾气(NO2、NO的混合气体)通常可用纯碱溶液吸收:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑,NO+NO2+Na2CO3=2NaNO2+CO2↑;尾气吸收过程中,每吸收5mol尾气,则生成CO2的物质的量为______________;
(4)硝酸厂的尾气也可利用尿素蒸汽将氨的氧化物还原为空气的主要成分而除去,写出尿素与NO2反应的化学方程式_______________________。
-
节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是( )
A.利用太阳能制氢 B.关停小火电企业
C.举行“地球一小时”熄灯活动 D.推广使用煤液化技术
-
节能减排对发展经济、保护环境有重要意义。下列不能减少二氧化碳排放的措施是
A.推广使用煤液化技术 B.关停小火电企业
C.举行““地球一小时”熄灯活动 D.利用太阳能制氢
-
节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是
A.利用太阳能制氢 B.关停小火电企业
C.举行“地球一小时”熄灯活动 D.推广使用煤液化技术










