在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是

A.0~4分钟时,A的平均反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C. 此反应的正反 应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
高二化学选择题困难题
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是

A.0~4分钟时,A的平均反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C. 此反应的正反 应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
高二化学选择题困难题
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是( )

A.0~4分钟时,A的平均反应速率为 0.01mol·L1·min1
B.由T1向T2变化时,V正>V逆
C.此反应的正反应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
高二化学选择题中等难度题查看答案及解析
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是

A.0~4分钟时,A的平均反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C. 此反应的正反 应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
高二化学选择题困难题查看答案及解析

高二化学选择题中等难度题查看答案及解析
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。
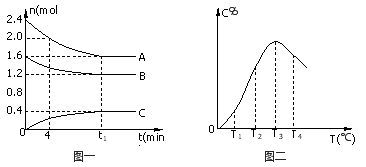
下列分析不正确的是: ( )
A. 0~4分钟时,A的平均反应速率为0.02mol/(L•min) B. 该反应的平衡常数表达式K=
C. 由T1向T2变化时,V正> V逆 D. 此反应的正反应为吸热反应.
高二化学选择题困难题查看答案及解析
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。

下列分析不正确的是:( )
A.0~4分钟时,A的速率为0.01mol/(L•min) B.由T1向T2变化时,V正> V逆
C.该反应的平衡常数表达式K= D.此反应的正反应为吸热反应.
高二化学选择题简单题查看答案及解析
在10L密闭容器中,A、B、C三种气体构成可逆反应体系,某温度下,A、B、C三者物质的量与时间的关系如图甲所示,而C的百分含量与温度的关系如图乙所示。下列说法错误的是
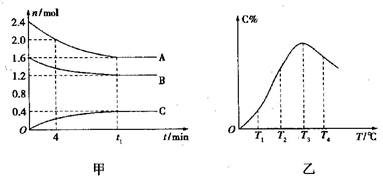
A.0-4min时,A的平均的反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,
C.此反应的正反应为吸热反应
D.其它条件不变时给平衡体系加压,达新平衡时,C的体积分数增大
高二化学选择题困难题查看答案及解析
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。
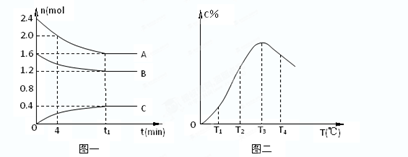
下列分析不正确的是:( )
A.此反应的正反应为吸热反应
B.由T1向T2变化时,V正> V逆
C.增大压强, 平衡向正反应方向移动
D.0~4分钟时,A的速率为0.01mol/(L•min)
高二化学选择题简单题查看答案及解析
在10L定容密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2。下列分析不正确的是

A. t1时刻前,混合气体的密度减小,t1时刻后,混合气体的密度不变
B. 该反应的平衡常数表达式
C. 由T1向T2变化时,V正> V逆
D. 此反应的正反应为放热反应
高二化学选择题困难题查看答案及解析
一定温度下,在体积为10L的密闭容器中,2molO2和2molSO2混合气体发生如下反应:2SO2(g)+ O2(g)2SO3(g),半分钟后,体系中O2的物质的量变为1.4mol,则此反应的平均速率为
A.v(O2) = 0.002mol/(L•s) B.v(SO2) = 0.002 mol/(L•s)
C.v(O2) = 0.02 mol/(L•s) D.v(SO3) = 0.04 mol/(L•s)
高二化学选择题简单题查看答案及解析
在10 L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.下列分析不正确的是 ( )

A. 该反应的平衡常数表达式为:
B. 0~4 min时,A的平均反应速率为0.01 mol/(L·min)
C. 由T1向T2变化时,v正>v逆
D. 平衡后升高温度,K值增大
高二化学选择题中等难度题查看答案及解析