-
(1)由地壳中含量最高的金属元素和非金属组成的化合物的化学式是________,该物质与氢氧化钠反应的离子方程式为________
(2)铁红常用于制造红色油漆和涂料.完成用废铁屑制备铁红的有关化学方程式:
①Fe+2HCl→FeCl2+H2↑ ②FeCl2+2NaOH→Fe(OH)2↓+2NaCl
③________④________
(3)判断存放的FeCl2溶液是否因氧化而变质.从现象观察看________;鉴定的方法为加入________试剂,若溶液出现________;则证明有________存在,鉴定反应的离子方程式________.高二化学填空题中等难度题查看答案及解析
-
下图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。已知X、Y、Z是日常生活中常见金属单质,X由地壳中含量最高的金属元素组成;D、E是常见气态非金属单质,其中D呈黄绿色。A的焰色反应呈紫色(透过蓝色钴玻璃),F的稀溶液呈蓝色。
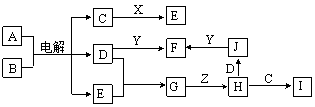
请回答下列问题:
⑴ C的电子式为 。
⑵ I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,该反应的化学方程式为 。
⑶ X与C溶液反应的离子方程式为 。
⑷ 写出J与Y反应的化学方程式,并标出电子转移的方向和数目: 。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下图所示。A为地壳
中含量仅次于氧的非金属元素的单质。

请填空:
(1)写出物质C的化学式 。
(2)写出B和碳高温反应生成A和E的化学方程式是 。
(3)写出B→D反应的离子反应方程式 。
高二化学推断题中等难度题查看答案及解析
-
已知A、B、C是中学化学常见物质,它们在一定条件下有如下转化关系:
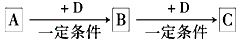
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为 .
(2)若D是由地壳中含量最多的元素组成的非金属单质,A为短周期元素中金属性最强的金属单质,则C的电子式为_____________.
(3)若D为
氯碱工业的主要产品,B是一种两性氢氧化物,则B转化为C反应的离子方程式为____________________.
(4)若D是一中常见金属,A为黄绿色气体,则C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明) .
(5)若D 是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴阳离子均含10个电子,则B转化为C的离子方程式为 .
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为 .
高二化学推断题困难题查看答案及解析
-
现有A、B、C、D、E五种物质,它们有如下反应关系:
(1)若A是由短周期中原子半径最大的元素与地壳中含量最多的元素组成的离子化合物,且两种元素的原子个数比为1:1。则A中存在的化学键是________、________。
(2)若A是可溶性强碱,B是正盐,E不溶于稀硝酸,则B的化学式为________,
(3)若A是NaHCO3,B是正盐,E既可溶于盐酸又可溶于NaOH溶液,该反应的离子方程式为________。
高二化学填空题中等难度题查看答案及解析
-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下Al2O3(s)+AlCl3(g)+3C(s) =3AlCl (g)+3CO(g) △H = a kJ·mol-1
3AlCl(g)=2Al(l)+ AlCl3 (g) △H = b kJ·mol-1
①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示)。
②Al4C3也是该反应过程中的一种中间产物。Al4C3 与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为_______________。
③甲烷和水反应可以制水煤气(混合气体),在恒温、固定体积为V升的密闭容器中的反应微观示意图如下所示,根据微观示意图得出的结论中,正确的是_____________。
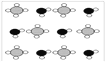
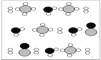
一定条件下经过t分钟达到化学平衡
a. 该反应方程式为:CH4+H2O = CO+3H2
b. 该反应平衡前后压强比为3:4
c. 该反应体系中含氢元素的化合物有3种
d. 该反应中甲烷的平衡转化率为50%
④水煤气中的H2可用于生产NH3,在进入合成塔前常用[Cu(NH3)2]Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
[Cu(NH3)2]Ac(aq) + CO(g) + NH3(g)
[Cu(NH3)3]Ac·CO(aq) △H<0
[Cu(NH3)2]Ac溶液吸收CO的适宜生产条件应是____________________。该条件下用气体表示的平衡常数表达式为:K=______________
(2)镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,一般在氩气环境中将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下可完全吸氢得到的混合物Y(含MgH2 和Al),Y在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是_________________。
②写出镁铝合金(Mg17Al12 ) 在一定条件下完全吸氢的化学方程式 _________________。
③在6. 0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17 Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2 的物质的量为_________。
高二化学填空题中等难度题查看答案及解析
-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原一氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH=a kJ·mol−1
3AlCl(g)===2Al(l)+AlCl3(g) ΔH=b kJ·mol−1
①反应Al2O3(s)+3C(s)===2Al(l)+3CO(g)的ΔH=________kJ·mol−1(用含a、b的代数式表示)。
②Al4C3是反应过程中的中间产物。Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为:_____________________________________________________。
(2)镁铝合金(Mg17Al12)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2===17MgH2+12Al。得到的混合物Y(17MgH2+12Al)在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是____________________________。
②在6.0mol·L−1 HCl溶液中,混合物Y能完全释放出H2。1mol Mg17Al12完全吸氢后得到的混合物Y与上述足量盐酸完全反应,释放出H2的物质的量为__________________。
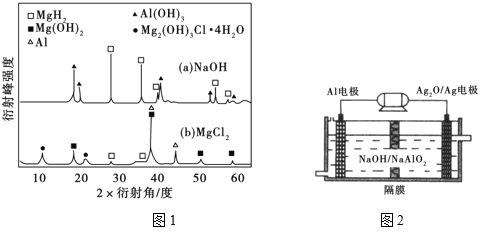
③在0.5mol·L−1 NaOH和1.0mol·L−1 MgCl2溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质的X-射线衍射谱图如图1所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。在上述NaOH溶液中,混合物Y中产生氢气的主要物质是_______________ (填化学式)。
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图2所示。该电池负极反应式为______________________________________。
高二化学综合题困难题查看答案及解析
-
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛.
(1)真空碳热还原氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g)△H=a kJ•mol﹣1
3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol﹣1
①反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H= kJ•mol﹣1(用含a、b的代数式表示).
②Al4C3是反应过程中的中间产物.Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为 .
(2)镁铝合金(Mg17Al12)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得.该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2═17MgH2+12Al.得到的混合物Y(17MgH2+12Al)在一定条件下可释放出氢气.
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是 .
②在6.0mol•L﹣1HCl溶液中,混合物Y能完全释放出H2.1mol Mg17Al12完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出H2的物质的量为 .
③在0.5 mol•L﹣1NaOH和1.0 mol•L﹣1MgCl2溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X﹣射线衍射谱图如下图所示(X﹣射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同).在上述NaOH溶液中,混合物Y中产生氢气的主要物质是 (填化学式).
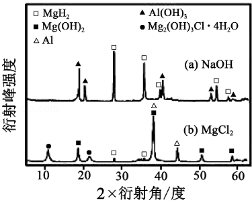
(3)铝电池性能优越,Al﹣AgO电池可用作水下动力电源,其原理如右下图(图2)所示.该电池反应的化学方程式为: .
高二化学填空题简单题查看答案及解析
-
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次递增。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D四种元素第一电离能最大的是_______________。
(2)B的氯化物的熔点比D的氯化物的熔点__________(填“高”或“低”),理由是
_______________________________________________________________________________。
(3)E的低价氧化物分子的立体构型是_________________,用KMnO4酸性溶液吸收该氧化物时,MnO4-被还原为Mn2+,该反应的离子方程式为______________________________________。
(4)F的核外电子排布式是___________。
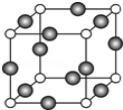
(5)A、F形成某种化合物的晶胞结构如下图所示(其中A显-3价),该化合物的化学式是_________________,若晶胞边长为a cm,阿伏伽德罗常数为NA,则该晶体的密度计算式为ρ=___________g/cm3(用含a、NA的符号表示)。
高二化学简答题困难题查看答案及解析
-
今有甲、乙、丙、丁四种元素,已知:甲元素是地壳中含量最高的元素;乙元素是金属元素,它的原子核外K、L层电子数之和等于M、N层电子数之和;丙元素的单质及其化合物的焰色反应都显黄色,氢气在丁元素单质中燃烧火焰呈苍白色。
(1)试推断并写出甲、乙、丙、丁四种元素的名称和符号______________________
(2)写出上述元素两两化合生成的化合物的化学式_____________________________
高二化学填空题简单题查看答案及解析