-
化学兴趣小组对品红溶液褪色实验进行探究.限选实验仪器与试剂为:试管、滴管、试管夹、1.0mol•L-1 Na2SO3溶液、1.0mol•L-1 NaClO溶液、品红溶液.
[探究一]
①甲同学提出假设
假设1:NaClO溶液能使品红溶液褪色
假设2:Na2SO3溶液能使品红溶液褪色
假设3:______.
②设计实验方案证明甲的假设
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量品红溶液于试管中,再加入少量的______. | 若品红溶液褪色,则假设1成立. |
步骤2:______
______
______. | 若______,则假设2成立. |
| 根据步骤1、2. | 若______,则假设3成立. |
[探究二]
乙同学为探究Na2SO3溶液是否发生变质,设计如下实验测定所用1.0mol•L-1 Na2SO3溶液的实际浓度:
(1)分液漏斗中应加入足量的下列试剂______(填序号).
a.浓硝酸b.65%硫酸 c.浓盐酸
(2)实验前后测得C装置增重 3.2g,则Na2SO3溶液实际的物质的量浓度为______.
(3)该实验装置还存在一个明显的缺陷是:______.
-
为探究Na2SO3溶液的性质,某学习小组设计了一系列实验,并记录实验现象。具达如下表所示。
| 实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
| 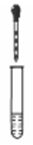
| ① | 0.2mol/LNa2SO3溶液 | 品红溶液 | 红色消失 |
| ② | 饱和Ag2SO4举泫 | 产生白色沉淀 |
| ③ | 0.2mol/L CuSO4溶液 | 溶液先变绿,继续滴加产生砖红色沉淀 |
| ④ | 0.lmol/L Al2(SO4)溶液 | 开始无明显现象,继续滴加产生白色沉淀,并有刺激性气味的气体生成 |
则以下说法不正确的是( )
A. Na2SO3溶液具有漂白性
B. Ksp(Ag2SO4)<Ksp(Ag2SO3)
C. 实验③,SO32-与Cu2+发生了氧化还原反应
D. 实验④发生反应的离子方程式为:3SO32-+2Al3++3H2O=2Al(OH)3↓+3SO2↑
-
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
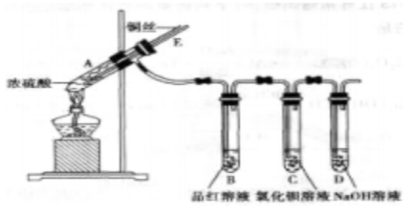
实验步骤:
①先连接好装置,检查气密性,再加入试剂;
②加热A试管,B中品红溶液褪色,熄灭酒精灯;
③将铜丝向上抽动离开液面。
(1)试管中发生反应的化学方程式为_____________________________.
(2)能够证明铜与浓硫酸反应生成气体的现象_________________________.
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其分成两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应的位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | __________ | ______________ |
写出其中SO2显示还原性的反应的离子方程式___________________.
(4)实验完毕后,先熄灭酒精灯,由于导管E存在,B中的液体不会倒吸入A中,其原因是___________________________________________.
(5)实验完毕后,装置中残留气体有毒,不能打开胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是_______________________.
-
(8分)某化学兴趣小组,拟探究和比较SO2和C12的漂白性,设计如下图所示的实验装置二套。请你参与探究并回答下列问题。

(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理________(填“相同”或“不相同”);
(4) C12通入品红溶液中,生成的具有漂白性的物质是________(填“HC1”或“HClO”)。
-
某化学小组进行Na2SO3 的性质实验探究。
(1)在白色点滴板的a、b、c三个凹槽中滴有Na2SO3 溶液,再分别滴加下图所示的试剂:
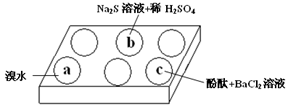
实验现象如下表:
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
根据实验现象进行分析:
① a中实验现象证明Na2SO3具有________性。
② b中发生反应的离子方程式是。
③ 应用化学平衡原理解释c中现象(用化学用语及简单文字表述)________。
(2)在用NaOH 溶液吸收SO2 的过程中,往往得到Na2SO3和NaHSO3 的混合溶液,溶液pH 随n(SO32-):n(HSO3-) 变化关系如下表:
| n(SO3 2—): n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
① 当吸收液中n(SO32-):n(HSO3-) =10:1 时,溶液中离子浓度关系正确的是________(填字母)。
A.c(Na+) +c(H+) = 2c(SO32-) +c(HSO3-) + c(OH-)
B.c(Na+) > c(HSO3-) > c(SO32-) > c(OH-)>c(H+)
C.c(Na+) > c(SO32-) > c(HSO3-) > c(OH-)>c(H+)
② 若n(SO32-):n(HSO3-) = 3:2,则0.8 mol NaOH溶液吸收了标准状况下的SO2 ________ L。
-
某化学小组进行Na2SO3的性质实验探究。
在白色点滴板的a、b、c三个凹槽中滴有Na2SO3溶液,再分别滴加下图所示的试剂:
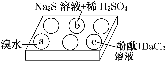
实验现象如下表:
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
根据实验现象进行分析:
(1)a中实验现象证明Na2SO3具有________性。
(2)b中发生反应的离子方程式是_____________________________________________
(3)应用化学平衡原理解释c中现象(用化学用语及简单文字表述)__________________________________________________________。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
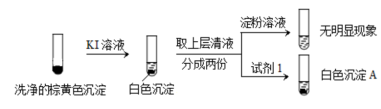
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32−的理由是_______________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和____________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i. Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
将对比实验方案补充完整。
步骤一:
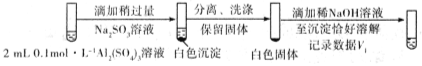
步骤二:

则V1___________V2(填>,<或=)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+  Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+  CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
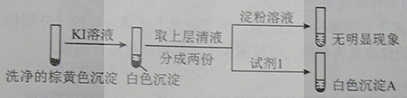
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32−的理由是___________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.呗Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
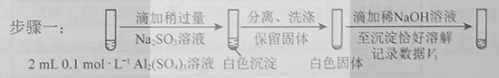
步骤二:_____________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4溶液 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
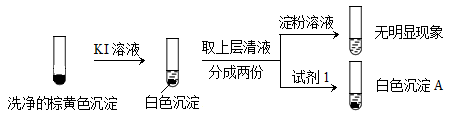
KI溶液 洗净的棕黄色沉淀 取上层清液 分成两份 淀粉溶液 试剂1 无明显现象
白色沉淀A
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu2+和SO32−的理由是___________。
(3)已知:Al2(SO4)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.被Al(OH)3所吸附;
ii.存在于铝的碱式盐中。
对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
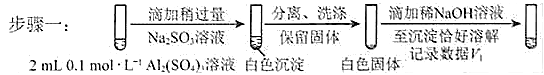
步骤二:_____________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液为实验对象,可探究盐的性质和盐溶液间反应的多样性
| 实验 | 试剂 | 现象 | 检验 结果 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 | 产物为Ag2SO3 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | 产物含Cu+、Cu2+和SO32− |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | 产物为 Al(OH)SO3 |
下列说法不正确的是
A. 现象Ⅰ对应的离子方程式:Ag2SO4(s) + SO32−(aq) === Ag2SO3(s) + SO42−(aq)
B. 用稀硫酸证实Ⅱ沉淀中含有Cu+的实验现象是析出红色固体
C. 现象Ⅲ中白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色
D. 上述实验现象涉及了亚硫酸盐的溶解性、氧化还原性及其水溶液的酸碱性










 Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ 



